
高一化学寒假作业及答案高一寒假作业 化学(七) Word版含答案
展开一.选择题(共7小题,每个小题只有一个正确选项)
1.下列实验方法错误的是( )
2.下列有关实验的做法不正确的是( )
3.由C16O和C18O组成的混合气体与同温、同压下空气(平均相对分子质量为29)的密度相同,则下列关系正确的是( )
4.能正确表示下列反应的离子方程式的是( )
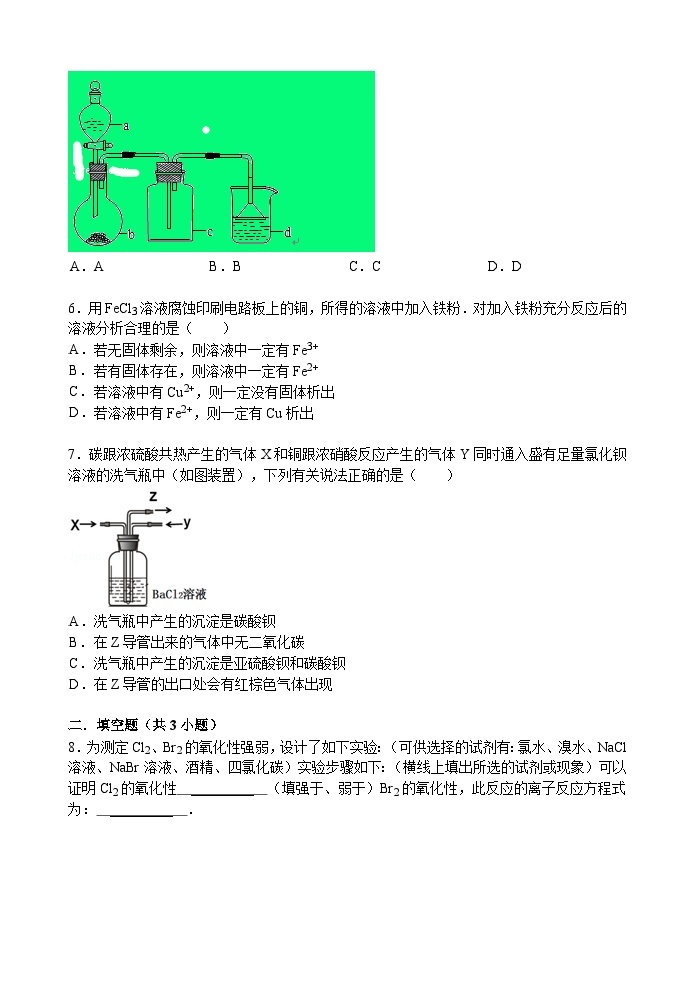
5.实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )
6.用FeCl3溶液腐蚀印刷电路板上的铜,所得的溶液中加入铁粉.对加入铁粉充分反应后的溶液分析合理的是( )
7.碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是( )
二.填空题(共3小题)
8.为测定Cl2、Br2的氧化性强弱,设计了如下实验:(可供选择的试剂有:氯水、溴水、NaCl溶液、NaBr溶液、酒精、四氯化碳)实验步骤如下:(横线上填出所选的试剂或现象)可以证明Cl2的氧化性 _________ (填强于、弱于)Br2的氧化性,此反应的离子反应方程式为: _________ .
9.某学生利用以下装置探究纯净干燥的氯气与氨气之间的反应.
回答下列问题:
(1)根据下列所给试剂,选择制取氨气的装置是(填对应字母) _________ ;写出制备氯气的离子反应方程式 _________ .
二氧化锰、碱石灰、浓盐酸、浓氨水、烧碱、生石灰
(2)已知,E装置是用于使纯净干燥的氯气与氨气发生反应的装置,试说明该装置的设计意图: _________ .
(3)根据实验目的,所选装置的连接顺序为(填装置的接口字母): _________ 接 _________ , _________ 接( f ),( g )接 _________ , _________ 接 _________ , _________ 接 _________ ;其中,G装置的作用是 _________ .
(4)氯气和氨气在常温下相混合就会发生反应生成氯化铵和氮气,该反应的化学方程式为: _________ ;其中,氧化剂与还原剂的物质的量之比是 _________ .
(5)请你评价此套装置有何缺点 _________ .
10.利用图进行浓硫酸与铜反应,并验证二氧化硫的性质.
实验操作如下:连接仪器和安放药品,用酒精灯加热1分钟后撤去酒精灯,将铜丝伸入液面以下,一段时间后拉起铜丝.
请回答下列问题:
(1)将反应后的试管充分静置,观察到试管底部有白色固体出现,中间层是浅黄色液体(浓硫酸),上层是蓝色溶液.白色固体的化学式为 _________ ,上述现象中体现了浓硫酸的性质有 _________ (填序号)
①酸性 ②强氧化性 ③吸水性 ④脱水性
(2)直玻璃管中依次观察到的现象是: _________ ; _________ ; _________ .
(3)某次实验中小烧杯中澄清石灰水始终未观察到浑浊,你猜想可能的原因是 _________ ,请设计实验证明它. _________ .
(4)某学生发现,常温下将铜片长时间放入浓硫酸的试管中并密封,最终生成黑色物质(Cu2S)和蓝色溶液,无气体生成,写出此条件下铜片与浓硫酸反应的化学方程式: _________ .
参考答案
一 选择题
1.B 2.D 3.B 4.D 5.B 6.B 7.D
A.
用丁达尔效应鉴别葡萄糖溶液和蛋白质溶胶
B.
用澄清石灰水鉴别SO2和CO2
C.
用过量的NaOH溶液鉴别AlCl3溶液和MgCl2溶液
D.
用加热后称量其质量是否变化鉴别Na2CO3和NaHCO3固体
A.
分液时,分液漏斗中的上层液体应由上口倒出
B.
用加热分解的方法区分碳酸钠和碳酸氢钠两种固体
C.
配置0.1000 ml•L﹣1氯化钠溶液时,将液体转移到容量瓶中需用玻璃棒引流
D.
检验NH4+时,往试样中加入NaOH溶液,微热,用湿润的蓝色石蕊试纸检验逸出的气体
A.
混合气体中C16O和C18O的分子数之比为14:15
B.
混合气体中C16O和C18O的物质的量之比为1:1
C.
混合气体中C16O和C18O的质量之比为15:14
D.
混合气体中C16O和C18O的密度之比为1:1
A.
Cl2通入NaOH溶液:Cl2+OH﹣═Cl﹣+ClO﹣+H2O
B.
NaHCO3溶液中加入稀HCl:CO32﹣+2H+═CO2↑+H2O
C.
AlCl3溶液中加入过量稀氨水:Al3++4NH3•H2O═AlO2﹣+4NH4++2H2O
D.
Cu溶于稀HNO3:3Cu+8H++2NO3﹣═3Cu2++2NO↑+4H2O
选项
a中的物质
b中的物质
c中收集的气体
d中的物质
A
浓氨水
CaO
NH3
H2O
B
浓硫酸
Na2SO3
SO2
NaOH溶液
C
稀硝酸
Cu
NO2
H2O
D
浓盐酸
MnO2
Cl2
NaOH溶液
A.
A
B.
B
C.
C
D.
D
A.
若无固体剩余,则溶液中一定有Fe3+
B.
若有固体存在,则溶液中一定有Fe2+
C.
若溶液中有Cu2+,则一定没有固体析出
D.
若溶液中有Fe2+,则一定有Cu析出
A.
洗气瓶中产生的沉淀是碳酸钡
B.
在Z导管出来的气体中无二氧化碳
C.
洗气瓶中产生的沉淀是亚硫酸钡和碳酸钡
D.
在Z导管的出口处会有红棕色气体出现
二. 8.
强Cl2+2Br﹣=Br2+2Cl﹣
(4
9.
(1)A; MnO2+4H++2C1﹣Mn2++C12↑+2H2O;
(2)将比空气轻的氨气从长管口f进入,比空气重的氯气从短管口g进入,使反应气体逆流接触充分反应,中间导管用于排出空气以减少内部压力;
(3)a;d;e;h;i;j;k;b;除去C12中的HCl气体;
(4)3C12+8NH3=6NH4Cl+N2;3:2;
(5)缺少尾气处理装置,造成空气污染
10.
(1)CuSO4;①②③;
(2)蓝色石蕊试纸变为红色;红色滤纸变为白色;紫红色滤纸变为白色;
(3)SO2易溶于水,大量SO2与Ca(OH)2生成易溶于水的Ca(HSO3)2而不产生CaSO3浑浊;取小烧杯中溶液少许于另一支试管中,加入足量NaOH溶液,若有白色沉淀生成,则证明猜想合理;
(4)5Cu+4H2SO4(浓)=Cu2S+3CuSO4+4H2O.
高一化学寒假作业及答案高一寒假作业 化学(十) Word版含答案: 这是一份高一化学寒假作业及答案高一寒假作业 化学(十) Word版含答案,共14页。
高一化学寒假作业及答案高一寒假作业 化学(一) Word版含答案: 这是一份高一化学寒假作业及答案高一寒假作业 化学(一) Word版含答案,共14页。
高一化学寒假作业及答案高一寒假作业 化学(九) Word版含答案: 这是一份高一化学寒假作业及答案高一寒假作业 化学(九) Word版含答案,共14页。












