
高一化学寒假作业及答案高一寒假作业 化学(九) Word版含答案
展开一.选择题(共7小题,每个小题只有一个正确选项)
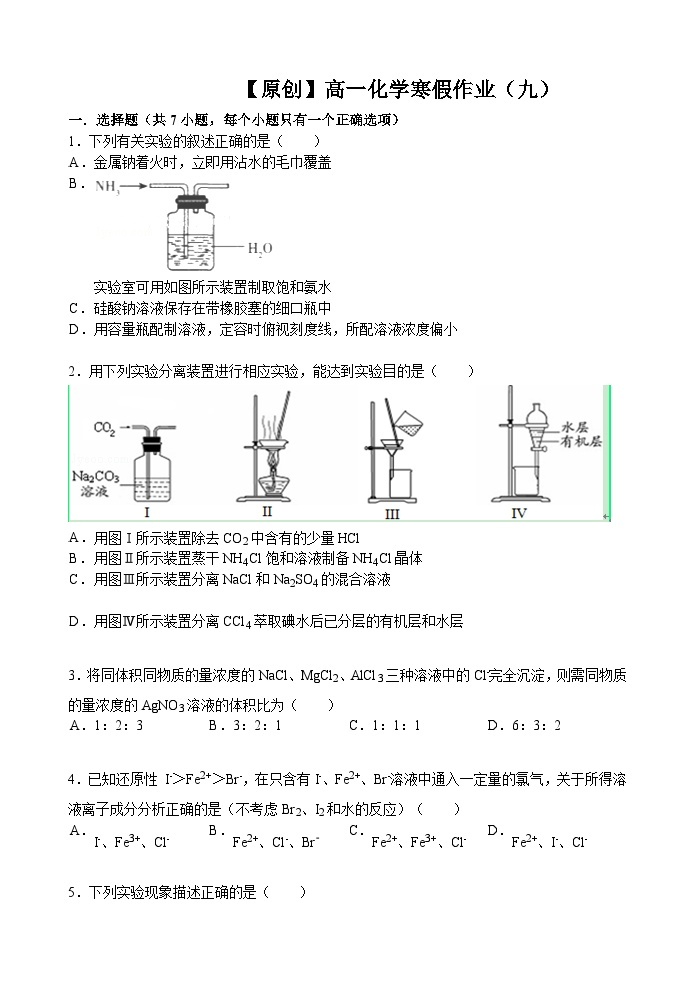
1.下列有关实验的叙述正确的是( )
2.用下列实验分离装置进行相应实验,能达到实验目的是( )
3.将同体积同物质的量浓度的NaCl、MgCl2、AlCl3三种溶液中的Cl﹣完全沉淀,则需同物质的量浓度的AgNO3溶液的体积比为( )
4.已知还原性 I﹣>Fe2+>Br﹣,在只含有I﹣、Fe2+、Br﹣溶液中通入一定量的氯气,关于所得溶液离子成分分析正确的是(不考虑Br2、I2和水的反应)( )
5.下列实验现象描述正确的是( )
6.下列反应所得溶液中只含一种溶质的是( )
7.下列物质中既能跟稀H2SO4反应,又能跟氢氧化钠溶液反应的是( )
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al ⑤Na2CO3.
二.填空题(共3小题)
8.实验室需要0.1ml/L NaOH溶液450mL和0.5ml/L硫酸溶液480mL.根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液需要的是 _________ (填字号),配制上述溶液还需用到的玻璃仪器是 _________ (填仪器名称).
(2)下列操作中,是容量瓶所具备的功能有 _________ .
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.配制任意浓度和体积的标准溶液
D.稀释某一浓度的溶液
E.量取一定体积的液体
(3)根据计算用托盘天平称取NaOH的质量为 _________ g.在实验中其他操作均正确,若定容时俯视刻度线,则所得溶液浓度 _________ (填“大于”“等于”或“小于”)O.1ml/L.若NaOH溶液在转移至容量瓶时,洒落了少许,则需要如何操作: _________ .
(4)根据计算得知,所需质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为 _________ ml.如果实验室有10mL,15mL,20mL量筒,应选用 _________ mL的量筒最好.配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是 _________ .
(5)下列操作会使配制的NaOH溶液浓度偏低的是 _________ .
A.用滤纸称量NaOH
B.选用的容量瓶内有少量蒸馏水
C.定容摇匀后,液面下降,又加水至刻度线
D.整个配制过程中,容量瓶不振荡.
9.下列框图涉及到的物质所含元素中,除一种元素外,其余均为1~18号元素.
已知:A、F为无色气体单质,B为具有刺激性气味的气体,C为黑色氧化物,E为红色金属单质(部分反应的产物未列出).请回答下列问题:
(1)B和C反应的化学方程式为 _________ .
(2)E与G的稀溶液反应的离子方程式为 _________ .
(3)J、K是同种金属的不同氯化物,K为白色沉淀.写出SO2还原J生成K的离子方程式 _________ .
10.利用图进行浓硫酸与铜反应,并验证二氧化硫的性质.
实验操作如下:连接仪器和安放药品,用酒精灯加热1分钟后撤去酒精灯,将铜丝伸入液面以下,一段时间后拉起铜丝.
请回答下列问题:
(1)将反应后的试管充分静置,观察到试管底部有白色固体出现,中间层是浅黄色液体(浓硫酸),上层是蓝色溶液.白色固体的化学式为 _________ ,上述现象中体现了浓硫酸的性质有 _________ (填序号)
①酸性 ②强氧化性 ③吸水性 ④脱水性
(2)直玻璃管中依次观察到的现象是: _________ ; _________ ; _________ .
(3)某次实验中小烧杯中澄清石灰水始终未观察到浑浊,你猜想可能的原因是 _________ ,请设计实验证明它. _________ .
(4)某学生发现,常温下将铜片长时间放入浓硫酸的试管中并密封,最终生成黑色物质(Cu2S)和蓝色溶液,无气体生成,写出此条件下铜片与浓硫酸反应的化学方程式: _________ .
参考答案
一 选择题
1.C 2.D 3.A 4.B 5.B 6.B 7.A
A.
金属钠着火时,立即用沾水的毛巾覆盖
B.
实验室可用如图所示装置制取饱和氨水
C.
硅酸钠溶液保存在带橡胶塞的细口瓶中
D.
用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小
A.
用图Ⅰ所示装置除去CO2中含有的少量HCl
B.
用图Ⅱ所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
C.
用图Ⅲ所示装置分离NaCl和Na2SO4的混合溶液
D.
用图Ⅳ所示装置分离CCl4萃取碘水后已分层的有机层和水层
A.
1:2:3
B.
3:2:1
C.
1:1:1
D.
6:3:2
A.
I﹣、Fe3+、Cl﹣
B.
Fe2+、Cl﹣、Br‑
C.
Fe2+、Fe3+、Cl﹣
D.
Fe2+、I﹣、Cl﹣
A.
氯化氢与氨气相遇,有大量的白雾生成
B.
用铂丝蘸取硫酸钠溶液灼烧,火焰呈黄色
C.
氯化亚铁溶液与无色的KSCN溶液混合,溶液呈红色
D.
SO2通入品红溶液,红色褪去,再加热,红色不再出现
A.
AlCl3溶液中滴入过量NaOH溶液
B.
Fe2(SO4)3溶液中加入过量铁粉
C.
稀HNO3中加入少量铜片
D.
Ca(ClO)2溶液中通入过量CO2
A.
①②③④
B.
②③④
C.
②③④⑤
D.
全部
二. 8.
(1)BDE;烧杯和玻璃棒;
(2)A;
(3)A; 2.0; 大于;重新配置;
(4)13.6;15;将浓硫酸沿烧杯内壁缓缓倒入水中,并用玻璃棒不断搅拌;
(5)AC.
9.
(1) 3CuO+2NH33Cu+N2+3H2O;
(2)3Cu+8H++2NO3﹣=3Cu2++2NO↑+4H2O;
(3)2Cu2++2Cl﹣+SO2+2H2O=2CuCl↓+4H++SO42﹣.
10.
(1)CuSO4;①②③;
(2)蓝色石蕊试纸变为红色;红色滤纸变为白色;紫红色滤纸变为白色;
(3)SO2易溶于水,大量SO2与Ca(OH)2生成易溶于水的Ca(HSO3)2而不产生CaSO3浑浊;取小烧杯中溶液少许于另一支试管中,加入足量NaOH溶液,若有白色沉淀生成,则证明猜想合理;
(4)5Cu+4H2SO4(浓)=Cu2S+3CuSO4+4H2O.
高一化学寒假作业及答案高一寒假作业 化学(七) Word版含答案: 这是一份高一化学寒假作业及答案高一寒假作业 化学(七) Word版含答案,共14页。
高一化学寒假作业及答案高一寒假作业 化学(十) Word版含答案: 这是一份高一化学寒假作业及答案高一寒假作业 化学(十) Word版含答案,共14页。
高一化学寒假作业及答案高一寒假作业 化学(一) Word版含答案: 这是一份高一化学寒假作业及答案高一寒假作业 化学(一) Word版含答案,共14页。












