




第07讲 物质的量 阿伏加德罗常数-2023-2024学年新高一化学暑假精品课(沪科版必修第一册)
展开第07讲 物质的量 阿伏加德罗常数
1. 物质的量
(1)意义:国际单位制中7个基本物理量之一,它表示含有一定数目粒子的集合体。
(2)符号:n
(3)单位:摩尔,简称摩,符号为mol
说明:①“物质的量”是一个基本物理量,这四个字是一个整体,不能有任何增减。②摩尔是单位,不是物理量。③物质的量只能用于计量微观粒子,不能用于计量宏观物体。④使用物质的量时,要指明微粒的种类,如,不能说“1摩尔氢”,只能说“1摩尔氢原子”,或“1摩尔氢分子”,或“1摩尔氢离子”。
【例1】下列关于物质的量的说法中正确的是
A.摩尔是国际单位制中的一个物理量
B.物质的量是指物质中所含微粒的个数
C.物质的量就是物质的质量
D.物质的量只能计量微观粒子
【例2】下列说法正确的是
A.物质的量可以理解为物质的质量
B.物质的量就是物质的粒子数目
C.物质的量是量度物质所含微观粒子多少的一个物理量
D.物质的量的单位——摩尔只适用于分子
2.阿伏伽德罗常数
(1)定义:1mol任何粒子含有的粒子数叫做阿伏加德罗常数。
(2)数值:1 mol精确包含6.022 140 76×1023个基本单元,该数称为阿伏加德罗常数(NA)。
(3)符号:NA
(4)单位:mol-1 (每摩尔)
(5)表达式:NA≈6.02×1023 mol-1
(6)计算公式:N=n · NA (其中n表示物质的量,NA表示阿伏加德罗常数,N表示粒子数)
说明:①这里指的基本单元可以是原子、分子、离子、电子、其他任意微粒或微粒的特定组合。②国际上曾规定,0.012 kg 12C含有的碳原子数为阿伏加德罗常数,现在我们使用的是精确测定的结果进行定义的。虽是常数,也有单位。
【例3】下列关于阿伏加德罗常数的说法错误的是
A.6.02×1023就是阿伏加德罗常数
B.0.012 kg12C含有的碳原子数就是阿伏加德罗常数
C.阿伏加德罗常数有单位
D.1mol氨气所含的原子数约为2.408×1024
【例4】22 g CO2 含有x个原子,则阿伏加德罗常数的值为
A.2x B. C. D.x
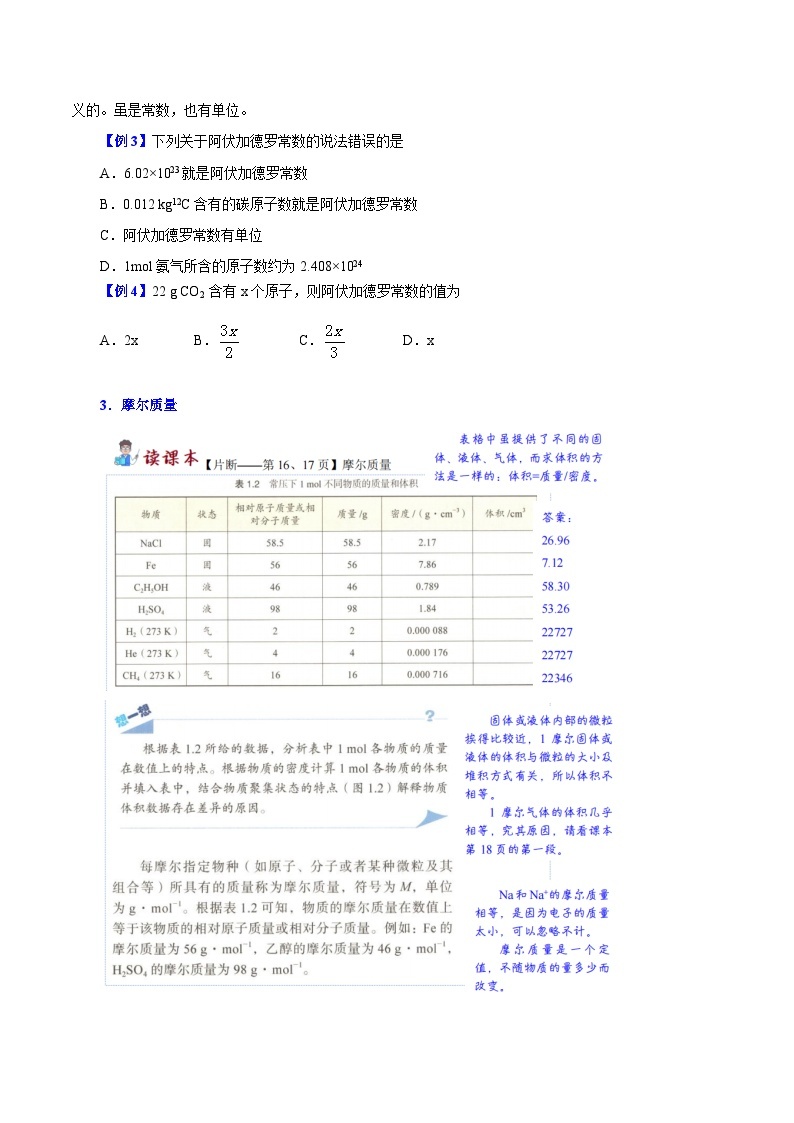
3.摩尔质量
(1)定义:单位物质的量的物质所具有的质量。
(2)符号:M。
(3)单位:g∙mol-1或g/mol。
(4)数值:l mol任何粒子或物质的摩尔质量以g/mol为单位时,其数值等于该粒子的相对原子(分子)质量。
(5)计算公式:m= n· M(其中n表示物质的量,m表示物质的质量,M表示摩尔质量)
【例5】已知32 g X与40 g Y恰好完全反应,生成0.5 mol Q和9 g R。则Q的摩尔质量是
A. 63 g ·mol-1 B. 122 g ·mol-1 C. 126 g ·mol-1 D. 144 g ·mol-1
【例6】填写下表:
物质 | 物质的量/mol | 分子数 (用数值表示) | 原子总数 (用NA表示) | 质量/g | 摩尔质量/g·mol-1 |
H2O | 2 |
|
|
|
|
H2SO4 |
| 3.01×1022 |
|
|
|
N2 |
|
|
| 14 |
|
4.物质的量应用于化学方程式的计算
在化学变化时,可以通过化学反应中反应物与生成物之间微粒的计量数之比,直接知道它们之间的物质的量之比。即化学方程式中,各微粒的个数之比等于它们的物质的量之比。
【例7】在一定体积的容器中,加入1.5 mol 氙气(Xe)和7.5 mol氟气(F2),在一定条件下充分反应后,容器内除得到一种无色晶体外,还余下4.5 mol氟气。则所得无色晶体中,氙与氟的原子个数比是 。
【例8】MgCl2·xH2O的晶体2.03g与足量的硝酸银溶液反应,生成沉淀2.87 g,则MgCl2·xH2O晶体中x的数值为
A. 2 B. 4 C. 6 D. 8
5.物质的量应用于化学式的计算
在化学式中,各微粒的个数之比等于它们的物质的量之比。
【例9】有一种氮的氧化物,氮元素与氧元素的质量比为7∶4,则该氧化物中氮元素的化合价为
A.+4 B.+1 C.+3 D.+5
【例10】0.2 mol A2和0.6 mol B2完全反应生成0.4 mol的化合物C,则C的化学式为
A.AB B.AB2 C.AB3 D.AB4
1.下列关于摩尔的说法中正确的是
A.摩尔是物理量之一 B.摩尔是物质的量的单位
C.摩尔是表示物质结构微粒的数量单位 D.摩尔是以克为单位的质量单位
2.Cl2的摩尔质量是
A.35.5g·mol-1 B.71 g·mol-1 C.35.5g·mol D.71 g·mol
3.与12.8 g SO2所含有原子数相等的NO的质量为
A.3.0g B.6.0g C.9.0g D.18.0g
4.一个27Al原子的质量约为
A.27g B.27×6.02×1023g
C.27×6.02×10—23g D.27×g
5.在0.3 mol NO2中,含有的原子数为
A.0.2NA B.0.3NA C.0.6NA D.0.9NA
6. 用NA表示阿伏加德罗常数,下列说法正确的是
A.摩尔是一个基本物理量
B.含有2NA个氢原子的水,其物质的量为1 mol
C.0.5 mol氧气所含氧元素为NA
D.2 mol NaCl中含离子数2NA
7.准确理解概念内涵才能准确把握概念本质,下列有关1 mol的含义叙述中错误的是
A. 1mol任何物质都含有6.02×1023个分子
B. 16 g O2约含有6.02×1023个氧原子
C. 4mol H2O中含有8molH和4molO
D. 1molNe中含有6.02×1024个电子
8.下列物质所含原子数与0.2 mol H3PO4所含原子数相等的是
A. 0.4 mol H2O2 B. 0.2 mol H2SO4 C. 0.8 mol CO2 D. 0.3 mol HNO3
9.下列有关阿伏加德罗常数(NA)的说法错误的是
A.32 g O2所含的原子数目为NA
B.0.5 mol H2O含有的原子数目为1.5NA
C.1 mol H2O含有的H2O分子数目为NA
D.0.5NA个氯气分子的物质的量是0.5 mol
10.已知硫酸中含有3.01×1023个氧原子,硫酸的物质的量是
A.0.500 mol B.1.00 mol C.0.250 mol D.0.125 mol
11. 0.5 mol O2中所含的氧原子数目为
A.3.01×1023个 B.6.02×1023 个 C.0.5个 D.1个
12. 光纤通信是一种现代化的通信手段,制造光导纤维的主要原料是SiO2,下列关于SiO2的说法正确的是
A.SiO2的摩尔质量是60
B.1 mol SiO2中含有1 mol O2
C.1.5 mol SiO2中含有1.806×1024个氧原子
D.1 mol SiO2的质量是60 g·mol-1
13.如果1g水中含有n个氢原子,则阿伏加德罗常数是
A.1/n mol-1 B.9n mol-1 C.2n mol-1 D.n mol-1
14.1个O原子的质量为m克,若阿伏伽德罗常数为NA,下列表示1个C原子质量
A.16/NA 克 B.m/12 克 C.3m/4 克 D.m NA 克
15.下列叙述错误的个数是
①1molH2O中含有1mol氢分子和1mol氧原子
②1mol任何物质都含有约6.02×1023个分子
③6.02×1023就是阿伏加德罗常数
④氢原子的摩尔质量是1g
⑤HCl的摩尔质量等于1molHCl分子的质量
A.2 B.3 C.4 D.5
16.常温下20滴水为1mL,水的密度为1g/mL,每滴水含有a个水分子,则阿伏德罗常数可表示为
A. a B. 2a C. 18a D. 360a
17.下列物质中含原子数最多的是
A.6.02×1023个H2SO4 分子 B.0.4 mol NH3
C.10 g氖气 D.4℃时5.4 mL水
18.40.5 g某金属氯化物RCl2含有0.6 mol氯离子,则金属R的摩尔质量为
A.135g B.135g·mol−1 C.64 D.64g·mol−1
19.下列说法正确的是
A.1 mol H2O中含有2 mol氢和1mol氧
B.CH4的摩尔质量为16 g
C.32 g SO2含有的分子数约为3.01×1023个
D.1 mol任何物质含有的微粒数都相同
20.下列说法正确的是
A.1 mol氢约含有6.02×1023个微粒
B.H2的摩尔质量是2 g
C.1mol O2的质量是32 g,含有的氧原子数为2NA
D.2NA个H2SO4的摩尔质量为196 g/mol
21.1.2 mol Cl2与元素A单质完全反应生成0.60 mol AClx,则x值为
A.1 B.2 C.3 D.4
22.(1)1.204×1024个CO2分子的摩尔质量是_______________。
(2)用NA表示阿伏加德罗常数的值,则0.3 mol HF中所含质子数与_____个CH4中所含质子数相等。
23.(1)0.5molO2中的氧气分子数目是___________。
(2)1molNH3中的氢原子数目是___________。
(3)1.5molNa2CO3中Na+的数目是___________。
(4)1.204×1023个CH4分子的物质的量___________。
(5)6.02×1023个氧原子中所含的质子数目是___________。
沪科技版(2020)必修第一册物质的量 阿伏加德罗常数达标测试: 这是一份沪科技版(2020)必修第一册物质的量 阿伏加德罗常数达标测试,共9页。试卷主要包含了单选题,填空题,实验题等内容,欢迎下载使用。
高中化学沪科技版(2020)必修第一册物质的量 阿伏加德罗常数精品一课一练: 这是一份高中化学沪科技版(2020)必修第一册物质的量 阿伏加德罗常数精品一课一练,文件包含同步讲义高中化学沪科版2020必修第一册--121物质的量阿伏加德罗常数学生版docx、同步讲义高中化学沪科版2020必修第一册--121物质的量阿伏加德罗常数教师版docx等2份试卷配套教学资源,其中试卷共24页, 欢迎下载使用。
高中化学沪科技版(2020)必修第一册物质的量 阿伏加德罗常数优秀达标测试: 这是一份高中化学沪科技版(2020)必修第一册物质的量 阿伏加德罗常数优秀达标测试,文件包含121物质的量阿伏加德罗常数教师版-2023-2024学年高一化学同步精品讲义沪科版2020必修第一册docx、121物质的量阿伏加德罗常数学生版-2023-2024学年学年高一化学同步精品讲义沪科版2020必修第一册docx等2份试卷配套教学资源,其中试卷共45页, 欢迎下载使用。












