





高中化学苏教版 (2019)必修 第一册第二单元 溶液组成的定量研究获奖课件ppt
展开1.了解物质的量浓度的含义、计算公式(重点)2.学会配制一定物质的量浓度溶液的实验技能(重点)3.物质的量浓度在化学反应计算中的应用(难点)
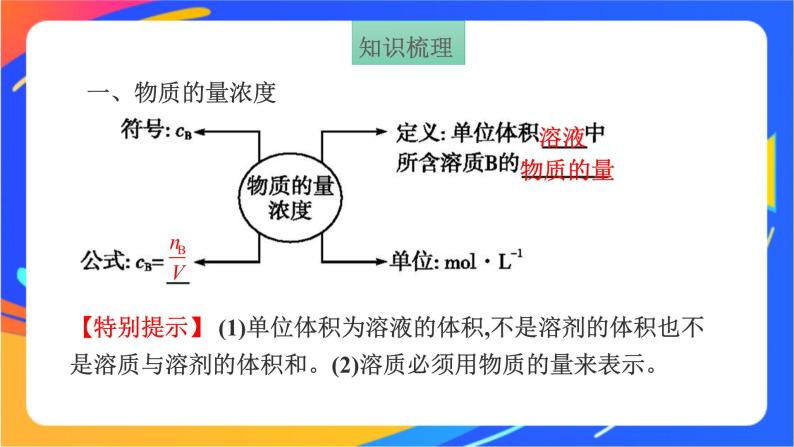
【特别提示】 (1)单位体积为溶液的体积,不是溶剂的体积也不是溶质与溶剂的体积和。(2)溶质必须用物质的量来表示。
二、容量瓶1.用途:配制一定______、一定______的溶液。
50mL、100mL、250mL、500mL
3.读数:溶液的_______正好与刻度线_______时,容量瓶中溶液的体积即为容量瓶上所标记体积。【思考1】 容量瓶使用前首先进行的操作是什么?提示:容量瓶使用前首先检查是否漏水。三、一定物质的量浓度溶液的配制以配制100 mL 0.100 ml·L-1 Na2CO3溶液为例1.主要仪器托盘天平、药匙、烧杯、玻璃棒、_____________、胶头滴管。2.配制步骤(1)计算:所需要Na2CO3固体的质量为 g。(2)称量:用托盘天平准确称取Na2CO3固体。
(3)溶解:将Na2CO3固体转移至100 mL烧杯中,加适量蒸馏水溶解,并冷却至 。(4)转移:用_______引流,将溶液转移到 中。(5)洗涤:用蒸馏水洗涤 和 2~3次,将洗涤液全部转移到 中。轻轻振荡容量瓶,使溶液混合均匀。(6)定容:先加蒸馏水至接近刻度线_______处,再改用________滴加蒸馏水至溶液凹液面正好与刻度线相切。(7)摇匀:盖好瓶塞,反复 颠倒,使溶液混合均匀。【思考2】 容量瓶用蒸馏水洗净后,不干燥是否可立即使用?提示:可以。容量瓶洗净后不需干燥,因为后面还要加蒸馏水定容。
有关物质的量浓度的计算要充分利用物质的量的四个基本公式:
2.已知标准状况下V L气体溶于1 L水后形成溶液,求cB
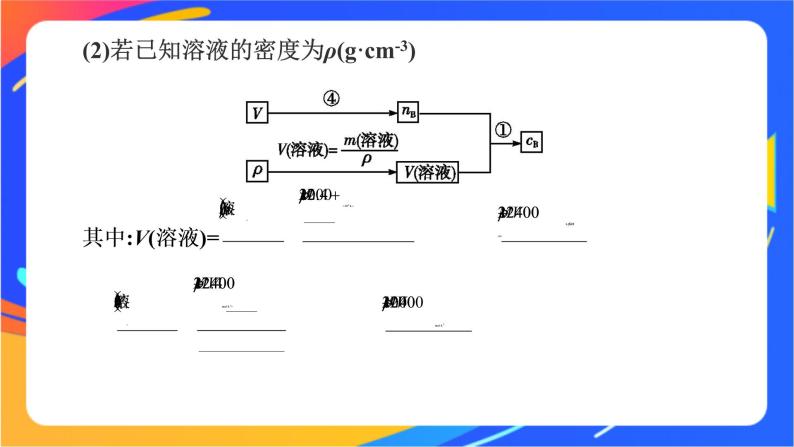
(2)若已知溶液的密度为ρ(g·cm-3)
3.溶液稀释或混合时,求cB(1)溶液稀释时溶质的物质的量不变c1V1=c2V2(c1、c2为稀释前后溶液的物质的量浓度,V1、V2为稀释前后溶液的体积)。(2)不同物质的量浓度溶液混合不同浓度的溶液,溶质相同,其物质的量在混合前后不变,c1V1+c2V2=c(混)·V(混)[c(混)为混合后溶液的物质的量浓度,V(混)为混合后溶液的体积]。
【特别提示】 (1)溶质可以是单质和化合物,也可以是离子或其他特定组合。
(2)带结晶水的物质作“溶质”时,溶质是不含结晶水的化合物,其物质的量的计算,用带结晶水的物质质量除以带结晶水的物质的摩尔质量即可。
1.1 ml·L-1硫酸溶液的含义是( )A.1 L水中含有1 ml硫酸B.1 L溶液中含1 ml H+C.将98 g硫酸溶于1 L水所配成的溶液D.1 L硫酸溶液中含有98 g H2SO4
解析:根据物质的量浓度的定义,A选项说法错误,不是1 L水,应该是1 L溶液;B选项,溶液的体积为1 L时含有 2 ml H+;C选项的错误仍在98 g H2SO4溶于1 L水,溶液的体积不清楚,故溶液的物质的量浓度也不清楚;D选项正确,因硫酸的相对分子质量为98,故98 g为1 ml。
2.用98%的浓H2SO4(ρ=1.84 g·mL-1)配制1 ml·L-1的稀H2SO4 100 mL,配制过程中可能用到下列仪器:①100 mL量筒 ②10 mL量筒 ③50 mL烧杯 ④托盘天平 ⑤100 mL 容量瓶 ⑥胶头滴管 ⑦玻璃棒。按使用时出现的先后顺序排列正确的是( )A.②⑥③⑦⑤B.④③⑤⑦⑥C.①③⑦⑤⑥D.②⑤⑦⑥
解析:浓溶液配稀溶液的过程为:①计算所需浓溶液体积:5.3 mL;②选用合适量筒量取浓溶液:10 mL量筒,并用胶头滴管滴加浓H2SO4到刻度线;③稀释浓H2SO4:将少量水放入50 mL烧杯中,沿玻璃棒缓缓将浓H2SO4注入水中;④将冷却至室温的稀溶液转移至100 mL容量瓶中;⑤定容。
3.利用碳酸钠晶体(Na2CO3·10H2O)来配制0.5 ml·L-1的Na2CO3溶液1000mL,假如其他操作均是准确无误的,下列情况会引起配制溶液的浓度偏高的是( )A.称取碳酸钠晶体100 gB.定容时,俯视观察刻度线C.移液时,对用于溶解碳酸钠晶体的烧杯没有进行冲洗D.定容后,将容量瓶上下颠倒,摇匀,静置时发现液面低于刻度线,于是又加入少量水至刻度线
解析:本题考查一定物质的量浓度溶液的配制过程及误差分析。Na2CO3·10H2O的质量为286 g·ml-1×0.5 ml=143 g,所以A项应偏低;B项平视时,凹液面的最低点与刻度线刚好相平,俯视时液面的最低点低于刻度线,导致浓度偏高;C项对用于稀释或溶解的烧杯,如不数次加水冲洗并将洗涤液也转入容量瓶,会使溶质损失,使所配制的溶液浓度偏低;D项定容后,上下颠倒,摇匀,静置,发现液面低于刻度线,这是由于液体沾在瓶壁和磨口等处所致,不会造成偏差,若加水,则使所配溶液浓度偏低。
4.某学生计划用12 ml·L-1的浓盐酸配制0.10 ml·L-1的稀盐酸450 mL。回答下列问题:(1)量取浓盐酸的体积为 mL,应选用的量筒规格为 。 (2)配制时应选用的容量瓶规格为 。 (3)配制时(除容量瓶外)还需选用的仪器主要有 、 、 、 和试剂瓶。
解析:配制稀盐酸450 mL,由于没有此种规格的容量瓶,所以用500 mL的容量瓶。设量取浓盐酸的体积为V,根据稀释前后HCl物质的量守恒建立关系式:12 ml·L-1×V=0.10 ml·L-1×500 mL,V=4.2 mL;根据量筒的规格选取10 mL量筒;结合配制步骤选取仪器。
答案:(1)4.2 10 mL (2)500 mL (3)量筒 烧杯 玻璃棒 胶头滴管
人教版 (2019)必修 第一册第三节 物质的量课堂教学课件ppt: 这是一份人教版 (2019)必修 第一册第三节 物质的量课堂教学课件ppt,共23页。PPT课件主要包含了物质的量浓度,符号cB,溶液混合的计算公式,课堂练习等内容,欢迎下载使用。
苏教版 (2019)必修 第一册第二单元 溶液组成的定量研究精品ppt课件: 这是一份苏教版 (2019)必修 第一册第二单元 溶液组成的定量研究精品ppt课件,共19页。PPT课件主要包含了学习目标,答案378体积,答案A,答案C,答案B等内容,欢迎下载使用。
化学必修 第一册第二单元 物质的化学计量试讲课ppt课件: 这是一份化学必修 第一册第二单元 物质的化学计量试讲课ppt课件,共29页。PPT课件主要包含了新课导入,曹冲称象原理,思考2,思考1,物质的量,mol,专有名词,知识梳理,阿伏加德罗常数,即使练习等内容,欢迎下载使用。













