
北京课改版九年级上册第8章 碳的世界第一节 碳的单质教学设计
展开碳的单质
(一)指导思想与理论依据
《初中化学新课程标准》(2011版)中要求激发学生学习化学的好奇心,启迪学生的科学思维,培养学生的实践能力,提高学生的科学素养,使学生初步了解化学对人类文明发展的巨大贡献,认识化学在实现人与自然和谐共处、促进人类和社会可持续发展中的地位和作用,认同化学将为实现人类更美好的未来继续发挥它的重大作用。这节课就是要带领学生通过品味历史中的碳文化,学习碳的化学性质,提升解决实际问题、科学探究和证据推理的能力,感受“确定要检验的物质→分析物质性质→寻找合适的试剂以产生不同现象(排除干扰)”的分析思路。
(二)教学背景分析
学习内容分析:
本节课内容设置在金刚石、石墨和C60 之后,教材中碳单质是初中学生学习氧气之后首次全面学习的固态非金属单质,此节内容起承上启下的作用,它是氧气学习的继续,同时为后面学习金属单质和化合物的化学性质打下基础。 教材编排首先对碳的典型单质——金刚石和石墨的结构、物理性质、用途进行学习,而后安排碳单质的化学性质学习,而碳单质的化学性质主要是常温下的稳定性、可燃性和高温下的还原性。碳还原氧化铜是对火法炼铜的模拟,也是一个进行科学探究的良好契机。
学生情况分析:
在本小节内容前,学生已经学习了探究碳的几种单质,对碳单质的结构、性质(物理性质)和用途已经有了一定的认识,学生在日常生活中,对碳的常温下稳定性有所了解,知识了解的不够深入,通过燃烧与灭火一章的学习,已经知道了碳在不同条件下能生成一氧化碳和二氧化碳,并且比较清楚一氧化碳的毒性,但从碳的角度来认识这些知识还不够深入。碳还原氧化铜实验的装置、现象和结论对于学生来说都比较陌生,经过之前的学习,学生已经具备了一定的观察和分析实验现象的能力,也具备了进行实验探究的能力,但是以前接触的物质鉴别都是纯净物的检验和鉴别,干扰信息比较少,这节课要体会混合物中物质的检验思路和方法:确定要检验的物质→分析物质性质→寻找合适的试剂以产生不同现象(排除干扰)的分析思路,为以后的物质鉴别打下基础。
本节课的障碍点在于碳还原氧化铜实验的分析、纯净物检验→混合物检验,为了突破障碍,本节课抓住契机,利用真实的实验情境,解决实际遇到的问题
教学方式与教学手段说明、技术准备:
本节课最重要的实验是炭还原氧化铜的实验,该实验需要事先做好准备,将氧化铜和炭按10:1的比例称量,烘干,并研磨8min,然后取少量于试管中,滴入少量水,让固体在试管壁上形成薄薄的一层。
(三)本课教学目标设计
教学目标:
- 了解碳在常温与高温下,表现出不同的化学性质,了解碳在不同条件下的燃烧产物。
- 掌握碳的化学性质,重点掌握碳还原氧化铜实验的装置、现象和结论。
- 通过观察木炭还原氧化铜的实验,培养观察和分析实验现象的能力,通过探究反应后剩余物质,学会混合物中物质检验的方法。
- 树立物质的组成、结构决定性质,性质决定用途的观点。
- 感受木炭在人类历史发展中的重要作用,体会化学来源于生活,服务于社会。
教学重点:掌握碳的化学性质
教学难点:设计实验检验混合物的成分
(四)教学过程与教学资源设计
教学内容及进程 | 教学活动 | 教学资源及 教学指导策略 | |
1. 通过史料,引出碳的化学性质 | 展示常见的碳单质和不定型碳 通过史料中周口店山洞发现的炭,引出碳的化学性质 | 阅读资料,感受木炭的历史悠久
| 史料引入,将历史事实与化学知识联系起来 |
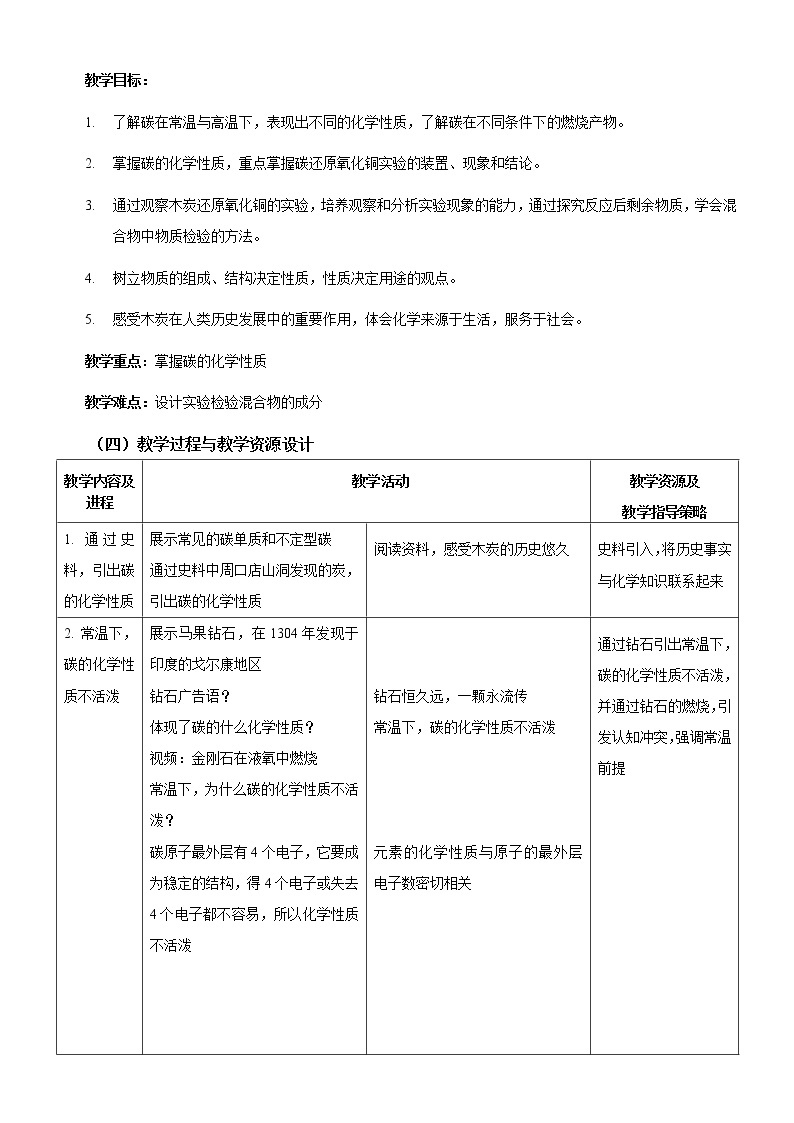
2. 常温下,碳的化学性质不活泼 | 展示马果钻石,在1304年发现于印度的戈尔康地区 钻石广告语? 体现了碳的什么化学性质? 视频:金刚石在液氧中燃烧 常温下,为什么碳的化学性质不活泼? 碳原子最外层有4个电子,它要成为稳定的结构,得4个电子或失去4个电子都不容易,所以化学性质不活泼 生活中还有哪些应用利用了碳的这个化学性质? |
钻石恒久远,一颗永流传 常温下,碳的化学性质不活泼
元素的化学性质与原子的最外层电子数密切相关
古代书画笔迹(墨中含碳)仍然不变;铁路上的枕木烧焦碳化 | 通过钻石引出常温下,碳的化学性质不活泼,并通过钻石的燃烧,引发认知冲突,强调常温前提 |
3.点燃条件下碳与氧气反应(可燃性) | 展示漫画,楚怀王,猜一个成语? 范成大(南宋):不是雪中须送炭,聊装风景要诗来。 体现了碳的什么化学性质? 在燃烧与灭火一章中,你对碳燃烧有了什么新认识? 反应物量的多少不同,生成物也可能不同。 这个化学性质有什么应用? | “雪中送炭”
点燃条件下与氧气发生燃烧反应 C + O2 点燃CO2 ( O2 充 足) 2C + O2 点燃2CO ( O2 不 足) 要注意通风
取暖、做饭、烧烤、炼钢
| 成语诗词引入,学生能感受到炭在古代文化中的重要作用,也体现了碳燃烧的重要应用 |
4.高温下,碳与金属氧化物反应(还原性) | 商周开始,对木炭量与质两方面的需求增加,需通过专门的炭窑烧取木炭 人类历史上,有石器时代、铜器时代、铁器时代……这主要是根据当时使用的工具的材料来划分的。铜器时代大约从距今5000年前开始的,直到约2000年前炼钢炼铁才逐渐兴起。人类使用铜器之所以早于铁器,除了自然界有天然的铜块外(当然是比较稀少的),最主要的是人们最早发现孔雀石 (主要成分是碱式碳酸铜Cu2(OH)2CO3)在木炭火中加热就可以生成铜,由此学会了利用化学反应从矿石中得到金属。其中发生了什么反应? 今天我们就循着古人的足迹,做做这个实验,需要哪些装置 演示实验:木炭还原氧化铜 哪些现象说明木炭与氧化铜反应生成铜? 展示石灰水和试管 | 冶炼青铜器需要木炭
感受木炭在青铜器冶炼中的重要作用,思考孔雀石与木炭怎么变成铜 写反应2CuO+C高温2Cu+CO2↑ 加热装置、试管、石灰水(检验二氧化碳) 观察实验 固体由黑变红,石灰水变浑浊(分析受到木炭与氧气反应的干扰) 仔细观察试管上的变化 | 从商周时期的炼铜开始,引入木炭还原氧化铜,体现了该反应的重要应用
这个实验很不好做,进行了改进,效果还是比较好的 |
5.探究反应后固体中的物质 | 反应后试管中除了铜还可能有什么?
如何证明你的猜想? 展示铜、碳、氧化铜的物理性质和化学性质 提示:取…放于…,加入…量…,若…则…,若…则… 演示实验:取少量反应后剩余物质,加入稀硫酸,加热 | 小组讨论, 展示:①碳 ②氧化铜 ②碳和氧化铜 利用物质的不同性质,排除铜干扰 读该化学性质 讨论实验方案,检验反应后的物质 展示实验方案 观察实验,判断所剩物质 液体变蓝,有黑色固体剩余:有碳和氧化铜 | 带领学生感受确定要检验的物质→分析物质性质→寻找合适的试剂以产生不同现象(排除干扰)的分析思路,为以后的物质检验打下基础 |
6.小结及随堂检测 | 你今天有哪些收获? 小结:确定要检验的物质→分析物质性质→寻找合适的试剂以产生不同现象(排除干扰) 讲解 | 说自己的收获 学到了哪些知识? 掌握了什么方法? 你还感悟到了什么? 完成随堂检测 | 沉淀思想,总结提升,归纳思路 |
板书设计 | |||
碳的单质 1、常温下,化学性质稳定性 2、碳与氧气的反应(可燃性) C+O2CO2(氧气充足) 2C+O22CO(氧气不足) 3、碳与某些氧化物的反应(还原性) C+2CuOCO2↑+2Cu (黑色粉末) (红色粉末)
澄清的石灰水变浑浊
固体由黑变红
确定要检验的物质→分析物质性质→寻找合适的试剂以产生不同现象(排除干扰)
| |||
(五)学习效果评价设计
学习效果评价 | |||||
姓名 | 时间 | ||||
评价项目 | 具体评价内容 | 评价结果 | |||
标准 | 满分 | 得分 | |||
学会碳的化学性质 | 完成随堂检测1-2题 | 一个空1分 | 3 |
| |
混合物中的物质检验 | 完成随堂检测3题 | 一个空1分 | 7 |
| |
课堂表现 | 你举过几次手? 你有几次被老师叫起来回答问题或进行展示? 在小组讨论中你发表过几次意见? |
1次1分 |
|
| |
|
| ||||
|
| ||||
随堂检测:
1. 齐白石最大尺幅黑白作品《松柏高立图·篆书四言联》以4、255亿人民币拍出,其画用墨汁的主要成分为炭黑,它能使画很长时间不褪色,这是因为墨汁中的炭黑具有_____________ 。
2.在高温下,碳能跟氧化铜反应,写出该化学方程式_____________________________ 。利用碳的还原性,可将其用于 。
3.几位同学在实验室做木炭还原氧化铜的实验,实验完毕后,他们发现试管内仍有黑色固体物质存在。该试管中的黑色固体物质是什么?
【提出猜想】小玉同学:木炭。小兰同学:氧化铜。小华同学:___________________。
【查阅资料】木炭、铜都不与稀硫酸反应; CuO能与稀硫酸反应生成蓝色溶液。
【实验设计】方案一:向盛有黑色固体的试管中加入______________,充分振荡,静置后观察现象。方案二:取少量该黑色固体在空气中灼烧,观察现象。
他们对“方案一”进行了分析讨论,达成了共识:若试管内溶液无色、还有黑色固体存在,证明_____同学的猜想正确。若试管中溶液呈蓝色、无黑色固体,证明_______同学的猜想正确。若出现的现象是_______________,证明小华同学的猜想是正确的。
他们按照“方案二”进行了实验操作,记录如下:
(六)教学反思
- 将古代文化与化学知识的学习有机结合起来,基本上按史料分析——分析体现的碳的化学性质——该性质的应用展开,学生通过这节课,真的感受到了碳在古代生产发展和生活中的重要应用,并能将这些性质与自己的日常生活练习起来,体现化学“从生活走向化学,从化学走向社会”的主旨。
- 木炭还原氧化铜的实验很难做成功,这节课我通过课前的多次实验,找到了能较好完成实验的方法,成功完成了演示实验。
- 带领学生感受确定要检验的物质→分析物质性质→寻找合适的试剂以产生不同现象(排除干扰)的分析思路,为以后的物质检验打下基础。经过前六个单元的学习,学生已经具备了一定的观察和分析实验现象的能力,也具备了进行实验探究的能力,但是以前接触的物质检验都是纯净物的检验,干扰信息比较少,这次存在铜的干扰,给学生提供了一个很好的探究的机会,通过真实的探究,体会物质检验的思路。
- 由于时间关系,物质检验鉴别的思路上课的时候梳理的是碳还原氧化铜后所得物质检验的方法,为了凸显思路,应对一般方法进行板书效果更好。
九年级上册第一节 空气教案: 这是一份九年级上册第一节 空气教案,共5页。
初中化学北京课改版九年级上册第一节 原子教学设计: 这是一份初中化学北京课改版九年级上册第一节 原子教学设计,共5页。教案主要包含了导入新课,新课教学,课堂小结等内容,欢迎下载使用。
初中化学北京课改版九年级上册第一节 水的净化教案设计: 这是一份初中化学北京课改版九年级上册第一节 水的净化教案设计,共3页。教案主要包含了水的净化,探究实验等内容,欢迎下载使用。













