





2022年中考化学基础梳理篇模块1身边的化学物质第8课时金属的化学性质讲本课件
展开· 考点1 金属的化学性质
· 考点2 金属活动性顺序
· 考点3 金属与酸反应的曲线分析
· 考点4 金属与盐溶液反应后滤液、滤渣成分的分析
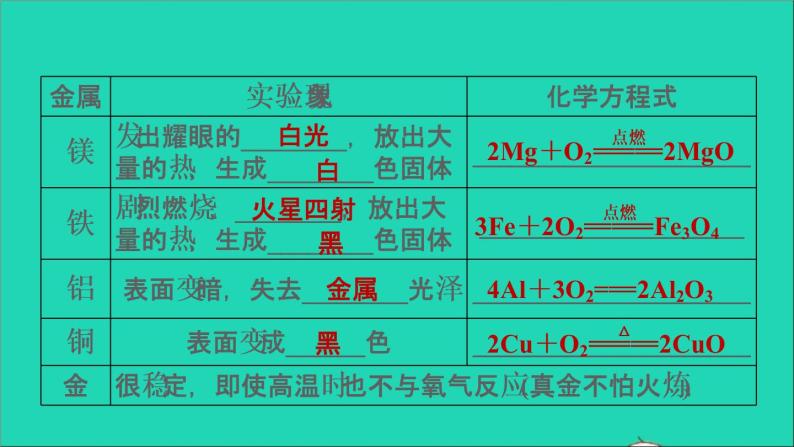
金属+氧气―→金属氧化物
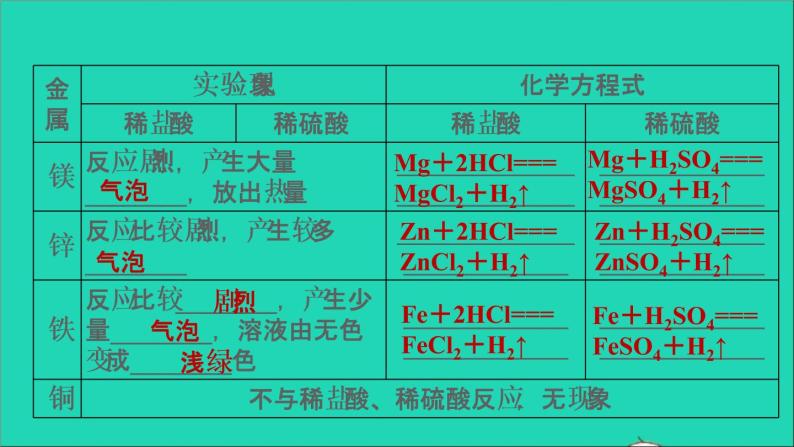
铝常温下就会与空气中的氧气反应,生成致密的氧化铝膜,使铝与氧气隔绝,起“自我保护”作用。活泼金属+酸―→盐+H2↑
Mg+2HCl===MgCl2+H2↑
Mg+H2SO4===MgSO4+H2↑
Zn+2HCl===ZnCl2+H2↑
Zn+H2SO4===ZnSO4+H2↑
Fe+2HCl===FeCl2+H2↑
Fe+H2SO4===FeSO4+H2↑
①活泼金属是指在金属活动性顺序中排在氢前面的金属。②这里的酸通常指稀盐酸或稀硫酸,不包括浓硫酸和硝酸。③利用金属与酸的反应判断金属活动性顺序时,通常要控制的量是酸的种类、浓度和体积,金属的形状、大小。④相同条件下,金属与酸反应越剧烈,金属的活动性越强。
铁与稀盐酸、稀硫酸或硫酸铜溶液反应时,生成物中铁元素呈+2价,生成氯化亚铁(FeCl2)、硫酸亚铁(FeSO4)。金属+盐(溶液)―→新金属+新盐(溶液)
Fe+CuSO4===FeSO4+Cu
Cu+2AgNO3===Cu(NO3)2+2Ag
①前可置后,盐要溶:在金属活动性顺序中,排在前面的金属能够把排在后面的金属从其盐溶液中置换出来。②钾、钙、钠三种金属过于活泼,不适合此反应。
(3)自然界中的存在形式——以单质形式存在的金属比以化合态形式存在的金属活动性________
例 【2021•厦门一中模拟•3分】有甲、乙、丙、丁四种颗粒大小相同的金属,分别投入等质量等浓度的稀盐酸中,只有乙、丙表面有气泡产生,且丙产生气泡较快。再将甲投入丁的化合物溶液中,甲的表面有丁析出。则这四种金属活动性顺序为( )A.甲>乙>丙>丁 B.丙>乙>甲>丁C.丙>乙>丁>甲 D.丁>甲>乙>丙
(1)实验原理①根据金属能否与酸反应,能与酸反应的比不与酸反应的活动性更强;②都能与酸反应的,在相同条件下,反应更剧烈的金属活动性更强;
3.探究金属活动性顺序的实验设计
③金属能否与另一种金属的盐溶液反应,能反应,金属的活动性比另一种金属的活动性更强;不能反应,则更弱。(2)探究方法方法一:金属与酸反应。在金属活动性顺序里,位于氢前面的金属能置换出盐酸、稀硫酸中的氢。方法二:金属与可溶性盐溶液反应。能发生反应,则表示该金属的活动性强于盐溶液中的金属。
(3)实验设计①比较两种金属活动性强弱
例 比较 Zn、Cu金属活动性顺序
锌表面有红色固体析出,溶液由蓝色变为无色
②验证三种金属的活动性顺序判断依据:能否发生置换反应实验方案:方案一:两金夹一盐( 盐中金属的活动性在“两金”之间)。方案二:两盐夹一金(“一金”的金属活动性在两盐中金属之间)。例 验证 Zn 、Cu、Ag的金属活动性顺序
a.在实验前,先将金属进行打磨。以除去金属表面的氧化物或污物。b. 进行金属与酸的反应时,一般用稀盐酸或稀硫酸,不用硝酸或浓硫酸。
(1)金属的活动性越强,曲线倾斜程度越______。产生氢气的质量________,反应的酸的质量相同,反应的金属质量不同。(2)酸不足、金属过量时,生成的氢气的质量由______的质量决定。
1.两种等质量的金属(足量)分别与等质量的同一种酸(不足量)反应,曲线如图所示:
(1)横坐标为反应时间,曲线如图所示:①曲线倾斜程度越大,对应的金属的活动性越______。图中乙的活动性______甲。反应的酸的质量不同,甲反应的酸的质量________乙。②酸足量时,生成氢气的质量由金属的种类及质量决定。即:
2.两种等质量的金属分别与同一种酸(足量)反应:
(2)横坐标为酸的质量,曲线如图所示:①开始反应时,酸的量不足,产生氢气的质量由__________的质量决定。
横坐标表示酸的质量,纵坐标表示产生氢气的质量时,无法判断金属活动性的强弱。
例 等质量的两种金属甲、乙分别加入足量的稀硫酸中,反应后金属都没有剩余。产生H2的质量与时间的关系如图所示。下列说法中正确的是( ) A.甲的活动性比乙强 B.反应消耗等质量的金属 C.反应产生等质量的氢气 D.甲的相对原子质量一定比乙小
1.金属与盐溶液的反应要遵行“活动性最强的金属与活动性最弱的金属的盐溶液先反应”的原则,即“先远后近”(金属活动性顺序表中的位置)原则;还要结合反应的程度进行分析。
例 将铁片放入Cu(NO3)2和AgNO3的混合溶液中,判断反应后滤液、滤渣的成分。
Fe(NO3)2、Cu(NO3)2、AgNO3
Fe(NO3)2、Cu(NO3)2
滤液中一定存在活动性最强的金属离子,滤渣中一定存在活动性最弱的金属单质。其余物质根据反应程度判断是否存在。
Mg+2HCl===MgCl2+H2↑(合理即可)
Fe+CuSO4===FeSO4+Cu(合理即可)
· 考点1 金属的化学性质(1)
· 考点2 金属活动性顺序(2)
· 考点3 金属与酸反应的曲线分析(3)
· 考点4 金属与盐溶液反应后滤液、滤渣成分的分析(4)
1.【2021•福建•3分】据文献报道:一种特殊的铜纳米颗粒具有与金、银极其相似的反应惰性,可替代黄金做精密电子元器件。下列对该铜纳米颗粒的判断,正确的是( )A.能与盐酸反应产生氢气B.在空气中容易锈蚀C.能与硫酸亚铁发生置换反应D.具有良好的导电性
2.【2021•莆田质检•3分】验证镁、铁、铜三种金属的活动性顺序,可选用的一组物质是( )A.铁、铜、氯化镁溶液B.镁、氯化亚铁溶液﹑氯化铜溶液C.铜、氯化镁溶液﹑氯化亚铁溶液D.镁、铜、氯化亚铁溶液
3.【2020•厦门双十中学模拟•3分】一定质量的锌、铁分别和等量的盐酸反应,产生氢气质量与时间的关系如图所示,下列说法不正确的是( )
A.t1时,产生氢气的质量锌比铁大B.t1时,产生氢气的速率锌比铁大C.t2时,参加反应的锌的质量与铁相同D.t2时,锌、铁消耗的盐酸质量相同
4.【易错题】【2021·厦门一中模拟·3分】将一定量的铁粉加入含有Zn(NO3)2、Cu(NO3)2和AgNO3的废液中,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生。下列判断正确的是( )
2022年中考化学基础梳理篇模块1身边的化学物质第11课时盐化肥讲本课: 这是一份2022年中考化学基础梳理篇模块1身边的化学物质第11课时盐化肥讲本课,共44页。PPT课件主要包含了·考点5化肥,金属离子,盐的概念,易错提醒,小苏打,石灰石,大理石,NaCl,Na2CO3,NaHCO3等内容,欢迎下载使用。
2022年中考化学基础梳理篇模块1身边的化学物质第10课时酸和碱(二)讲本课: 这是一份2022年中考化学基础梳理篇模块1身边的化学物质第10课时酸和碱(二)讲本课,共35页。PPT课件主要包含了NaOH,CaOH2,熟石灰,氢氧化钙的制取,化学性质,Na2CO3+H2O,CaCO3↓+H2O,CaCl2+2H2O,OH-,阳离子等内容,欢迎下载使用。
2022年中考化学基础梳理篇模块1身边的化学物质第9课时酸和碱(一)讲本课件: 这是一份2022年中考化学基础梳理篇模块1身边的化学物质第9课时酸和碱(一)讲本课件,共35页。PPT课件主要包含了不变色,酸碱指示剂,~14,pH试纸,标准比色卡,pH的测定方法,酸碱度的应用,HCl,H2SO4,刺激性等内容,欢迎下载使用。












