






2022年中考化学基础梳理篇模块1身边的化学物质第6课时溶液(二)讲本课
展开· 考点1 饱和溶液与不饱和溶液、溶解度
· 考点2 溶解度曲线
(1)概念在一定温度下,向一定量溶剂里加入某种溶质,当溶质不能继续溶解时,所得的溶液叫做这种溶质的__________; 还能继续溶解的溶液, 叫做这种溶质的______________。
1.饱和溶液与不饱和溶液
某种物质的饱和溶液中,不能继续溶解该物质,但还能够溶解其他物质,如在饱和硝酸钾溶液中可以溶解氯化钠。
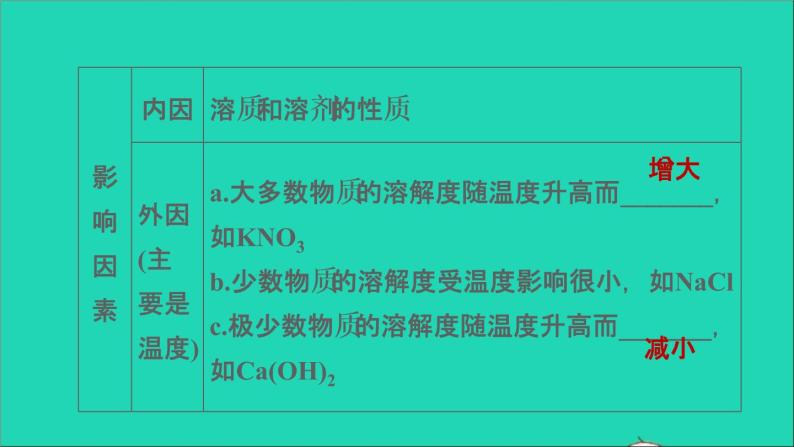
(2)饱和溶液与不饱和溶液转化对于大多数溶解度随温度升高而 的物质(如KNO3):不饱和溶液 饱和溶液对于少数溶解度随温度升高而 的物质[如Ca(OH)2]:不饱和溶液 饱和溶液
(3)溶解度与溶解性常温下(20 ℃)溶解度和溶解性的关系
CaCO3(合理即可)
降温结晶:通过冷却热饱和溶液的方法使溶质析出。适用于溶解度受温度影响较大的物质,如_________。蒸发结晶:通过蒸发溶剂的方法使溶质析出。适用于溶解度受温度影响较小的物质,如___________。
用纵坐标表示溶解度,横坐标表示温度,根据某物质不同温度时的溶解度数据绘制出来的曲线叫做溶解度曲线。以图为例,回答问题:
(1)溶解度曲线中点、线、面的含义
(2)溶解度曲线的应用①某温度下物质溶解度的大小a.t2 ℃时,甲、乙、丙三种物质的溶解度由大到小的顺序为___________________;b.t1 ℃时,甲、丙的溶解度相等,均为________。②饱和溶液与不饱和溶液的判断a.t3 ℃时,将40 g甲物质加入到50 g水中,充分溶解,形成的是该物质的_______(填“饱和”或“不饱和”,下同)溶液;
b.t2 ℃时,将15 g乙物质加入到50 g水中,充分溶解,形成的是该物质的__________溶液。③饱和溶液与不饱和溶液转化a.将接近饱和的甲溶液转化成饱和溶液,可采取的方法是____________________________________;b.t3 ℃时,将40 g甲的不饱和溶液转化成该温度下的饱和溶液,可采取的方法是____________________________。
增加甲物质(或蒸发溶剂或降低温度)
增加甲物质(或恒温蒸发溶剂)
④判断物质结晶或提纯的方法a.当甲中混有少量的乙时,提纯甲所用的方法是________________________________。b.当丙中混有少量的甲时,提纯丙所用的方法是__________________。
降温结晶(或冷却热饱和溶液)
⑤溶液中溶质质量、溶剂质量的计算:a.t1 ℃时,81 g甲的饱和溶液中溶质的质量为_________g;b.t2 ℃时,将45 g乙加入到100 g水中,充分溶解,溶液中溶质与溶剂的质量比为 。
⑥溶液中溶质质量分数的计算a.t1 ℃时,将40 g丙物质加入到100 g水中,充分溶解,所得溶液的溶质质量分数约为 ;b.t2 ℃时,乙的饱和溶液的溶质质量分数约为 。
⑦一定温度下配制饱和溶液时,所需溶剂质量与溶质质量的大小比较a.t2 ℃时,将等质量的甲、乙、丙三种物质配制成该温度下各自的饱和溶液,所需溶剂质量的大小关系为 。b.t2 ℃时,欲将乙、丙两种物质配制成等质量的饱和溶液,所需溶质质量的大小关系为 。
⑧温度改变时,饱和溶液中各种量的变化情况t2 ℃ 时甲、乙、丙的饱和溶液各a g,降温到t1 ℃:a.析出晶体的有 ;b.无晶体析出的有 ;c.所得溶液中溶质的质量分数由小到大依次为 ;d.溶液质量由小到大依次为 。
增加溶质、蒸发溶剂、改变温度
· 考点1 饱和溶液与不饱和溶液、溶解度(1 2)
· 考点2 溶解度曲线(3 4 )
1.【2020·福建·3分】NaCl和KNO3在不同温度时的溶解度如下表。下列说法错误的是( )
A.20 ℃时,100 g水中最多能溶解36.0 g NaClB.40 ℃时,KNO3饱和溶液的溶质质量分数小于63.9%C.可用冷却海水的方法获取大量食盐D.其他条件不变,升温可将KNO3饱和溶液变为不饱和溶液
2.【2021·福建节选·5分】如图为我国古代“布灰种盐”生产海盐的部分场景,其过程为“烧草为灰,布在滩场,然后以海水渍之,俟晒结浮白,扫而复淋”。
(1)“晒结浮白”是指海水浸渍的草灰经日晒后出现白色海盐颗粒的过程,化学上称之为 。
(2)将“上等卤水”在100 ℃恒温蒸发至刚有晶体析出,所得溶液的组成为150 g溶液中含H2O 100 g、NaCl 39.8 g、MgCl27.65 g及其他成分2.55 g。将150 g此溶液降温至20 ℃,有______g NaCl析出(溶解度见下表)。此时, ______(填“有”或“没有”)MgCl2析出,原因是_______________________________________________________。
20 ℃时溶液中的氯化镁未达到饱和状态
3.【2019·福建·3分】KNO3 的溶解度曲线如下图所示。下列说法错误的是( )
A.0~ 60 ℃,KNO3 的溶解度随温度升高而增大B.60 ℃时的 KNO3 饱和溶液降温至 20 ℃,有晶体析出C.20 ℃,100 g 水中最多能溶解 31.6 g KNO3D.60 ℃时,可配制溶质质量分数为 60%的 KNO3 溶液
4.【2017·福建·3分】如图是甲、乙两种固体物质的溶解度曲线。下列说法错误的是( )
2022年中考化学基础梳理篇模块1身边的化学物质第11课时盐化肥讲本课: 这是一份2022年中考化学基础梳理篇模块1身边的化学物质第11课时盐化肥讲本课,共44页。PPT课件主要包含了·考点5化肥,金属离子,盐的概念,易错提醒,小苏打,石灰石,大理石,NaCl,Na2CO3,NaHCO3等内容,欢迎下载使用。
2022年中考化学基础梳理篇模块1身边的化学物质第10课时酸和碱(二)讲本课: 这是一份2022年中考化学基础梳理篇模块1身边的化学物质第10课时酸和碱(二)讲本课,共35页。PPT课件主要包含了NaOH,CaOH2,熟石灰,氢氧化钙的制取,化学性质,Na2CO3+H2O,CaCO3↓+H2O,CaCl2+2H2O,OH-,阳离子等内容,欢迎下载使用。
2022年中考化学基础梳理篇模块1身边的化学物质第9课时酸和碱(一)讲本课件: 这是一份2022年中考化学基础梳理篇模块1身边的化学物质第9课时酸和碱(一)讲本课件,共35页。PPT课件主要包含了不变色,酸碱指示剂,~14,pH试纸,标准比色卡,pH的测定方法,酸碱度的应用,HCl,H2SO4,刺激性等内容,欢迎下载使用。












