
- 7.4结晶现象教案 教案 2 次下载
- 粤科版化学九下 第七章复习课件 课件 1 次下载
- 8.1溶液的酸碱性课件教案 教案 1 次下载
- 8.1常见的酸碱性教案 教案 4 次下载
- 8.2常见的酸和碱(1)课件 课件 1 次下载
初中化学科粤版九年级下册第七章 溶液综合与测试公开课教学设计及反思
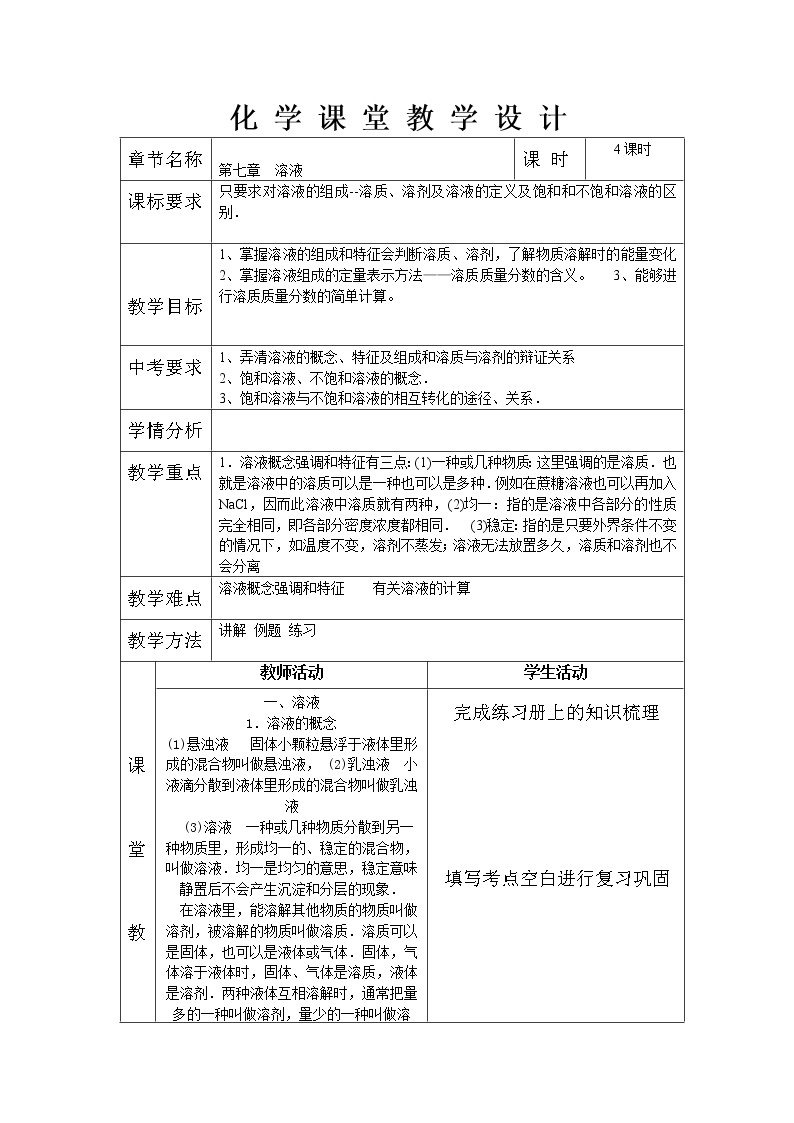
展开化 学 课 堂 教 学 设 计
章节名称 |
第七章 溶液 | 课 时 | 4课时 | ||
课标要求 | 只要求对溶液的组成--溶质、溶剂及溶液的定义及饱和和不饱和溶液的区别.
| ||||
教学目标 | 1、掌握溶液的组成和特征会判断溶质、溶剂,了解物质溶解时的能量变化 2、掌握溶液组成的定量表示方法——溶质质量分数的含义。 3、能够进行溶质质量分数的简单计算。 | ||||
中考要求 | 1、弄清溶液的概念、特征及组成和溶质与溶剂的辩证关系 2、饱和溶液、不饱和溶液的概念. 3、饱和溶液与不饱和溶液的相互转化的途径、关系. | ||||
学情分析 |
| ||||
教学重点 | 1.溶液概念强调和特征有三点:(1)一种或几种物质:这里强调的是溶质.也就是溶液中的溶质可以是一种也可以是多种.例如在蔗糖溶液也可以再加入NaCl,因而此溶液中溶质就有两种,(2)均一:指的是溶液中各部分的性质完全相同,即各部分密度浓度都相同. (3)稳定:指的是只要外界条件不变的情况下,如温度不变,溶剂不蒸发;溶液无法放置多久,溶质和溶剂也不会分离 | ||||
教学难点 | 溶液概念强调和特征 有关溶液的计算 | ||||
教学方法 | 讲解 例题 练习 | ||||
课
堂
教
学
过
程
设
计
思
路 | 教师活动 | 学生活动 | |||
一、溶液 1.溶液的概念 (1)悬浊液 固体小颗粒悬浮于液体里形成的混合物叫做悬浊液, (2)乳浊液 小液滴分散到液体里形成的混合物叫做乳浊液 (3)溶液 一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物,叫做溶液.均一是均匀的意思,稳定意味静置后不会产生沉淀和分层的现象. 在溶液里,能溶解其他物质的物质叫做溶剂,被溶解的物质叫做溶质.溶质可以是固体,也可以是液体或气体.固体,气体溶于液体时,固体、气体是溶质,液体是溶剂.两种液体互相溶解时,通常把量多的一种叫做溶剂,量少的一种叫做溶质.当溶液中有水存在时,不论水的量有多少,习惯 上都把水看作溶剂,通常不指明溶剂的溶液,一般是水溶液. 2.溶液的基本特征 溶液的基本特征是溶液的均一性和稳定性,在溶液中,溶质的分子(或离子)高度分散到水分子中间,形成 透明的混合物.均一性,是指溶液各处密度和浓度都一样,性质 都相同 (二)饱和溶液 不饱和溶液 1.概念 (1)饱和溶液和不饱和溶液 在一定温度下,在一定量溶剂里,不能再溶解某种溶质的溶液,叫做这种溶质的饱和溶液,还能继续溶解某种溶质的溶液,叫做这种溶质的不饱和溶液. 理解这两个概念必须注意如下两点: ①首先要指明一定温度,一定的溶剂量.因为溶液饱和或不饱和与温度有关也与溶 剂质量有关.②强调这种溶质的饱和溶液或不饱和溶液. (2)浓溶液和稀溶液 为了粗略地表示溶液里溶质含量的多少,常把溶液分为浓溶液和稀溶液.含溶质多的溶液是较浓溶液.含溶质少的溶液是较稀溶液. 2、饱和溶液和不饱和溶液的相互转化关系 3、浓溶液、稀溶液与饱和溶液、不饱和溶液的关系 二、溶解度 1、固体的溶解度 (1)溶解度定义:在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量 四要素:①条件:一定温度②标准:100g溶剂③状态:达到饱和④质量:单位:克 (2)溶解度的含义:3)影响固体溶解度的因素:①溶质、溶剂的性质(种类) ②温度 2、气体的溶解度 (1)气体溶解度的定义:在压强为101kPa和一定温度时,气体溶解在1体积水里达到饱和状态时的气体体积。 (2)影响因素: ①气体的性质 ②温度(温度越高,气体溶解度越小) ③压强(压强越大,气体溶解度越大)三、溶质质量分数 1)、溶质的质量分数 溶液中溶质的质量分数是溶质质量与溶液质量之比。溶液中溶质的质量分数可以用下式计算: 溶质的质量分数=(溶质质量/溶液质量)*100% = [溶质质量/(溶质质量+溶剂质量]*100% 关于溶液稀释或增浓的计算 2)关于溶液稀释的计算 因为溶液稀释前后,溶质的质量不变,所以若设浓溶液质量为A g,溶质的质量分数为a%,加水稀释成溶质的质量分数为b%的稀溶液B g,则A g×a%=Bg×b%(其中B=A+m水) ②关于溶液增浓(无溶质析出)的计算 溶液增浓通常有几种情况: a、向原溶液中添加溶质: 因为溶液增加溶质前后,溶剂的质量不变。增加溶质后,溶液中溶质的质量=原溶液中溶质的质量+增加的溶质的质量,而溶液的质量=原溶液的质量+增加的溶质的质量。所以,若设原溶液质量为A g,溶质的质量分数为a%,加溶质Bg后变成溶质的质量分数为b%的溶液,则Ag×a%+Bg=(A g+Bg)×b%。 b、将原溶液蒸发去部分溶剂 因为溶液蒸发溶剂前后,溶质的质量不变。所以,若设原溶液质量为A g,溶质的质量分数为a%,蒸发Bg水后变成溶质的质量分数为b%的溶液,则:Ag×a%=(Ag-Bg)×b%。 c、与浓溶液混合 因为混合后的溶液的总质量等于两混合组分溶液的质量之和,混合后的溶液中溶质质量等于两混合组分的溶质质量之和。所以,设原溶液质量为 A g,溶质的质量分数为a%,浓溶液质量为B g,溶质的质量分数为b%,两溶液混合后得到溶质的质量分数为c%的溶液,则:Ag×a%+B g× b%=(Ag+Bg)×c%。 | 完成练习册上的知识梳理
填写考点空白进行复习巩固
回忆 填写考点
完成练习
填写考点空白 完成练习进行巩固复习 | ||||
板 书 设 计
| 第15、16课时 溶液 有关溶液的计算 一、溶液 1.溶液的概念 (1)悬浊液 (2)乳浊液 (3)溶液 二、溶解度 1、固体的溶解度 2、气体的溶解度 三、溶质质量分数 1)、溶质的质量分数 2)关于溶液稀释的计算
| ||||
作业 | 课时15、16 练习册 | ||||
教 学 反 思
|
| ||||
化学科粤版4.2 水的组成优秀教案: 这是一份化学科粤版4.2 水的组成优秀教案,共9页。教案主要包含了知识与技能,过程与方法等内容,欢迎下载使用。
初中化学科粤版九年级上册4.2 水的组成教案: 这是一份初中化学科粤版九年级上册4.2 水的组成教案,共4页。教案主要包含了教学目标,教学重点,教学难点,教学手段,教材分析,学生分析,教学过程,教学评价等内容,欢迎下载使用。
科粤版九年级上册第一章 大家都来学化学1.1 身边的化学教学设计: 这是一份科粤版九年级上册第一章 大家都来学化学1.1 身边的化学教学设计,共2页。教案主要包含了学习目标要求,教学设计思路等内容,欢迎下载使用。













