

2021年广东省普通高中学业水平选择性考试 化 学练习题
展开www.ks5u.com2021年广东省普通高中学业水平选择性考试
化 学
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1. 今年五一假期,人文考古游持续成为热点。很多珍贵文物都记载着中华文明的灿烂成就,具有深邃的文化寓意和极高的学术价值。下列国宝级文物主要由合金材料制成的是( )
选项 | A | B | C | D |
文物 | ||||
名称 | 铸客大铜鼎 | 河姆渡出土陶灶 | 兽首玛瑙杯 | 角形玉杯 |
2. 广东有众多国家级非物质文化遗产,如广东剪纸、粤绣、潮汕工夫茶艺和香云纱染整技艺等。下列说法不正确的是( )
A. 广东剪纸的裁剪过程不涉及化学变化
B. 冲泡工夫茶时茶香四溢,体现了分子是运动的
C. 制作粤绣所用的植物纤维布含有天然高分子化合物
D. 染整技艺中去除丝胶所用的纯碱水溶液属于纯净物
3. “天问一号”着陆火星,“嫦娥五号”采回月壤。腾飞中国离不开化学,长征系列运载火箭使用的燃料有液氢和煤油等化学品。下列有关说法正确的是( )
A. 煤油是可再生能源
B. 燃烧过程中热能转化为化学能
C. 火星陨石中的质量数为20
D. 月壤中的与地球上的互为同位素
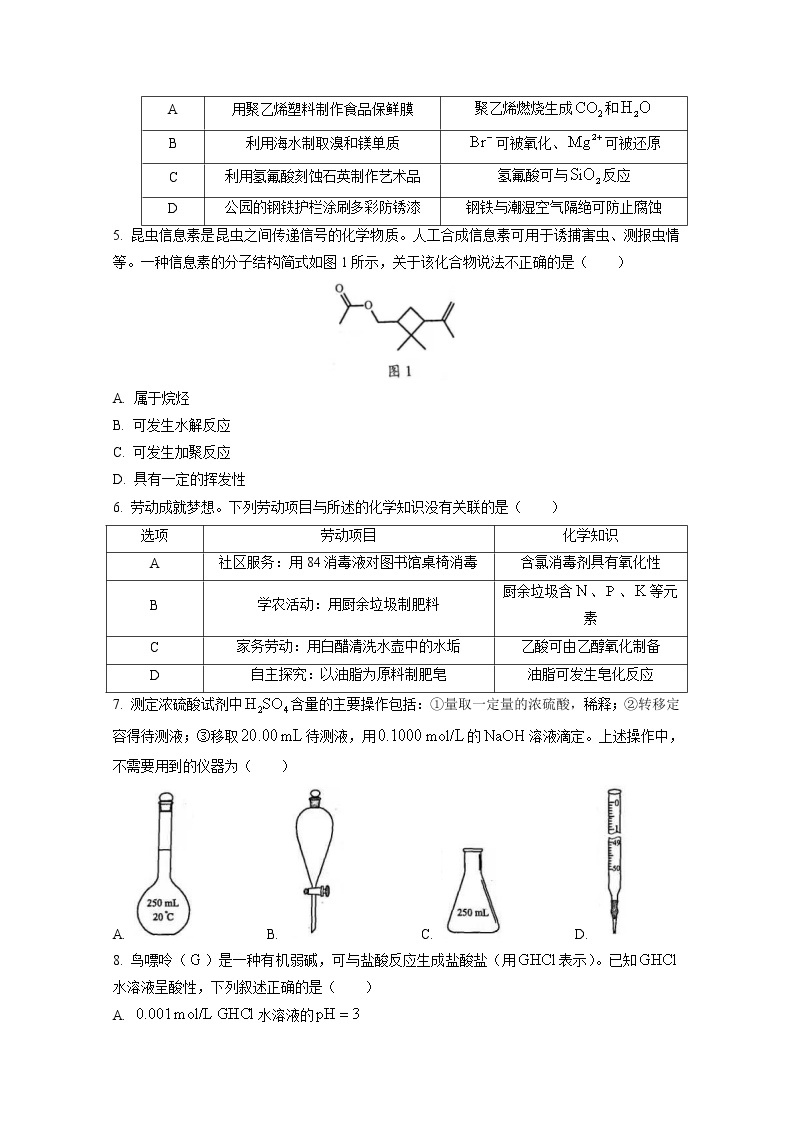
4. 化学创造美好生活。下列生产活动中,没有运用相应化学原理的是( )
选项 | 生产活动 | 化学原理 |
A | 用聚乙烯塑料制作食品保鲜膜 | 聚乙烯燃烧生成和 |
B | 利用海水制取溴和镁单质 | 可被氧化、可被还原 |
C | 利用氢氟酸刻蚀石英制作艺术品 | 氢氟酸可与反应 |
D | 公园的钢铁护栏涂刷多彩防锈漆 | 钢铁与潮湿空气隔绝可防止腐蚀 |
5. 昆虫信息素是昆虫之间传递信号的化学物质。人工合成信息素可用于诱捕害虫、测报虫情等。一种信息素的分子结构简式如图1所示,关于该化合物说法不正确的是( )
A. 属于烷烃
B. 可发生水解反应
C. 可发生加聚反应
D. 具有一定的挥发性
6. 劳动成就梦想。下列劳动项目与所述的化学知识没有关联的是( )
选项 | 劳动项目 | 化学知识 |
A | 社区服务:用84消毒液对图书馆桌椅消毒 | 含氯消毒剂具有氧化性 |
B | 学农活动:用厨余垃圾制肥料 | 厨余垃圾含、、等元素 |
C | 家务劳动:用白醋清洗水壶中的水垢 | 乙酸可由乙醇氧化制备 |
D | 自主探究:以油脂为原料制肥皂 | 油脂可发生皂化反应 |
7. 测定浓硫酸试剂中含量的主要操作包括:①量取一定量的浓硫酸,稀释;②转移定容得待测液;③移取待测液,用的溶液滴定。上述操作中,不需要用到的仪器为( )
A. B. C. D.
8. 鸟嘌呤()是一种有机弱碱,可与盐酸反应生成盐酸盐(用表示)。已知水溶液呈酸性,下列叙述正确的是( )
A. 水溶液的
B. 水溶液加水稀释,升高
C. 在水中的电离方程式为:
D. 水溶液中:
9. 火星大气中含有大量,一种有参加反应的新型全固态电池有望为火星探测器供电。该电池以金属钠为负极,碳纳米管为正极,放电时( )
A. 负极上发生还原反应 B. 在正极上得电子
C. 阳离子由正极移向负极 D. 将电能转化为化学能
10. 部分含铁物质的分类与相应化合价关系如图2所示。下列推断不合理的是( )
A. 可与反应生成
B. 既可被氧化,也可被还原
C. 可将加入浓碱液中制得的胶体
D. 可存在的循环转化关系
11. 设为阿伏加德罗常数的值。下列说法正确的是( )
A. 含有键的数目为
B. 的盐酸含有阴离子总数为
C. 与混合后的分子数目为
D. 与足量反应生成的分子数目为
12. 化学是以实验为基础的科学。下列实验操作或做法正确且能达到目的的是( )
选项 | 操作或做法 | 目的 |
A | 将铜丝插入浓硝酸中 | 制备 |
B | 将密闭烧瓶中的降温 | 探究温度对平衡移动的影响 |
C | 将溴水滴入溶液中,加入乙醇并振荡 | 萃取溶液中生成的碘 |
D | 实验结束,将剩余固体放回原试剂瓶 | 节约试剂 |
13. 一种麻醉剂的分子结构式如图3所示。其中,的原子核只有1个质子;元素、、原子序数依次增大,且均位于的下一周期;元素的原子比原子多8个电子。下列说法不正确的是( )
A. 是一种强酸
B. 非金属性:
C. 原子半径:
D. 中,的化合价为+2价
14. 反应经历两步:①;②。反应体系中、、的浓度随时间的变化曲线如图4所示。下列说法不正确的是( )
A. 为随的变化曲线
B. 时,
C. 时,的消耗速率大于生成速率
D. 后,
15. 宏观辨识与微观探析是化学学科核心素养之一。下列物质性质实验对应的反应方程式书写正确的是( )
A. 放入水中:
B. 通过灼热铁粉:
C. 钢丝插入热的浓硫酸中:
D. 通入酸性溶液中:
16. 钴()的合金材料广泛应用于航空航天、机械制造等领域。图5为水溶液中电解制备金属钴的装置示意图。下列说法正确的是( )
A. 工作时,Ⅰ室和Ⅱ室溶液的均增大
B. 生成,Ⅰ室溶液质量理论上减少
C. 移除两交换膜后,石墨电极上发生的反应不变
D. 电解总反应:
二、非选择题:共56分。第17~19题为必考题,考生都必须作答。第20~21题为选考题,考生根据要求作答。
(一)必考题:共42分。
17.(15分)
含氯物质在生产生活中有重要作用。1774年,舍勒在研究软锰矿(主要成分是)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素组成的单质,并命名为chlorine(中文命名“氯气”)。
(1)实验室沿用舍勒的方法制取的化学方程式为___________。
(2)实验室制取干燥时,净化与收集所需装置的接口连接顺序为___________。
(3)某氯水久置后不能使品红溶液褪色,可推测氯水中__________已分解。检验此久置氯水中存在的操作及现象是___________。
(4)某合作学习小组进行以下实验探究。
①实验任务 通过测定溶液电导率,探究温度对溶解度的影响。
②查阅资料 电导率是表征电解质溶液导电能力的物理量。温度一定时,强电解质稀溶液的电导率随溶液中离子浓度的增大而增大;离子浓度一定时,稀溶液电导率随温度的升高而增大。时,。
③提出猜想 猜想a:较高温度的饱和溶液的电导率较大。
猜想b:在水中的溶解度。
④设计实验、验证猜想 取试样Ⅰ、Ⅱ、Ⅲ(不同温度下配制的饱和溶液),在设定的测试温度下,进行表1中实验1~3,记录数据。
表1
实验序号 | 试样 | 测试温度/ | 电导率/ |
1 | Ⅰ:的饱和溶液 | 25 | |
2 | Ⅱ:的饱和溶液 | 35 | |
3 | Ⅲ:的饱和溶液 | 45 |
⑤数据分析、交流讨论 的饱和溶液中,__________。
实验结果为。小组同学认为,此结果可以证明③中的猜想成立,但不足以证明猜想成立。结合②中信息,猜想不足以成立的理由有_______________。
⑥优化实验 小组同学为进一步验证猜想,在实验1~3的基础上完善方案,进行实验4和5。请在答题卡上完成表2中内容。
表2
实验序号 | 试样 | 测试温度/ | 电导率/ |
4 | Ⅰ | __________ | |
5 | __________ | __________ |
⑦实验总结 根据实验1~5的结果,并结合②中信息,小组同学认为猜想也成立。猜想成立的判断依据是____________。
18.(13分)
对废催化剂进行回收可有效利用金属资源。某废催化剂主要含铝()、钼()、镍()等元素的氧化物,一种回收利用工艺的部分流程如下:
已知:时,的,;;;该工艺中,时,溶液中元素以的形态存在。
(1)“焙烧”中,有生成,其中元素的化合价为____________。
(2)“沉铝”中,生成的沉淀为______________。
(3)“沉钼”中,为7.0。
①生成的离子方程式为__________。
②若条件控制不当,也会沉淀。为避免中混入沉淀,溶液中___________(列出算式)时,应停止加入溶液。
(4)①滤液Ⅲ中,主要存在的钠盐有和,为___________。
②往滤液Ⅲ中添加适量固体后,通入足量______________(填化学式)气体,再通入足量,可析出。
(5)高纯(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图6所示,图中所示致密保护膜为一种氧化物,可阻止刻蚀液与下层(砷化镓)反应。
①该氧化物为___________。
②已知:和同族,和同族。在与上层的反应中,元素的化合价变为+5价,则该反应的氧化剂与还原剂物质的量之比为___________。
19.(14分)
我国力争于2030年前做到碳达峰,2060年前实现碳中和。与重整是利用的研究热点之一。该重整反应体系主要涉及以下反应:
)
)
)
)
)
(1)根据盖斯定律,反应的______________(写出一个代数式即可)。
(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有__________。
A. 增大与的浓度,反应、、的正反应速率都增加
B. 移去部分,反应、、的平衡均向右移动
C. 加入反应的催化剂,可提高的平衡转化率
D. 降低反应温度,反应的正、逆反应速率都减小
(3)一定条件下,分解形成碳的反应历程如图7所示。该历程分_________步进行,其中,第________步的正反应活化能最大。
(4)设为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为)除以()。反应、、的随(温度的倒数)的变化如图8所示。
①反应、、中,属于吸热反应的有__________(填字母)。
②反应的相对压力平衡常数表达式为__________。
③在图8中点对应温度下、原料组成为、初始总压为的恒容密闭容器中进行反应,体系达到平衡时的分压为。计算的平衡转化率,写出计算过程。
(5)用途广泛,写出基于其物理性质的一种用途:____________________。
21. [选修5:有机化学基础](14分)
天然产物Ⅴ具有抗疟活性,某研究小组以化合物Ⅰ为原料合成Ⅴ及其衍生物Ⅵ的路线如下(部分反应条件省略,表示):
(1)化合物Ⅰ中含氧官能团有____________(写名称)。
(2)反应①的方程式可表示为:,化合物的分子式为__________。
(3)化合物Ⅳ能发生银镜反应,其结构简式为__________。
(4)反应②③④中属于还原反应的有___________,属于加成反应的有___________。
(5)化合物Ⅵ的芳香族同分异构体中,同时满足如下条件的有___________种,写出其中任意一种的结构简式:__________。
条件:)能与反应;)最多能与2倍物质的量的反应;)能与3倍物质的量的发生放出的反应;)核磁共振氢谱确定分子中有6个化学环境相同的氢原子;)不含手性碳原子(手性碳原子是指连有4个不同的原子或原子团的饱和碳原子)。
(6)根据上述信息,写出以苯酚的一种同系物及为原料合成的路线__________(不需注明反应条件)。
2022年广东省普通高中学业水平选择性考试化学试题(解析版): 这是一份2022年广东省普通高中学业水平选择性考试化学试题(解析版),共27页。试卷主要包含了考生必须保持答题卡的整洁, 劳动开创未来等内容,欢迎下载使用。
2023年广东省普通高中学业水平选择性考试临考化学预测押题密卷: 这是一份2023年广东省普通高中学业水平选择性考试临考化学预测押题密卷,共10页。
2023年广东省普通高中学业水平选择性考试冲刺卷(二) 化学 PDF版: 这是一份2023年广东省普通高中学业水平选择性考试冲刺卷(二) 化学 PDF版,共19页。












