






人教版 (新课标)选修2 化学与技术第二单元 化学与资源开发利用课题1 获取洁净的水课前预习ppt课件
展开2、你认为水污染还有其它原因吗?
实验:在一杯浑浊的黄河水中撒入一药匙明矾粉末,观察现象。写出有关的离子方程式。
KAl(SO4)2= Al3+ +K++2 SO42-Al3+ + 3H2O Al(OH)3 + 3H+
结论:绿矾净水效果不如明矾
绿矾溶于水呈酸性,但碱性条件下更易氧化,使用时将PH调至9,变成效果更好的三价铁离子
水中呈胶体状态的污染物质,通常都带有负电荷,若向水中投加带相反电荷的电解质(混凝剂),可是污水中的胶体颗粒失去稳定性,并在分子引力作用下凝聚成大颗粒而下沉。通过混凝法可除去污水中细分散固体颗粒、乳状油及胶状物质。目前常用的混凝剂有:明矾、碱式氯化铝、铁盐等。注意:含铝混凝剂处理饮用水的安全性。
硬水溶有较多量的钙离子,镁离子的水。 如矿泉水,自来水,以及自然界中的地面水和地 下水等。软水只溶有少量或者不含钙离子,镁离子的水。如雨水,雪水,纯净水等。
矿泉水和蒸馏水有什么区别?
最初硬度是指水能溶解肥皂的程度
现在主要指水中含钙离子镁离子的浓度
☆硬度定义 1升水中含有10mmgCaO 或者相当于10mmgCaO)称为1度(1。)
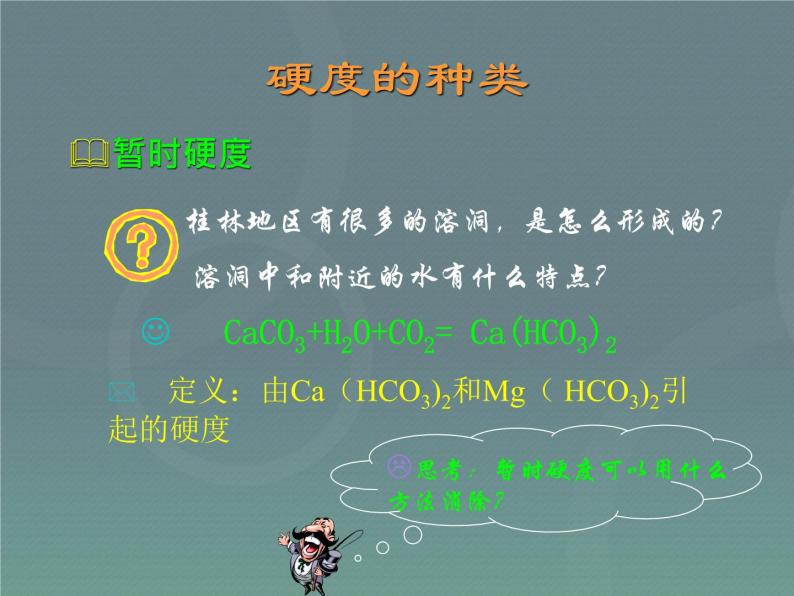
CaCO3+H2O+CO2= Ca(HCO3)2
定义:由Ca(HCO3)2和Mg( HCO3)2引 起的硬度
煮沸暂时硬水时的反应:
请翻看书后的溶解度附表,说出CaCO3 和MgCO3 溶解度的差别。
CaCO3不溶, MgCO3 微溶
所以碳酸镁在进一步加热的条件下还可以与水反应生成更难溶的氢氧化镁。
所以水垢的主要成分是CaCO3和Mg(OH)2 ,可以用稀盐酸洗,但是为了防止腐蚀设备,需要加入合适的缓蚀剂。
?思考:钙和镁形成的可溶性盐还有哪些?
还有:硫酸钙 硫酸镁 氯化钙 硝酸钙 硝酸镁
?思考:可以也象暂时硬水那样煮沸消除吗? 提示: 用反证法思考 比如说:假如氯化镁加热煮沸能反应的话, 生成什么物质?可能吗?
定义: 由钙镁硫酸盐和氯化物引起的,不能用煮沸法消除的硬度叫做永久硬度。
看课本:水中有哪些阴离子?哪些阳离子?
水的硬度往往是暂时硬度和永久硬度的总和。
阴离子有:HCO3-,CO32-,Cl-,SO42-,NO3- 等阳离子有:Ca2+ ,Mg2+ 等
硬水和软水硬水:硬度大于8度的水软水:硬度小于8度的水自然界中只有雨水、雪水这样的结晶水才是纯软水。
蒸馏水 暂时硬水 永久硬水
你还能想出其他方法来吗?
3.有一最硬水,硬度是由碳酸氢镁引起的,测定硬度为30度。取一升这种水,常压下加热蒸发,最后得到残渣多少克?
【分析】 硬度的计算是把镁离子折算成氧化钙,只含有碳酸氢镁的暂时硬水加热煮沸,最后得到的残渣是氢氧化镁。
所以: 水中相当于含有钙离子的质量: m=30度*10毫克/度=300毫克钙离子看成是以氧化钙的形式,所以钙离子的物质的量为 n=300/56 毫摩尔一个钙离子由一个镁离子折算得到,所以n镁离子=n钙离子=300/56毫摩尔=0.3/56摩尔最后镁离子转化为氢氧化镁,质量为: 0.32/56*58=0.31克
返回
硬水的危害
长期饮用硬度过高的水对人体健康不利 高硬度水中与结合SO42-有苦涩味,还会使人的肠胃功能紊乱,出现站是性的腹胀,排气多,腹泻等现象。久居南方的人初到北方,开始一段时间会出现“水土不服”的现象,是因为北方不少地方饮用硬度比较高的地下水,而时间长了,胃肠逐渐适应后,这种现象就会随之消失。
那么硬水毫无是处了吗?
不对,否则怎么会有那么多的人要买矿泉水喝呢?
原来钙和镁都是生命必需元素中的宏量金属元素科学和医学家们还调查发现,人的某些心血管疾病,如高血压和动脉硬化性心脏病的死亡率,与饮水的硬度成反比,水质硬度低,死亡率反而高。长期饮用过硬或者过软的水都不利与人体健康。我国规定:饮用水的硬度不得超过25度
硬水对我们的生产和生活也有很大的危害 洗涤———浪费肥皂 锅炉———结成水垢,危害生产 所以,我们必须将硬水进行软化。那么,就让我们接着学习硬水软化的方法吧!
返回
煮沸法离子交换法石灰-纯碱法其他方法
仅仅适用于软化 硬水
碳质离子交换剂 离子交换树脂 ——磺化煤(黑色颗粒,不溶于酸碱)
碳质离子交换剂:磺化煤 NaR 烟煤和褐煤用发烟硫或 浓硫酸处理后的产物 钠离子可以交换水中的钙镁离子
交换: 2NaR+Ca2+=CaR2+2Na+ 2NaR+Mg2+=MgR2+2Na+
交换过程
返回
交换并非是无止境的。当交换后的水不再符合软水的标准时, 磺化煤就失效了,需要
再生: 用8%~10%的食盐水浸泡 磺化煤交换剂。 CaR2+2Na+=2NaR+Ca2+ MgR2+2Na+=2NaR+Mg2+
再生过程是交换过程的逆过程。
交换: 2NaR+Ca2+=CaR2+2Na+ 2NaR+Mg2+=MgR2+2Na+
水质变化: 原水硬度降低 阴离子基本不变 钠离子数目大大增加
磺化煤缺点:不耐热,交换容量小,再生剂消耗大。 交换容量和原水硬度以及再生水平有关,影响因素较多。
优点:质量高,占地小,设备简单,操 作方便。
性状:透明或半透明,颜色有黄色,白色 等,形状 有交换膜,球状,柱状等
用途:纯水制取(H型+OH型)硬水软化, 原料提纯,有机合成等。
缺点:原水硬度和碱度高时,经济效益不 好。
工业上也用化学药剂来软化硬水。 CaO白色粉末CaO+H2O=Ca(OH)2 (避免灰尘污染)
想想还有哪些可能发生的反应?
1、了解家用简易净水器的工作原理。
2、利用滤纸、木炭粉、细沙、沙砾、碎石、棉花等物品制作简易过滤器。。
每一层分别放上:滤纸、木炭粉、细沙、沙砾、碎石、棉花等
高中课题1 获取洁净的水教案配套课件ppt: 这是一份高中课题1 获取洁净的水教案配套课件ppt,共15页。PPT课件主要包含了获取洁净的水,FeSO4·7H2O,来源充足,化学软化法,MgCO3,污水处理,污水处理的程度,二级三级,中和法,范围酸性和碱性废水等内容,欢迎下载使用。
人教版 (新课标)选修2 化学与技术课题1 获取洁净的水评课课件ppt: 这是一份人教版 (新课标)选修2 化学与技术课题1 获取洁净的水评课课件ppt,共19页。PPT课件主要包含了本节课的学习目标,天然水的净化,混凝法,明矾或绿矾,肥皂水法,泡沫少有大量浮渣,有大量泡沫无浮渣,化学软化法,加热法,蒸发皿底部有白色固体等内容,欢迎下载使用。
高中化学第二单元 化学与资源开发利用课题1 获取洁净的水教课课件ppt: 这是一份高中化学第二单元 化学与资源开发利用课题1 获取洁净的水教课课件ppt,共20页。PPT课件主要包含了水为什么要净化,本节课的学习目标,天然水的净化,混凝法,明矾或绿矾,肥皂水法,泡沫少有大量浮渣,有大量泡沫无浮渣,化学软化法,加热法等内容,欢迎下载使用。













