




初中化学人教版九年级上册课题 3 利用化学方程式的简单计算示范课课件ppt
展开利用化学方程式进行计算的策略
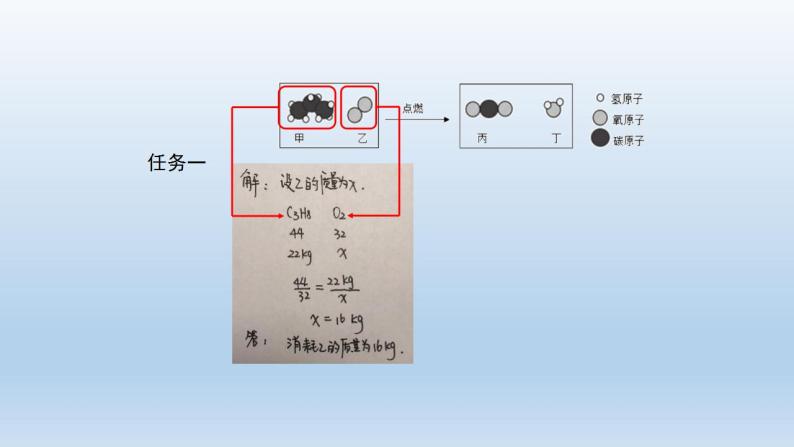
丙烷(C3H8)是液化石油气的主要成分之一,燃烧前后分子种类变化微观示意图如下。根据图示回答:已知反应物甲消耗的质量为22 kg,求反应中消耗乙的质量为 。
相对原子质量 H 1 C 12 O 16
答:消耗乙的质量为80 kg。
解:设消耗乙的质量为x。
液氢是火箭升空的常用燃料。若火箭升空至少要携带100 kg液氢,充分燃烧才能获得足够的能量。试计算100 kg液氢完全燃烧后产生水的质量是多少?
相对原子质量 H 1 O 16
化学变化中存在的质量关系
参加反应的各物质质量总和=反应后生成的各物质质量总和
各物质之间存在固定的质量比
反应前后元素的质量守恒
若火箭升空时携带了100 kg 液氢,火箭助燃仓中填充1000 kg 液氧。待充分反应后,求产生水的质量是多少?
100 kg + 1000 kg = 1100 kg
2H2 + O2 2H2O
x = 800 kg
答:消耗液氧的质量为800 kg。
解:设消耗液氧的质量为x。
100 kg + 800 kg = 900 kg
经分析,参加反应的液氧质量为800 kg
解:经分析,100 kg液氢全部参加了反应
x = 900 kg
答:生成水的质量为900 kg。
解:经分析,800 kg液氧参加了反应
参加了反应/反应生成的物质质量
贝壳中含有大量碳酸钙,对废弃贝壳资源化利用的有效途径之一是高温煅烧贝壳,生产主要成分为氧化钙的建筑材料,发生反应的化学方程式是:某工厂回收了200 t废弃贝壳,其中碳酸钙的质量分数是91%,则理论上可生产氧化钙的质量是多少?
CaCO3 CaO + CO2
相对原子质量 H 1 C 12 O 16 Ca 40
解:设生成氧化钙的质量为x。
x = 101.92 t
答:生成氧化钙的质量为101.92 t。
参加了反应/反应生成的纯净物质量
如图是“快长高”补钙剂商品的含量标签图。小乙同学想测定其碳酸钙的含量标注是否属实。
测出每片钙片中碳酸钙的质量
与1.24 g 比较
实验过程:取出4片片剂,研碎后放入烧杯中。加入稀盐酸,至不再放出气体为止,共用去稀盐酸40.0 g,称量烧杯中剩余物质质量为47.8 g。(不含烧杯质量,已知钙片中其他成分不与稀盐酸反应)
CaCO3+2HCl=CaCl2+H2O+CO2
资料1 碳酸钙与盐酸反应生成氯化钙、水、二氧化碳。资料2 盐酸是氯化氢气体和水的混合物。
1.块状固体→粉末2.目的是增大反应物之间的接触面积,使反应更充分。
1.反应结束2.碳酸钙已反应完全
钙片的总质量4×2.5 g =10 g
混合物质量包含:HCl、H2O
混合物质量包含:氯化钙、水、未反应的其他物质
答:该钙片中的成分含量标注属实。
设碳酸钙的总质量为x。
CaCO3+2HCl=CaCl2+ H2O+CO2
5 g÷4 =1.25 g
1.25 g﹥1.24 g,属实
4×2.5 g = 10 g
40 g + 10 g - 47.8 g = 2.2 g
1.写2.2 g的来源
2.计算CaCO3的质量
定量计算在生活实际中应用广泛
1.精准控制反应物用量
2.测定混合物中某物质的含量
1.用“ ”和“ ”分别代表两种不同的单质分子A2和B2,它们在一定条件下能发生化学反应,其反应的微观示意图如下:
若3 g A2完全反应,得到17 g产物。已知B2的相对分子质量为28,则生成物的相对分子质量为 。
2021学年课题 3 利用化学方程式的简单计算说课课件ppt: 这是一份2021学年课题 3 利用化学方程式的简单计算说课课件ppt,共21页。PPT课件主要包含了质量守恒定律,未知数,化学方程式,相对分子质量,化学计量数,已知量,92g,在O2下面,漏掉比例式,∶1∶2等内容,欢迎下载使用。
初中化学人教版九年级上册课题 3 利用化学方程式的简单计算备课课件ppt: 这是一份初中化学人教版九年级上册课题 3 利用化学方程式的简单计算备课课件ppt,共10页。PPT课件主要包含了课前导入,该怎么计算呢,正比例,课堂探究,解题注意,课堂练习等内容,欢迎下载使用。
化学课题 3 利用化学方程式的简单计算复习ppt课件: 这是一份化学课题 3 利用化学方程式的简单计算复习ppt课件,共19页。PPT课件主要包含了学习目标,重点难点,55%等内容,欢迎下载使用。