

晶体综合计算 高考化学一轮复习强化提升课学案新人教版
展开晶体综合计算
本部分知识在高考中更多是以主观填空题形式考查,考查学生分析图象的能力,能正确分析晶胞或简单结构中所含的粒子个数、粒子位置关系,从而计算粒子间距、晶体密度、空间利用率等。考查了晶体结构、定量计算,考查了宏观辨识与微观探析、证据推理和模型认知。
命题角度1.粒子间距的计算
【典例1】(2019·全国Ⅰ卷节选)在普通铝中加入少量Cu和Mg后,形成一种称为拉维斯相的MgCu2微小晶粒,其分散在Al中可使得铝材的硬度增加、延展性减小,形成所谓“坚铝”,是制造飞机的主要材料。
图(a)是MgCu2的拉维斯结构,Mg以金刚石方式堆积,八面体空隙和半数的四面体空隙中,填入以四面体方式排列的Cu。图(b)是沿立方格子对角面取得的截图。可见,Cu原子之间最短距离x=__________pm,Mg原子之间最短距离
y=__________pm。设阿伏加德罗常数的值为NA,则MgCu2的密度是__________g·cm-3(列出计算表达式)
。
【解析】根据晶胞结构可知Cu原子之间最短距离为面对角线的,由于棱长是a pm,则面对角线是a pm,则x=a pm;Mg原子之间最短距离为体对角线的,由于棱长是a pm,则体对角线是a pm,则y=a;根据晶胞结构可知晶胞中含有镁原子的个数是8×+6×+4=8,则Cu原子个数为16,晶胞的质量是 g。由于棱长是a pm,则MgCu2的密度
g·cm-3。
答案:a a
命题角度2.粒子坐标的计算
【典例2】(2019·全国Ⅱ卷节选)近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为FeSmAsFO组成的化合物。
一种四方结构的超导化合物的晶胞如图1所示,晶胞中Sm和As原子的投影位置如图2所示。
以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图1中原子1的坐标为(,,),则原子2和3的坐标分别为________、________。
【解析】图1中原子1的坐标为(,,),原子2位于面心,坐标为
(,,0),原子3位于棱心,坐标为(0,0,)。
答案:(,,0) (0,0,)
命题角度3.晶体密度的计算
【典例3】(2020·全国Ⅱ卷节选)钙钛矿(CaTiO3)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料,回答下列问题:
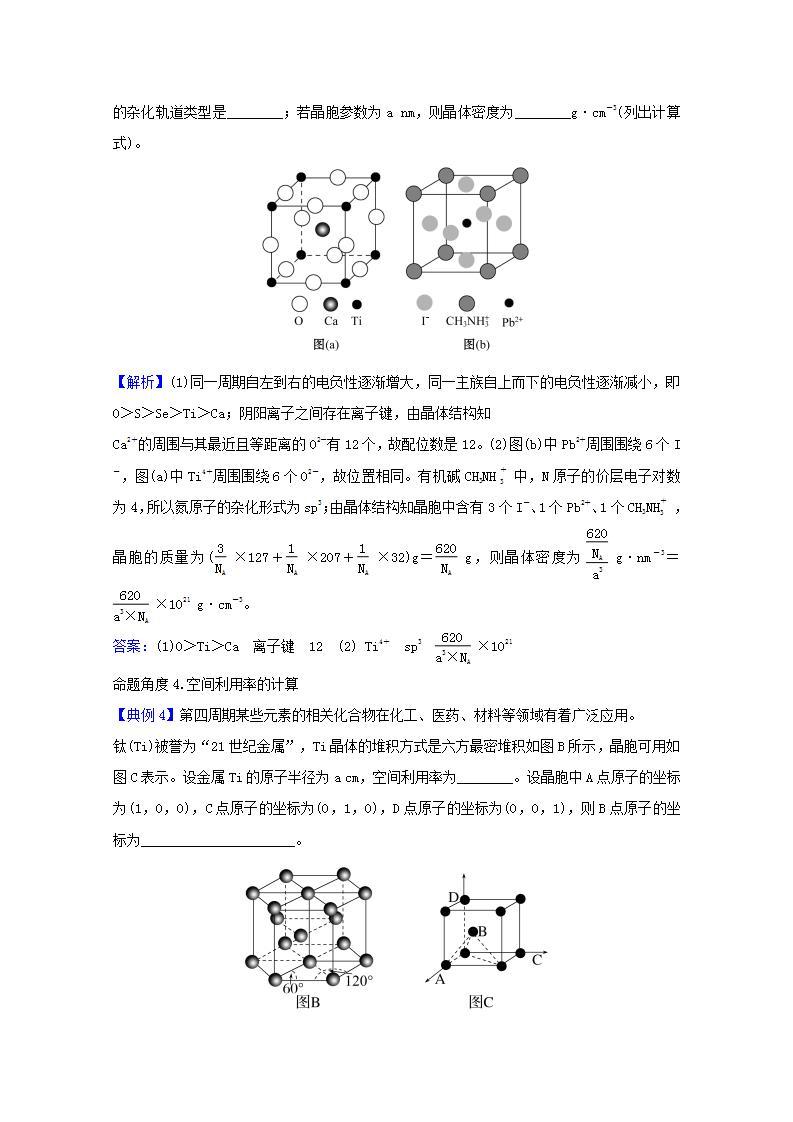
(1)CaTiO3的晶胞如图(a)所示,其组成元素的电负性大小顺序是________;金属离子与氧离子间的作用力为________,Ca2+的配位数是________。
(2)一种立方钙钛矿结构的金属卤化物光电材料的组成为Pb2+、I-和有机碱离子CH3NH,其晶胞如图(b)所示。其中Pb2+与图(a)中________的空间位置相同,有机碱CH3NH中,N原子的杂化轨道类型是________;若晶胞参数为a nm,则晶体密度为________g·cm-3(列出计算式)。
【解析】(1)同一周期自左到右的电负性逐渐增大,同一主族自上而下的电负性逐渐减小,即O>S>Se>Ti>Ca;阴阳离子之间存在离子键,由晶体结构知
Ca2+的周围与其最近且等距离的O2-有12个,故配位数是12。(2)图(b)中Pb2+周围围绕6个I-,图(a)中Ti4+周围围绕6个O2-,故位置相同。有机碱CH3NH中,N原子的价层电子对数为4,所以氮原子的杂化形式为sp3;由晶体结构知晶胞中含有3个I-、1个Pb2+、1个CH3NH,晶胞的质量为(×127+×207+×32)g=g,则晶体密度为g·nm-3=×1021 g·cm-3。
答案:(1)O>Ti>Ca 离子键 12 (2) Ti4+ sp3 ×1021
命题角度4.空间利用率的计算
【典例4】第四周期某些元素的相关化合物在化工、医药、材料等领域有着广泛应用。
钛(Ti)被誉为“21世纪金属”,Ti晶体的堆积方式是六方最密堆积如图B所示,晶胞可用如图C表示。设金属Ti的原子半径为a cm,空间利用率为________。设晶胞中A点原子的坐标为(1,0,0),C点原子的坐标为(0,1,0),D点原子的坐标为(0,0,1),则B点原子的坐标为______________________。
【解析】晶胞中B与连线原子形成正四面体,紧密相邻,设金属Ti的原子半径为a cm,则晶胞底面棱长为2a cm,晶胞底面为菱形,锐角为60°,底面积=
2a cm×2a cm×sin60°=2 a2 cm2,正四面体的高= cm=a cm,故晶胞的高为2×a cm,晶胞体积=2a2 cm2×2×a cm,晶胞中Ti原子数目为2,晶胞中原子总体积=2×πa3 cm3,空间利用率=[2×πa3 cm3÷(2a2 cm2×2×a cm)]×100%=×100%≈74%。由各原子坐标参数,可知A处于x轴,C处于y轴,D处于z轴,B处于晶胞中三棱锥的中心位置,距离上、下底面距离相等,为B的参数z的值=0.5,B在底面投影B′处于AC连线上且AB′长度为AC长度的。则B′到左侧面距离为C的,即为参数y=×1=,则B′到后平面距离为A的,即为参数x=×1=,故B的坐标为(,,)。
答案:74% (,,)
1.晶胞计算相关公式:
(1)晶胞质量=晶胞占有的微粒的质量=晶胞占有的微粒数×。
(2)晶体中体心立方堆积、面心立方堆积中的几组公式(设棱长为a)
①面对角线长=a。
②体对角线长=a。
③体心立方堆积4r=a(r为原子半径)。
④面心立方堆积4r=a(r为原子半径)。
(3)空间利用率=。
2.涉及晶胞图的相关计算:
(1)计算晶胞中的粒子数目或计算化学式。
(2)计算晶胞参数,如密度、摩尔质量、粒子在空间的坐标点。
(3)计算晶胞中粒子之间的距离。
1.(粒子间距的计算)(2021·武汉模拟)自从第一次合成稀有气体元素的化合物XePtF6以来,人们又相继发现了氙的一系列化合物,如XeF2、XeF4等。图甲为XeF4的结构示意图,图乙为XeF2晶体的晶胞结构图。下列有关说法错误的
是( )
A.XeF4是由极性键构成的非极性分子
B.XeF2晶体属于分子晶体
C.一个XeF2晶胞中实际拥有4个XeF2
D.XeF2晶体中距离最近的两个XeF2之间的距离为(a为晶胞参数)
【解析】选C。根据XeF4的结构示意图判断,Xe和F之间形成极性键,该分子为平面正方形,为非极性分子,故A正确;XeF2为一个分子,XeF2晶体由这样的分子构成,所以是分子晶体,故B正确;一个XeF2晶胞中实际拥有XeF2的数目为8×+1=2个,故C错误;根据晶胞结构分析,体心的XeF2与每个顶点的XeF2之间的距离最近,最近的距离为,故D正确。
2.(粒子坐标的计算)(2021·枣庄模拟)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。氧化镍原子分数坐标参数A为(0,0,0),B为(1,1,1),则C的坐标参数为( )
A.(,,) B.(1,1,)
C.(,1,) D.(1,,)
【解析】选D。C位于右侧面的面心处,已知A为(0,0,0),B为(1,1,1),则C在xy平面的投影为(1,),在z方向投影为,所以C的坐标参数为
(1,,)。
3.(晶体密度的计算)(2021·日照模拟)钒的某种氧化物的立方晶胞结构如图所示,晶胞参数为a pm。下列说法错误的是( )
A.该钒的氧化物的化学式为VO2
B.V原子在该晶体中的堆积方式为体心立方
C.V原子的配位数与O原子的配位数之比为1∶2
D.该晶胞的密度为 g·cm-3
【解析】选C。晶胞中V原子位于顶点和体心,数目为1+8×=2;O原子位于上下面上和体内,数目=2+4×=4,二者原子数目之比为1∶2,故氧化物化学式为VO2,故A正确;晶胞中V原子位于顶点和体心,符合体心立方的堆积方式,故B正确;体心V原子的配位数为6,O原子配位数为3,所以V原子的配位数与O原子的配位数之比为2∶1,故C错误;m= g,V=a3 pm3=(a×10-10)3 cm3,ρ== g·cm-3,故D正确。
4.(粒子坐标、晶体密度的计算)(2021·厦门模拟)我国科学家合成太阳能电池材料(CH3NH3)PbI3,其晶体结构如图,属于立方晶系,晶体密度为ρ g·cm-3。其中A代表(CH3NH3)+;原子坐标参数A为(0,0,0),B为(,,),下列说法错误的是( )
A.B代表Pb2+
B.每个晶胞含有I-的数目为6
C.M的原子坐标参数为(,,0)
D.(CH3NH3)PbI3的摩尔质量为ρ·a3×6.02×10-7 g·mol-1
【解析】选B。A的数目为8×+4×=2个,A代表(CH3NH3)+;而B代表微粒数也为2,则B是Pb2+,故A正确;每个晶胞含有I-数目为6×=3个,不是6个,故B错误;M点处于xOy面,坐标是(,,0),故C正确;取1 mol晶胞,则有6.02×1023个晶胞,1 mol晶胞质量为M g,密度为ρ= g·cm-3,所以摩尔质量为M=ρ·a3·6.02×10-7 g·mol-1,故D正确。
5.(粒子间距、晶体密度的计算)(1)①KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立方结构,棱长为a=0.446 nm,晶胞中K、I、O分别处于顶角、体心、面心位置,如图1所示。K与O间的最短距离为__________nm,与K紧邻的O个数为____________。
②在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则K处于__________位置,O处于__________位置。
(2)MgO具有NaCl型结构(如图2),晶胞面对角线上的O2-紧密相邻,X射线衍射实验测得MgO 的晶胞参数为a=0.420 nm,则r(O2-)为__________nm。MnO也属于NaCl型结构,晶胞参数为a′=0.448 nm,则r(Mn2+)为__________nm。
【解析】(1)①K与O间的最短距离为面对角线的一半,则K与O间的最短距离为×0.446 nm≈0.315 nm,以顶点K研究,与之相邻的O位于面心,顶点为12个面共有,面心为2个晶胞共用,即与K紧邻的O个数为=12;
②将图中晶胞扩展为2×2×2结构,8个晶胞体心的8个I构成新立方晶胞的顶点,可知K处于新晶胞体心、O原子处于新晶胞棱心。
(2)MgO晶胞面对角线上的O2-紧密相邻,2个O2-核间距(即2个O2-半径之和)等于晶胞棱长的,故r(O2-)=0.420 nm××≈0.148 nm,2r(O2-)+
2r(Mn2+)=0.448 nm,则 r(Mn2+)=0.076 nm。
答案:(1)①0.315 12 ②体心 棱心
(2)0.148 0.076
【加固训练—拔高】
1.食盐晶体是由钠离子(图中的“”)和氯离子(图中的“”)组成的,且均为等距离的交错排列。已知食盐的密度是2.2 g·cm-3,阿伏加德罗常数为6.02×1023 mol-1。在食盐晶体中两个距离最近的钠离子中心间的距离最接近
于( )
A.3.0×10-8 cm B.3.5×10-8 cm
C.4.0×10-8 cm D.5.0×10-8 cm
【解析】选C。从NaCl晶体结构模型中分割出一个小立方体,如图所示,
a表示其棱长,d表示两个Na+中心间的距离。每个小立方体含Na+:×4=,含Cl-:×4=,即每个小立方体含Na+—Cl-离子对个。则有
a3·2.2 g·cm-3=,解得a≈2.81×10-8 cm,又因为d=a,故食盐晶体中两个距离最近的Na+中心间的距离为d=×2.81×10-8 cm≈4.0×
10-8 cm。
2.如图依次为金刚石、CuO的晶胞结构。
(1)假设金刚石晶胞中相邻的碳原子紧密相切,则金刚石晶胞图中空间利用率为__________(保留两位有效数字,=1.732)
(2)CuO为四方晶胞(a=b≠c,α=β=γ=90°)图中黑球代表________(填写“氧”或“铜”),白球的配位数为__________,CuO的密度是______________g·cm-3(保留两位有效数字)
【解析】(1)一个晶胞中含碳原子数为8×+6×+4=8,令碳原子直径为a,晶胞中C原子总体积=8×π()3,碳原子与周围的4个原子形成正四面体结构,中心碳原子与正四面体顶点原子相邻,其连线处于体对角线上,且为对角线长的,故体对角线长为4a,故棱长为a,则晶胞体积为(a)3,晶胞空间利用率={[8×π()3]÷(a)3}×100%≈34%。
(2)Cu原子半径大于氧原子半径,故黑色球为O元素,CuO中Cu、O原子配位数相等,黑色球配位数为4,则白色球的配位数为4,晶胞中Cu原子数、O原子数目均为4,晶胞质量为4×g,则晶胞密度为4×g
÷[(400×10-10cm)2×500×10-10cm]≈6.6 g·cm-3。
答案:(1)34% (2)氧 4 6.6
“热重曲线”分析 高考化学一轮复习强化提升课学案新人教版: 这是一份“热重曲线”分析 高考化学一轮复习强化提升课学案新人教版,共8页。学案主要包含了归纳总结,加固训练——拔高等内容,欢迎下载使用。
中和滴定的拓展应用 高考化学一轮复习强化提升课学案新人教版: 这是一份中和滴定的拓展应用 高考化学一轮复习强化提升课学案新人教版,共10页。学案主要包含了加固训练—拔高等内容,欢迎下载使用。
实验操作的规范描述 高考化学一轮复习强化提升课学案新人教版: 这是一份实验操作的规范描述 高考化学一轮复习强化提升课学案新人教版,共9页。学案主要包含了归纳总结,加固训练—拔高等内容,欢迎下载使用。













