






初中科粤版第六章 金属6.2 金属的化学性质习题ppt课件
展开1.金属活动性顺序(1)金属活动性依次减弱的顺序K _______ Na _______ _______ Zn _______ Sn Pb (H) _______Hg _______ Pt Au。(2)金属活动性顺序的应用:金属的位置越靠前,它的活动性_________;排在___________的金属能置换出稀盐酸、稀硫酸里的_______;位于_______________能把位于_______________从它们的化合物溶液里置换出来。
2.置换反应:(1)概念:由一种_________与一种___________生成另一种_________和另一种___________的反应。(2)通式:A+BC→___________。
知识点一 置换反应1.(2020·湘西中考)下列化学反应中不属于置换反应的是( )A.Fe+H2SO4===FeSO4+H2↑B.CO+CuO Cu+CO2C.Cl2+2NaI===2NaCl+I2D.Fe+CuSO4===FeSO4+Cu
2.下列化学反应属于置换反应的是( )A.Zn+H2SO4===ZnSO4+ H2↑B.Ba(OH)2+H2SO4===BaSO4↓+2H2OC.4Fe(OH)2+O2+2H2O===4Fe(OH)3D.2HgO 2Hg+ O2↑
3.我国第四套人民币硬币中含有金属镍(Ni),镍及其化合物能发生下列反应: ①Ni+2HCl===NiCl2+H2↑;②NiO+2HCl===NiCl2+H2O;③NiO2+4HCl===NiCl2+Cl2↑+2H2O分析化学方程式,回答以下问题:(1)上述三个反应_______属于置换反应。(2)金属镍((Ni)与硝酸银溶液反应的化学方程式为________________________________。(3)反应③中Ni的化合价在反应前后_________(填“不变”“升高”或“降低”)。
Ni+2AgNO3===Ni(NO3)2+2Ag
知识点二 金属活动性顺序及其应用4.(2021·柳州质检)下列金属,不能置换出盐酸中的氢,但能置换出AgNO3溶液中银的是( )A.Mg B.Cu C.Al D.Fe5.《天工开物》是世界上第一部关于农业和手工业生产的综合性著作,里面详细记述了金、锌、铜、铁等金属的开采和冶炼方法。上述金属中金属活动性最强的是( )A.金 B.锌 C.铜 D.铁
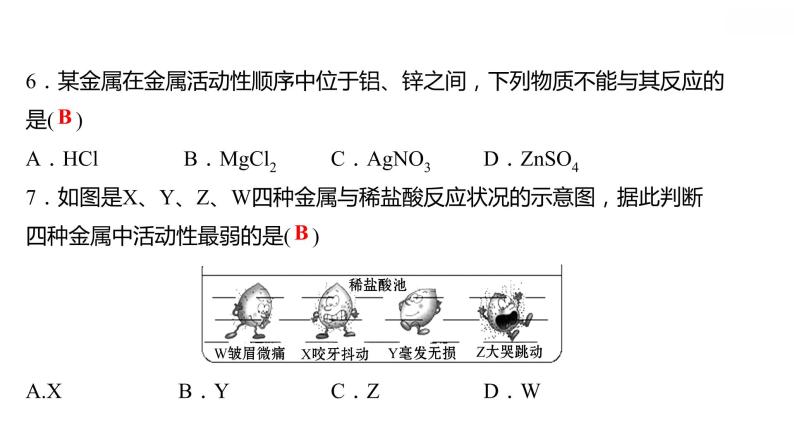
6.某金属在金属活动性顺序中位于铝、锌之间,下列物质不能与其反应的是( )A.HCl B.MgCl2 C.AgNO3 D.ZnSO47.如图是X、Y、Z、W四种金属与稀盐酸反应状况的示意图,据此判断四种金属中活动性最弱的是( )A.X B.Y C.Z D.W
8.(2021·梧州质检)下列物质中能由金属与稀酸直接反应得到的是( )A.AgCl B.CuSO4 C.ZnSO4 D.FeCl39.(2020·聊城中考)把X、Y、Z三种金属分别加入稀盐酸中,Y表面有气泡产生,X、Z无明显变化;再把X放到Z的硝酸盐溶液中,X的表面有固体析出,则三种金属的活动性顺序是( )A.Y>X>Z B.Y>Z>XC.X>Z>Y D.Z>X>Y
10.(2020·河池中考)下列各组物质能验证Al、Cu、Ag三种金属活动性强弱的是( )A.Al、Cu、Ag、稀盐酸B.Cu、Al2(SO4)3溶液、AgNO3溶液C.Al、Cu、AgNO3溶液D.Ag、Al2(SO4)3溶液、Cu(NO3)2溶液
11.金属材料在日常生活、工农业生产和科学研究中占有重要地位。(1)在野外遇到雷电天气,要远离铁塔以防雷击,是因为铁具有_________性。(2)在铝、铜、银三种金属中,最容易被氧化的是____________。探究铝、铜、银的活动性顺序,除铝、铜、银外,还需用的一种试剂是__________溶液(填化学式)。
12.(2021·都安质检) 若金属锰(Mn)在金属活动性顺序中位于铝和锌之间,则下列反应不正确的是( )A.Mn+H2SO4===MnSO4 + H2 ↑B.Mg+MnSO4===Mn+MgSO4C.Fe+MnSO4===Mn+FeSO4D.Mn+CuSO4===MnSO4+Cu
13.某同学为验证锌、铜、银三种金属的活动性顺序,他设计了以下四种实验方案,其中不能达到实验目的的是( )A.将Zn丝、Ag丝分别放入CuSO4溶液中B.将Zn丝分别放入Cu(NO3)2溶液、AgNO3溶液中C.将Cu丝分别放入Zn(NO3)2 溶液和AgNO3溶液中D.将Zn丝、Cu丝分别放入稀硫酸中,将Ag丝放入CuSO4溶液中
14.下列说法符合图中漫画情景的是( )A.此反应可能是化合反应B.若金属1是锌,金属2可能是银C.此反应可能是Cu+2AgCl===2Ag+CuCl2D.比较铁和铜活动性强弱可用硫酸镁溶液
15.(2021·岑溪质检)把等质量的X、Y、Z、M四种金属分别加入同体积、同浓度的足量稀盐酸中。再把Y加入MNO3溶液中。反应关系如图所示。据此判断四种金属的活动性顺序为( )A.Z>X>M>Y B.X>Z>Y>MC.X>Z>M>Y D.Y>M>Z>X
16.下列事实,不能判断X、Y的金属活动性强弱的是( )A.X能与盐酸反应而Y不能B.X能从Y的化合物的溶液中置换出YC.X能在空气中燃烧而Y不能D.在化合物中X显+3价,Y显+2价
17.(2021·贵港质检)有X、Y、Z三种金属,把Y投入X(NO3)2溶液中,Y表面有X析出,溶液质量增大;把X投入Z(NO3)2溶液中,得到X(NO3)2,溶液质量减小。下列判断错误的是( )A.X、Y、Z可能依次是Cu、Fe、AgB.元素的相对原子质量可能是Z>Y>XC.金属活动性顺序是Y>X>Z D.X、Y、Z可能依次是Fe、Zn、Hg
18.(2020·贺州质检)向盛有氯化亚铁和氯化铜的混合溶液的烧杯中加入一定量的镁粉,充分反应后,得到固体M和溶液N。下列叙述错误的是( )A.当镁无剩余时,M中一定有Cu,可能有FeB.当镁无剩余时,N中一定有MgCl2和FeCl2C.当镁有剩余时,M中一定有Fe、Cu和MgD.当镁有剩余时,N中一定没有FeCl2、CuCl2
【自我挑战】19.(2020·眉山中考)金属制品与我们的日常生活密不可分。(1)有铝、锌、铜三种金属,其中不能与稀硫酸发生反应的是____________。(2)铝的化学性质比较活泼,但铝制品具有很好的抗腐蚀性能,其原因是铝表面容易形成_______________________。
初中化学科粤版九年级下册6.2 金属的化学性质授课ppt课件: 这是一份初中化学科粤版九年级下册6.2 金属的化学性质授课ppt课件,共17页。
初中化学科粤版九年级下册6.2 金属的化学性质习题ppt课件: 这是一份初中化学科粤版九年级下册6.2 金属的化学性质习题ppt课件,共25页。PPT课件主要包含了覆盖一层,红色物质,置换反应,活动性较强,活动性较弱,较活泼的金属,稀硫酸和稀盐酸,一类的稀酸,不活泼的金属,CuSO4等内容,欢迎下载使用。
初中化学科粤版九年级下册6.2 金属的化学性质习题课件ppt: 这是一份初中化学科粤版九年级下册6.2 金属的化学性质习题课件ppt,共25页。PPT课件主要包含了金属氧化物,A+BC―→AC+B,Mg3N2,置换反应,H2O,FeSO4等内容,欢迎下载使用。













