

高考化学真题汇编专题15:化学实验
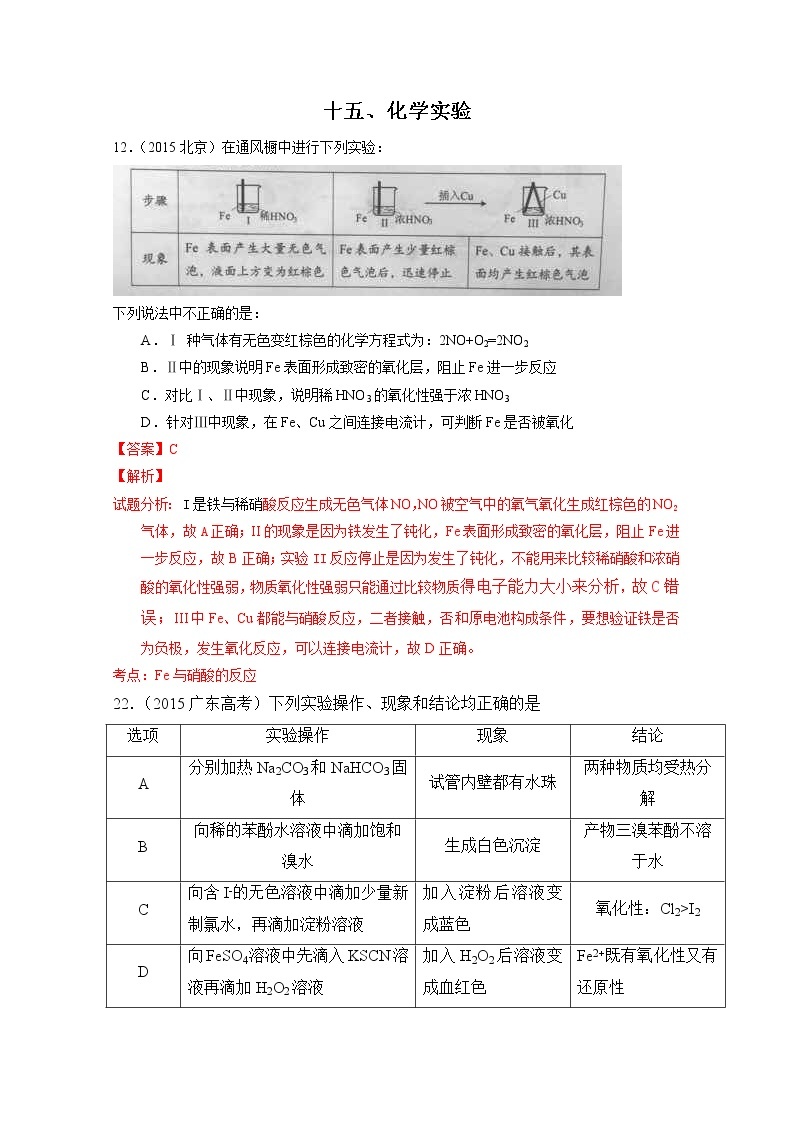
展开下列说法中不正确的是:
A.Ⅰ 种气体有无色变红棕色的化学方程式为:2NO+O2=2NO2
B.Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C.对比Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3
D.针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化
【答案】C
【解析】
试题分析: I是铁与稀硝酸反应生成无色气体NO,NO被空气中的氧气氧化生成红棕色的NO2气体,故A正确;II的现象是因为铁发生了钝化,Fe表面形成致密的氧化层,阻止Fe进一步反应,故B正确;实验II反应停止是因为发生了钝化,不能用来比较稀硝酸和浓硝酸的氧化性强弱,物质氧化性强弱只能通过比较物质得电子能力大小来分析,故C错误;III中Fe、Cu都能与硝酸反应,二者接触,否和原电池构成条件,要想验证铁是否为负极,发生氧化反应,可以连接电流计,故D正确。
考点:Fe与硝酸的反应
22.(2015广东高考)下列实验操作、现象和结论均正确的是
【答案】BC
11.(2015山东高考)下列由实验现象得出的结论正确的是:
【答案】C
【解析】
试题分析:A、Cl‾与I‾浓度不相等,不能比较Ksp,错误;B、该溶液可能含有Fe2+或Fe3+,错误;C、上层呈橙红色,说明Cl2与NaBr反应生成了Br2和NaCl,则Br‾的还原性强于Cl‾,正确;D、不是升华,试管底部NH4Cl分解生成NH3和HCl,试管口NH3与HCl反应生成了NH4Cl,错误。
考点:化学实验、元素及化合物
10.(2015新课标1高考)下列实验中,对应的现象以及结论都正确且两者具有因果关系的是( )
【答案】D
【解析】
试题分析:A、稀硝酸与过量的Fe分反应,则生成硝酸亚铁和NO气体、水,无铁离子生成,所以加入KSCN溶液后,不变红色,现象错误;B、Cu与硫酸铁发生氧化还原反应,生成硫酸铜和硫酸亚铁,无黑色固体出现,现象错误;C、铝在空气中加热生成氧化铝的熔点较高,所以内部熔化的铝不会滴落,错误;D、硫酸镁与氢氧化钠溶液反应生成氢氧化镁沉淀,再加入硫酸铜,则生成氢氧化铜蓝色沉淀,沉淀的转化符合由溶解度小的向溶解度更小的沉淀转化,所以氢氧化铜的溶度积比氢氧化镁的溶度积小,正确,答案选D。
12.(2015安徽)某同学将光亮的镁条放入盛有NH4Cl溶液的试管中,有大量气泡产生。为探究该反应原理,该同学做
了以下试验并观察到相关现象,由此得出的结论不合理的是:
【答案】C
【解析】
试题分析:A、检验氨气的方法正确,故A正确;B、火焰成淡蓝色,该气体为H2,B正确;C、氯化铵溶
液呈酸性,使金属镁氧化,故C错误;D、NaHCO3溶液呈弱碱性,故D正确;此题选C
28.(2015安徽)(14分)某研究小组将纯净的SO2气体通入0.1ml·L-1的Ba(NO3)2溶液中,得到了BaSO4沉淀,为探究上述溶液中何种微粒能氧化通入的SO2,该小组突出了如下假设:
假设一:溶液中的NO3-
假设二:溶液中溶解的O2
验证假设
该小组涉及实验验证了假设一,请在下表空白处填写相关实验现象
(2)为深入研究该反应,该小组还测得上述两个实验中溶液的pH随通入SO2体积的变化曲线入下图
实验1中溶液pH变小的原因是____;V1时,实验2中溶液pH小于实验1的原因是(用离子方程式表示)_________。
验证假设二
请设计实验验证假设二,写出实验步骤,预期现象和结论。
若假设二成立,请预测:在相同条件下,分别通入足量的O2和KNO3,氧化相同的H2SO3溶液(溶
液体积变化忽略不计),充分反映后两溶液的pH前者_______(填大于或小于)后者,理由是___________
【答案】(1)无现象、白色沉淀生成(2)SO2溶于水后生成H2SO3,亚硫酸显酸性,故pH值减小;SO2 +H2OH2SO3 H2SO32H+ +SO32-,H++NO3-=HNO3,硝酸酸性大于亚硫酸;
(3)大于,前者是将H2SO3氧化成硫酸,后者是生成硝酸,硝酸的酸性大于硫酸,故前者pH大于后者。
26.(2015新课标1高考)草酸(乙二酸)存在于自然界的植物中,其K1=5.4×10-2,K2=5.4×10-5。草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水。草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,易溶于水,受
热脱水、升华,170℃以上分解。回答下列问题:
(1)甲组同学按照如图所示的装置,通过实验检验草酸晶体的分解产物。装置C中可观察到的现象是_________,由此可知草酸晶体分解的产物中有_______。装置B的主要作用是________。
(2)乙组同学认为草酸晶体分解的产物中含有CO,为进行验证,选用甲组实验中的装置A、B和下图所示的部分装置(可以重复选用)进行实验。
①乙组同学的实验装置中,依次连接的合理顺序为A、B、______。装置H反应管中盛有的物质是_______。
②能证明草酸晶体分解产物中有CO的现象是_______。
(3)①设计实验证明:
①草酸的酸性比碳酸的强______。
②草酸为二元酸______。
【答案】⑴有气泡产生,澄清石灰水变浑浊;CO2;冷凝分解产物中的水和甲酸。
⑵ ①F、D、G、H、D; CuO(氧化铜);
②H前的装置D中的石灰水不变浑浊,H后的装置D中的石灰水变浑浊;
⑶ ① 向1ml/Ld的NaHCO3溶液中加入1ml/L的草酸溶液,若产生大量气泡则说明草酸的酸性比碳酸强。
② 将浓度均为0.1ml/L的草酸和氢氧化钠溶液等体积混合,测反应后的溶液的pH,若溶液呈酸性,则说明草酸是二元酸。
33.(2015广东高考)(17分)NH3及其盐都是重要的化工原料。
(1)用NH4Cl和Ca(OH)2制备NH3,反应发生、气体收集和尾气处理装置依次为
(2)按图13装置进行NH3性质实验。
①先打开旋塞1,B瓶中的现象是 ,原因是 ,稳定后,关闭旋塞1。
②再打开旋塞2,B瓶中的现象是 。
(3)设计实验,探究某一种因素对溶液中NH4Cl水解程度的影响。
限制试剂与仪器:固体NH4Cl、蒸馏水、100mL容量瓶、烧杯、胶头滴管、玻璃棒、药匙、天平、PH计、温度计、恒温水浴槽(可控制温度)
①实验目的:探究 对溶液中NH4Cl水解程度的影响。
②设计实验方案,拟定实验表格,完整体现实验方案(列出能直接读取数据的相关物理量及需拟定的数据,数据用字母表示;表中V(溶液)表示所配制溶液的体积)。
③按实验序号I所拟数据进行实验,若读取的待测物理量的数值为Y,则NH4Cl水解反应得平衡转化率为 (只列出算式,忽略水自身电离的影响)。
【答案】(1)ACG(2)①产生白色的烟;氯化氢与氨气反应生成了氯化铵小颗粒,氯化铵小颗粒形成白烟。②烧杯中的石蕊溶液会倒流进入到B瓶中。(3)①温度
②
③
(10-Y×5.35)/m
27.(2015北京)(14分)
研究CO2在海洋中的转移和归宿,是当今海洋科学研究的前沿领域。
溶于海水的CO2主要以4种无机碳形式存在,其中HCO3-占95%,写出CO2溶于水产生HCO3-的方程式: 。
在海洋循环中,通过右图所示的途径固碳。
①写出钙化作用的离子方程式: 。
②同位素示踪法证实光合作用释放出的O2只来自于H2O,用18O标记物质的光合作用的化学方程式如下,将其补充完整: + ===(CH2O)x+x18O2+xH2O
海水中溶解无机碳占海水总碳的95%以上,其准确测量是研究海洋碳循环的基础,测量溶解无机碳, 可采用如下方法:
①气提、吸收CO2,用N2从酸化后的还说中吹出CO2并用碱液吸收(装置示意图如下),将虚线框中的装置补充完整并标出所用试剂。
②滴定。将吸收液洗后的无机碳转化为NaHCO3,再用xml/LHCl溶液滴定,消耗ymlHCl溶液,海水中溶解无机碳的浓度= ml/L。
利用右图所示装置从海水中提取CO2,有利于减少环境温室气体含量。
①结合方程式简述提取CO2的原理: 。
②用该装置产生的物质处理b室排出的海水,合格后排回大海。处理至合格的方法是 。
【答案】 (1)CO2+H2OHCO3-+H+
(2)①Ca2++ 2HCO3-=== CaCO3↓+ CO2+H2O
②xCO2 + 2x H218O
(3)①
②xy/z
(4)①a室发生阳极反应:4OH--4e-== O2+2H2O,c(OH-)下降,H2OOH-+H+平衡右移,c(H+)增大,H+从a室进入b室,发生反应:HCO3-+H+== CO2+H2O。 ②中和法
【解析】
试题分析:(1)考查碳酸的第1步电离:CO2+H2OHCO3-+H+
(2)①根据反应物是HCO3-,生成物是CaCO3和CO2,易知本题的反应方程式。
Ca2++ 2HCO3-=== CaCO3↓+ CO2+H2O 。
②根据元素守恒法,及示踪原子的标记可知方程式中的填空为:xCO2 + 2x H218O
(3)①注意酸化的试剂要用硫酸,一定不能用盐酸,HCl会挥发出来影响后续的滴定。
②该滴定过程转化的关系式为:
CO2 ~ HCO3-~ HCl
1 1
n(CO2) x ml/L×y×10-3L
解得:n(CO2)=xy×10-3ml 所以:c(CO2) =xy/z ml/L
(4)①海水pH>8,显碱性,需要H+中和降低海水的碱性,a室发生阳极反应:4OH--4e-== O2+2H2O, c(OH-)下降,H2OOH-+H+平衡右移,c(H+)增大,H+从a室进入b室,发生反应:HCO3-+H+== CO2+H2O。
②中和法,阴极H+放电,H2OOH-+H+平衡右移,c(H+)增大,c(OH-)增大, b室的Na+移向c室,产生NaOH,可用于中和显酸性的海水,再排回大海。
考点:盐类水解、方程式书写、化学实验、化学平衡移动、电解、化学计算等。
选项
实验操作
现象
结论
A
分别加热Na2CO3和NaHCO3固体
试管内壁都有水珠
两种物质均受热分解
B
向稀的苯酚水溶液中滴加饱和溴水
生成白色沉淀
产物三溴苯酚不溶于水
C
向含I-的无色溶液中滴加少量新制氯水,再滴加淀粉溶液
加入淀粉后溶液变成蓝色
氧化性:Cl2>I2
D
向FeSO4溶液中先滴入KSCN溶液再滴加H2O2溶液
加入H2O2后溶液变成血红色
Fe2+既有氧化性又有还原性
操作及现象
结论
A
向AgCl悬浊液中加入NaI溶液时出现黄色沉淀。
Ksp(AgCl)< Ksp(AgI)
B
向某溶液中滴加氯水后再加入KSCN溶液,溶液呈红色。
溶液中一定含有Fe2+
C
向NaBr溶液中滴入少量氯水和苯,振荡、静置,溶液上层呈橙红色。
Br—还原性强于Cl—
D
加热盛有NH4Cl固体的试管,试管底部固体消失,试管口有晶体凝结。
NH4Cl固体可以升华
选项
实验
现象
结论
A.
将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液
有气体生成,溶液呈血红色
稀硝酸将Fe氧化为Fe3+
B.
将铜粉加1.0ml·L-1Fe2(SO4)3溶液中
溶液变蓝、有黑色固体出现
金属铁比铜活泼
C.
用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热
熔化后的液态铝滴落下来
金属铝的熔点较低
D.
将0.1ml·L-1MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1ml·L-1CuSO4溶液
先有白色沉淀生成后变为浅蓝色沉淀
Cu(OH)2的溶度积比Mg(OH)2的小
选项
实验及现象
结论
A
将湿润的红色石蕊试纸放在试管口,试纸变蓝
反应中有NH3产生
B
收集产生的气体并点燃,火焰呈淡蓝色
反应中有H2产生
C
收集气体的同事测得溶液的pH为8.0
弱碱性溶液中Mg也可被氧化
D
将光亮的镁条放入pH为8.6的NaHCO3溶液中,有气泡产生
弱碱性溶液中OH-氧化了Mg
实验步骤
实验现象
结论
实验1:在盛有不含O2的25ml0.1ml/LBaCl2溶液的烧杯中,缓慢通入纯净的SO2气体
假设一成立
实验2:在盛有不含O2的25ml0.1ml/LBa(NO3)2溶液的烧杯中,缓慢通入纯净的SO2气体
实验步骤、预期现象和结论(不要求写具体操作过程)
实验步骤
实验现象
结论
实验1:在盛有不含O2的25ml0.1ml/LBaCl2溶液的烧杯中,缓慢通入纯净的SO2气体
无现象
假设二成立
实验2:在盛有富含O2的25ml0.1ml/LBaCl2溶液的烧杯中,缓慢通入纯净的SO2气体
有白色沉淀生成
物理量
实验序号
V(溶液)/mL
NH4Cl质量(g)
pH
温度(℃)
1
100
m
Y
T1
2
100
m
Z
T2
2023年高考化学真题分类汇编 专题10 化学实验基础: 这是一份2023年高考化学真题分类汇编 专题10 化学实验基础,文件包含专题10化学实验基础解析版docx、专题10化学实验基础原卷版docx等2份试卷配套教学资源,其中试卷共29页, 欢迎下载使用。
高考化学真题和模拟题分类汇编专题15化学实验基本方法(2份打包,含解析+原卷版,可预览): 这是一份高考化学真题和模拟题分类汇编专题15化学实验基本方法(2份打包,含解析+原卷版,可预览),文件包含高考化学真题和模拟题分类汇编专题15化学实验基本方法含解析doc、高考化学真题和模拟题分类汇编专题15化学实验基本方法原卷版doc等2份试卷配套教学资源,其中试卷共66页, 欢迎下载使用。
高考化学真题和模拟题分类汇编15化学实验基本方法含解析: 这是一份高考化学真题和模拟题分类汇编15化学实验基本方法含解析,共52页。试卷主要包含了多选题,单选题等内容,欢迎下载使用。