



2019年天津卷理综化学高考真题及答案解析(原卷+解析卷)
展开2019年普通高等学校招生个国统一考试(天津卷)理科综合
化学部分
理科综合共300分,考试用时150分钟。
化学试卷分为第Ⅰ卷(选择题)和第Ⅱ卷两部分,第Ⅰ卷1至2页,第Ⅱ卷3至6页,共100分。
答卷前,考生务必将自己的姓名、准考号填写在答题卡上,并在规定位置粘贴考试用条形码。答卷时,考生务必将答案涂写在答题卡上,答在试卷上的无效。考试结束后,将本试卷和答题卡一并交回。
祝各位考生考试顺利!
第Ⅰ卷
注意事项:
1.每题选出答案后,用铅笔将答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。
2.本卷共6题,每题6分,共36分。在每题给出的四个选项中,只有一项是最符合题目要求的。
以下数据可供解题时参考:
相对原子质量:
1. 化学在人类社会发展中发挥着重要作用,下列事实不涉及化学反应的是( )
A. 利用废弃的秸秆生产生物质燃料乙醇
B. 利用石油生产塑料、化纤等高分子材料
C. 利用基本的化学原料生产化学合成药物
D. 利用反渗透膜从海水中分离出淡水
【答案】D
【解析】
【分析】化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变化,化学变化和物理变化的本质区别是否有新物质生成;据此分析判断.
【详解】A、秸杆主要成分为纤维素,利用废弃的秸秆生产生物质燃料乙醇,有新物质生成,属于化学变化,故A涉及化学反应;
B、利用石油生产塑料、化纤等高分子材料,产生新物质,属于化学变化,故B涉及化学反应;
C、利用基本化学原料生产化学合成药,产生新物质,属于化学变化,故C涉及化学反应;
D、海水中的水淡化成淡水,没有产生新物质,属于物理变化,故D不涉及化学反应;
故选D。
【点睛】本题考查物理变化与化学变化的区别与联系,难度不大,解答时要分析变化过程中是否有新物质生成,若没有新物质生成属于物理变化,若有新物质生成属于化学变化.
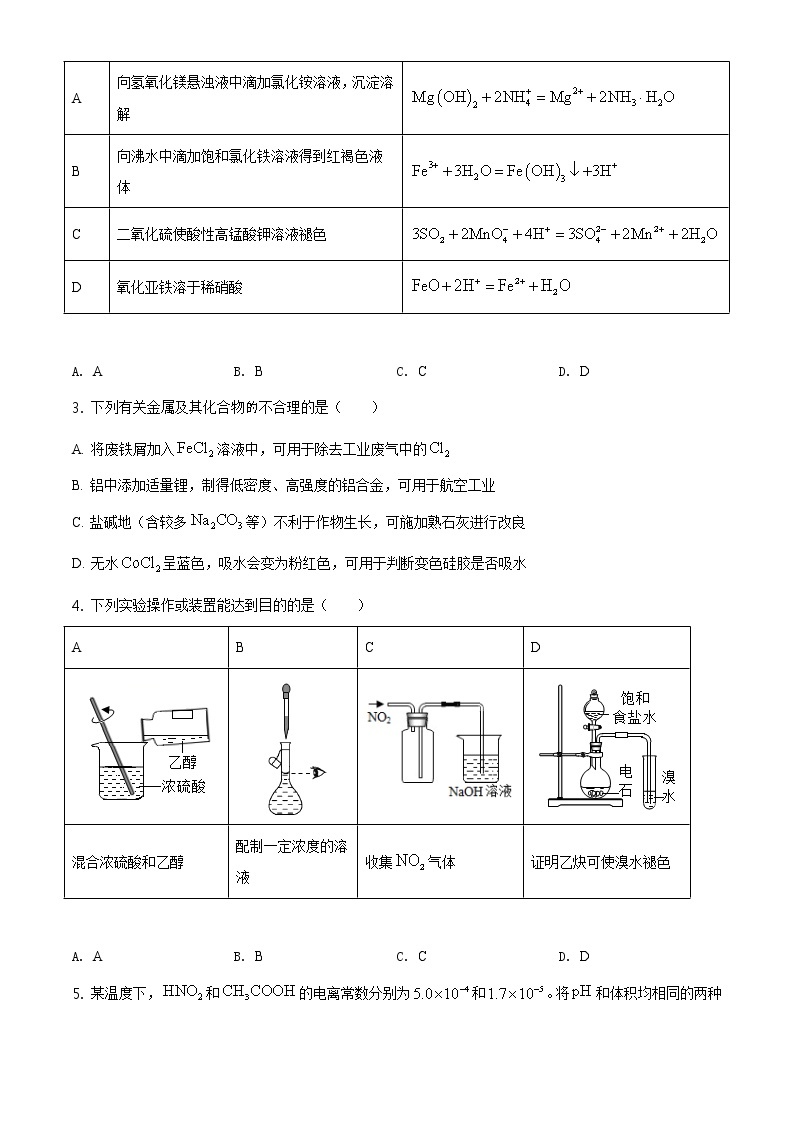
2. 下列离子方程式能用来解释相应实验现象的是( )
A. AB. BC. CD. D
【答案】A
【解析】
【分析】A、氢氧化镁碱性强于氨水;
B、制氢氧化铁胶体条件是加热,在化学式后注明胶体,得不到沉淀;
C、电荷不守恒;
D、硝酸具有强氧化性,将亚铁氧化成铁离子;
【详解】A、氢氧化镁碱性强于氨水,故A能用来解释相应实验现象;
B、制氢氧化铁胶体条件是加热,在化学式后注明胶体,得不到沉淀,离子方程式为:Fe3++3H2OFe(OH)3(胶体)+3H+,故B不能用来解释相应实验现象;
C、电荷不守恒,正确的离子方程式为:5SO2+2MnO4-+2H2O=2Mn2++4H++5SO42-,故C不能用来解释相应实验现象;
D、硝酸具有强氧化性,其可将亚铁氧化成铁离子,正确的离子方程式为:3FeO+10H++NO3-=3Fe3++NO↑+5H2O,故D不能用来解释相应实验现象;
故选A。
【点睛】本题考查离子反应方程式书写,解题关键:结合原理正确书写离子方程式,难点C:氧化还原反应的离子方程式的书写,配平前不能将H+写在反应物中,应先配电子转移守恒,再通过电荷守恒将H+补在生成物中。
3. 下列有关金属及其化合物的不合理的是( )
A. 将废铁屑加入溶液中,可用于除去工业废气中的
B. 铝中添加适量锂,制得低密度、高强度的铝合金,可用于航空工业
C. 盐碱地(含较多等)不利于作物生长,可施加熟石灰进行改良
D. 无水呈蓝色,吸水会变为粉红色,可用于判断变色硅胶是否吸水
【答案】C
【解析】
【分析】A、氯气能将铁和亚铁氧化;
B、根据合金性质判断;
C、Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,产物仍然呈碱性;
D、利用无水氯化钴和氯化钴晶体的颜色不同。
【详解】A、铁和亚铁能将氯气还原为氯离子,从而除去工业废气中的氯气,故A不选;
B、根据铝合金的性质,铝合金具有密度低、强度高,故可应用于航空航天等工业,故B不选;
C、Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,产物仍然呈碱性,不能改变土壤碱性,反而使土壤更板结,故C选;
D、利用无水氯化钴和氯化钴晶体的颜色不同,故可根据颜色判断硅胶中是否能吸水,故D不选。
故选C
【点睛】本题考查金属元素及其化合物的应用,易错点C,除杂不只是将反应物反应掉,还要考虑产物在应用中是否符合要求,生成的NaOH仍然呈碱性,达不到降低碱度的目的。
4. 下列实验操作或装置能达到目的的是( )
A. AB. BC. CD. D
【答案】B
【解析】
【分析】A、乙醇的密度小于浓硫酸;
B、容量瓶上的刻度与凹液面的最低处相切;
C、二氧化氮的密度大于空气;
D、乙炔中的杂质也能使溴水褪色。
【详解】A、乙醇的密度小于浓硫酸,混合时应将浓硫酸沿烧杯壁倒入乙醇中,边倒边搅拌,若顺序相反则容易引起液体飞溅,故A不能达到目的;
B、容量瓶上的刻度与凹液面的最低处相切,胶头滴管垂直位于容量瓶的正上方,故B能达到目的;
C、二氧化氮的密度大于空气,集气瓶中的导气管应长进短出,故C不能达到目的;
D、乙炔中的H2S等杂质也能使溴水褪色,应先通过一个盛碱液的洗气瓶将杂质除去,故D不能达到目的;
故选B。
【点睛】本题考查实验装置和基本操作,易错点D,学生易忽略实验室用电石制乙炔中的H2S等还原性杂质也能使溴水褪色。
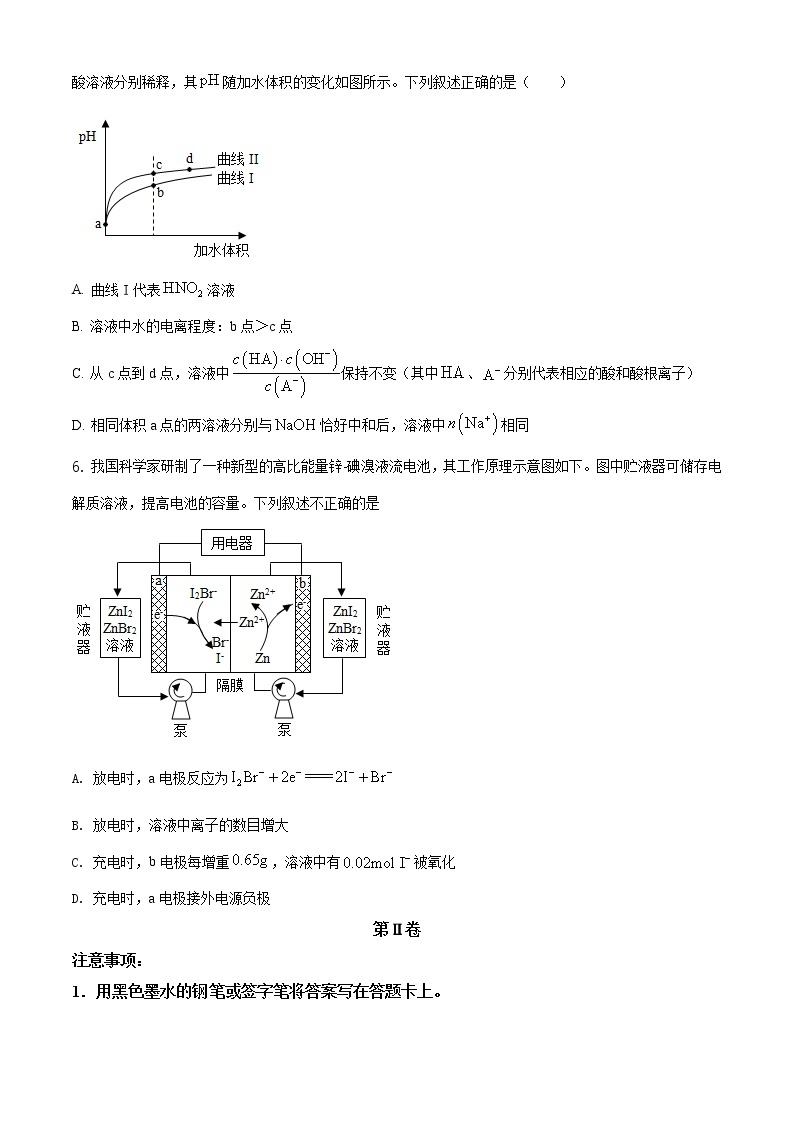
5. 某温度下,和的电离常数分别为和。将和体积均相同的两种酸溶液分别稀释,其随加水体积的变化如图所示。下列叙述正确的是( )
A. 曲线Ⅰ代表溶液
B. 溶液中水的电离程度:b点>c点
C. 从c点到d点,溶液中保持不变(其中、分别代表相应的酸和酸根离子)
D. 相同体积a点的两溶液分别与恰好中和后,溶液中相同
【答案】C
【解析】
【分析】电离常数HNO2大于CH3COOH,酸性HNO2大于CH3COOH;
A、由图可知,稀释相同的倍数,Ⅱ的变化大,则Ⅱ的酸性比I的酸性强,溶液中氢离子浓度越大,酸性越强;
B、酸抑制水电离,b点pH小,酸性强,对水电离抑制程度大;
C、kw为水的离子积常数,k(HNO2)为HNO2的电离常数,只与温度有关,温度不变,则不变;
D、体积和pH均相同的HNO2和CH3COOH溶液,c(CH3COOH)>c(HNO2)。
【详解】A、由图可知,稀释相同的倍数,Ⅱ的变化大,则Ⅱ的酸性比I的酸性强,Ⅱ代表HNO2,I代表CH3COOH,故A错误;
B、酸抑制水电离,b点pH小,酸性强,对水电离抑制程度大,故B错误;
C、Ⅱ代表HNO2,c(HNO2)c(OH-)/c(NO2-)=c(H+)·c(HNO2)c(OH-)/[c(H+)·c(NO2-)]=kw/k(HNO2),kw为水的离子积常数,k(HNO2)为HNO2的电离常数,这些常数只与温度有关,温度不变,则不变,故C正确;
D、体积和pH均相同的HNO2和CH3COOH溶液,c(CH3COOH)>c(HNO2),分别滴加同浓度的NaOH溶液至恰好中和,CH3COOH消耗的氢氧化钠溶液体积多,HNO2消耗的NaOH少,故D错误;
故选C。
【点睛】本题考查酸的稀释及图象,明确强酸在稀释时pH变化程度大及酸的浓度与氢离子的浓度的关系是解答本题的关键,难点C,要将已知的c(HNO2)c(OH-)/c(NO2-)分子和分值母同乘以c(H+),变成与kw为水的离子积常数和k(HNO2)为HNO2的电离常数相关的量,再判断。
6. 我国科学家研制了一种新型的高比能量锌-碘溴液流电池,其工作原理示意图如下。图中贮液器可储存电解质溶液,提高电池的容量。下列叙述不正确的是
A. 放电时,a电极反应为
B. 放电时,溶液中离子的数目增大
C. 充电时,b电极每增重,溶液中有被氧化
D. 充电时,a电极接外电源负极
【答案】D
【解析】
【分析】放电时,Zn是负极,负极反应式为Zn-2e-═Zn2+,正极反应式为I2Br-+2e-=2I-+Br-,充电时,阳极反应式为Br-+2I--2e-=I2Br-、阴极反应式为Zn2++2e-=Zn,只有阳离子能穿过交换膜,阴离子不能穿过交换膜,据此分析解答。
【详解】A、放电时,a电极为正极,碘得电子变成碘离子,正极反应式为I2Br-+2e-=2I-+Br-,故A正确;
B、放电时,正极反应式为I2Br-+2e-=2I-+Br-,溶液中离子数目增大,故B正确;
C、充电时,b电极反应式为Zn2++2e-=Zn,每增加0.65g,转移0.02ml电子,阳极反应式为Br-+2I--2e-=I2Br-,有0.02mlI-失电子被氧化,故C正确;
D、充电时,a是阳极,应与外电源的正极相连,故D错误;
故选D。
【点睛】本题考查化学电源新型电池,会根据电极上发生的反应判断正负极是解本题关键,会正确书写电极反应式,易错选项是B,正极反应式为I2Br-+2e-=2I-+Br-,溶液中离子数目增大。
第Ⅱ卷
注意事项:
1.用黑色墨水的钢笔或签字笔将答案写在答题卡上。
2.本卷共4题,共64分。
7. 氮、磷、砷、锑、铋、镆为元素周期表中原子序数依次增大的同族元素。回答下列问题:
(1)砷在元素周期表中的位置______。的中子数为______。
已知:(,白磷)=(,黑磷) ;
(,白磷)=(,红磷) ;
由此推知,其中最稳定的磷单质是______。
(2)氮和磷氢化物性质的比较:热稳定性:______(填“>”“<”)。
沸点:______(填“>”“<”),判断依据是______。
(3)和与卤化氢的反应相似,产物的结构和性质也相似。下列对与反应产物的推断正确的是______(填序号)。
a.不能与反应 b.含离子键、共价键 c.能与水反应
(4)能发生较强烈的水解,生成难溶的,写出该反应的化学方程式_______________________,因此,配制溶液应注意_______________________。
(5)在1L真空密闭容器中加入a ml PH4I固体,t℃时发生如下反应:
①
②
③
达平衡时,体系中,,,则℃时反应①的平衡常数值为______(用字母表示)。
【答案】 (1). 第四周期第VA族 (2). 173 (3). 黑磷 (4). > (5). > (6). 分子间存在氢键 (7). b、c (8). (“”写成“”亦可) (9). 加盐酸,抑制水解 (10).
【解析】
【详解】(1)砷元素的原子序数为33,与氮元素、磷元素均位于ⅤA族,最外层有5个电子,则砷在周期表中的位置为第四周期ⅤA族;288115Mc的质量数为288,质子数为115,由由中子数=质量数—中子数可知288115Mc的中子数为288—115=173;将已知转化关系依次编号为①②,由盖斯定律可知,①—②可得P(s,红磷)= P(s,黑磷)△H=△H1—△H2=(—39.3kJ/ml)—(—17.6 kJ/ml)=—21.7 kJ/ml。由于放热反应中,反应物总能量大于生成物总能量,则白磷、红磷和黑磷三者能量的大小顺序为白磷>红磷>黑磷,能量越高越不稳定,则最稳定的是黑磷,故答案为第四周期ⅤA族;173;黑磷;
(2)元素非金属性越强,氢化物的稳定性越强,N元素非金属性强于P元素,则NH3热稳定性强于PH3;N元素非金属性强,原子半径小,N2H4分子间可以形成氢键,增大分子间作用力,而PH3分子间不能形成氢键,则N2H4的沸点高于PH3,故答案为>;>;N2H4分子间形成氢键;
(3)由题意可知,PH3与NH3性质类似,与HI反应生成反应PH4I,PH4I能与氢氧化钠溶液反应生成PH3,a错误;PH4I为离子化合物,化合物中含有离子键和共价键,b正确;PH4I与NH4I类似,可以发生水解反应,c正确,bc正确,故答案为bc;
(4)由题意可知,SbCl3发生水解反应生成SbOCl沉淀和HCl,水解的化学方程式为SbCl3+H2O=SbOCl↓+2HCl;配制SbCl3溶液时,为防止SbCl3水解,应加入盐酸,故答案为SbCl3+H2O=SbOCl↓+2HCl;加入盐酸抑制SbCl3水解;
(5)由PH4I(s)PH3(g)+HI(g)可知,amlPH4I分解生成的物质的量的PH3和HI,由2HI(g)H2(g)+I2(g)可知HI分解生成c(H2)= c(I2)=cml/L,PH4I分解生成c(HI)为(2c+b)ml/L,则4 PH3(g)P4(g)+ 6H2(g)可知PH3分解生成c(H2)=(d—c)ml/L,则体系中c(PH3)为[(2c+b)—(d—c)] ml/L=,故反应PH4I(s)PH3(g)+HI(g)的平衡常数K=c(PH3)c(HI)=,故答案为。
【点睛】本题考查化学反应基本理论,涉及了物质结构、元素周期律、盖斯定律、盐类水解和化学平衡常数等知识,注意元素周期律的应用,掌握盖斯定律和化学平衡常数的计算方法,明确盐类水解的应用是解答关键。
8. 我国化学家首次实现了膦催化的环加成反应,并依据该反应,发展了一条合成中草药活性成分茅苍术醇的有效路线。
已知环加成反应:
(、可以是或)
回答下列问题:
(1)茅苍术醇的分子式为____________,所含官能团名称为____________,分子中手性碳原子(连有四个不同的原子或原子团)的数目为____________。
(2)化合物B的核磁共振氢谱中有______个吸收峰;其满足以下条件的同分异构体(不考虑手性异构)数目为______。
①分子中含有碳碳叁键和乙酯基
②分子中有连续四个碳原子在一条直线上
写出其中碳碳叁键和乙酯基直接相连的同分异构体的结构简式____________。
(3)的反应类型为____________。
(4)的化学方程式为__________________,除外该反应另一产物的系统命名为____________。
(5)下列试剂分别与和反应,可生成相同环状产物的是______(填序号)。
a. b. c.溶液
(6)参考以上合成路线及条件,选择两种链状不饱和酯,通过两步反应合成化合物,在方框中写出路线流程图(其他试剂任选)。_______
【答案】 (1). (2). 碳碳双键、羟基 (3). 3 (4). 2 (5). 5 (6). 和 (7). 加成反应或还原反应 (8). (9). 2-甲基-2-丙醇 (10). b (11). 或(写成等合理催化剂亦可)
【解析】
【分析】由有机物的转化关系可知,与CH3C≡CCOOC(CH3)3发生题给信息反应生成,与氢气在催化剂作用下发生加成反应生成,与甲醇在浓硫酸作用下,共热发生酯基交换反应生成,一定条件下脱去羰基氧生成,与氢气在催化剂作用下发生加成反应生成,一定条件下反应生成茅苍术醇。
【详解】(1)茅苍术醇的结构简式为,分子式为C15H26O,所含官能团为碳碳双键、羟基,含有3个连有4个不同原子或原子团的手性碳原子,故答案为C15H26O;双键、羟基;3;
(2)化合物B的结构简式为CH3C≡CCOOC(CH3)3,分子中含有两类氢原子,核磁共振氢谱有2个吸收峰;由分子中含有碳碳叁键和—COOCH2CH3,且分子中连续四个碳原子在一条直线上,则符合条件的B的同分异构体有、CH3CH2CH2C≡CCOOCH2CH3、CH3CH2C≡C—CH2COOCH2CH3、CH3—C≡C—CH2CH2COOCH2CH3和等5种结构,碳碳叁键和—COOCH2CH3直接相连的为、CH3CH2CH2C≡CCOOCH2CH3,故答案为2;5;、CH3CH2CH2C≡CCOOCH2CH3;
(3)C→D反应为与氢气在催化剂作用下发生加成反应(或还原反应)生成,故答案为加成反应(或还原反应);
(4)与甲醇与浓硫酸共热发生酯基交换反应生成,反应的化学方程式为,HOC(CH3)3的系统命名法的名称为2—甲基—2—丙醇,故答案为,2—甲基—2—丙醇;
(5)和均可与溴化氢反应生成,故答案为b;
(6)由题给信息可知,CH3C≡CCOOCH2CH3与CH2=COOCH2CH3反应生成,与氢气发生加成反应生成,故答案为。
【点睛】本题考查有机物推断与合成,对比物质的结构明确发生的反应,侧重对有机化学基础知识和逻辑思维能力考查,有利于培养自学能力和知识的迁移能力,需要熟练掌握官能团的结构、性质及相互转化。
9. 环己烯是重要的化工原料。其实验室制备流程如下:
回答下列问题:
Ⅰ.环己烯的制备与提纯
(1)原料环己醇中若含苯酚杂质,检验试剂为____________,现象为__________________。
(2)操作1的装置如图所示(加热和夹持装置已略去)。
①烧瓶A中进行的可逆反应化学方程式为________________________,浓硫酸也可作该反应的催化剂,选择而不用浓硫酸的原因为________________________(填序号)。
a.浓硫酸易使原料碳化并产生
b.污染小、可循环使用,符合绿色化学理念
c.同等条件下,用比浓硫酸的平衡转化率高
②仪器B的作用为____________。
(3)操作2用到的玻璃仪器是____________。
(4)将操作3(蒸馏)的步骤补齐:安装蒸馏装置,加入待蒸馏的物质和沸石,____________,弃去前馏分,收集83℃的馏分。
Ⅱ.环己烯含量的测定
在一定条件下,向环己烯样品中加入定量制得的,与环己烯充分反应后,剩余的与足量作用生成,用的标准溶液滴定,终点时消耗标准溶液(以上数据均已扣除干扰因素)。
测定过程中,发生的反应如下:
①
②
③
(5)滴定所用指示剂为____________。样品中环己烯的质量分数为____________(用字母表示)。
(6)下列情况会导致测定结果偏低的是____________(填序号)。
a.样品中含有苯酚杂质
b.在测定过程中部分环己烯挥发
c.标准溶液部分被氧化
【答案】 (1). 溶液 (2). 溶液显紫色 (3). (4). a、b (5). 减少环己醇蒸出 (6). 分液漏斗、烧杯 (7). 通冷凝水,加热 (8). 淀粉溶液 (9). (10). b、c
【解析】
【分析】I.(1)检验物质时通常是利用该物质的特殊性质,或利用不同物质间的性质差异。苯酚能与氯化铁溶液发生显色反应而醇不能,可依此设计用氯化铁溶液检验苯酚的存在;
(2)书写陌生情境的化学方程式时,一定要将题给的所有信息挖掘出来,比如题给的反应条件,如催化剂、加热的温度、此反应已明确指出的“可逆”;
(3)催化剂选择FeCl3·6H2O而不用浓硫酸的理由分析,显然要突出浓硫酸的缺点,突出FeCl3·6H2O的优点;
(4)在发生装置中加装冷凝管,显然是为了冷凝回流,提高原料的利用率。
(5)计算此问时尽可能采用关系式法,找到已知和未知之间的直接关系。
(6)误差分析时,利用相关反应式将量尽可能明确化。
【详解】I.(1)检验苯酚的首选试剂是FeCl3溶液,原料环己醇中若含有苯酚,加入FeCl3溶液后,溶液将显示紫色;
(2)①从题给的制备流程可以看出,环己醇在FeCl3·6H2O的作用下,反应生成了环己烯,对比环己醇和环己烯的结构,可知发生了消去反应,反应方程式为:,注意生成的小分子水勿漏写,题目已明确提示该反应可逆,要标出可逆符号,FeCl3·6H2O是反应条件(催化剂)别漏标;此处用FeCl3·6H2O而不用浓硫酸的原因分析中:a项合理,因浓硫酸具有强脱水性,往往能使有机物脱水至炭化,该过程中放出大量的热,又可以使生成的炭与浓硫酸发生反应:C+2H2SO4(浓) CO2↑+SO2↑+2H2O;b项合理,与浓硫酸相比,FeCl3·6H2O对环境相对友好,污染小,绝大部分都可以回收并循环使用,更符合绿色化学理念;c项不合理,催化剂并不能影响平衡转化率;
②仪器B为球形冷凝管,该仪器的作用除了导气外,主要作用是冷凝回流,尽可能减少加热时反应物环己醇的蒸出,提高原料环己醇的利用率;
(3)操作2实现了互不相溶的两种液体的分离,应是分液操作,分液操作时需要用到的玻璃仪器主要有分液漏斗和烧杯;
(4)题目中已明确提示了操作3是蒸馏操作。蒸馏操作在加入药品后,要先通冷凝水,再加热;如先加热再通冷凝水,必有一部分馏分没有及时冷凝,造成浪费和污染;
II.(5)因滴定的是碘单质的溶液,所以选取淀粉溶液比较合适;根据所给的②式和③式,可知剩余的Br2与反应消耗的Na2S2O3的物质的量之比为1:2,所以剩余 Br2的物质的量为:n(Br2)余=×cml·L-1×vmL×10-3L·mL-1=ml,反应消耗的Br2的物质的量为(b-)ml,据反应①式中环己烯与溴单质1:1反应,可知环己烯的物质的量也为(b-)ml,其质量为(b-)×82g,所以ag样品中环己烯的质量分数为:。
(6)a项错误,样品中含有苯酚,会发生反应:,每反应1mlBr2,消耗苯酚的质量为31.3g;而每反应1ml Br2,消耗环己烯的质量为82g;所以苯酚的混入,将使耗Br2增大,从而使环己烯测得结果偏大;b项正确,测量过程中如果环己烯挥发,必然导致测定环己烯的结果偏低;c项正确,Na2S2O3标准溶液被氧化,必然滴定时消耗其体积增大,即计算出剩余的溴单质偏多,所以计算得出与环己烯反应的溴单质的量就偏低,导致最终环己烯的质量分数偏低。
【点睛】①向规范、严谨要分数。要注意题设所给的引导限定词语,如“可逆”、“玻璃”等,这些是得分点,也是易扣分点。
②要计算样品中环己烯的质量分数,只需要算出环己烯的物质的量即可顺利求解。从所给的3个反应方程式可以得出:2Na2S2O3~I2~Br2~,将相关已知数据代入计算即可。
③对于a项的分析,要粗略计算出因苯酚的混入,导致单位质量样品消耗溴单质的量增加,最终使测得环己烯的结果偏高。
10. 多晶硅是制作光伏电池的关键材料。以下是由粗硅制备多晶硅的简易过程。
回答下列问题:
Ⅰ.硅粉与在300℃时反应生成气体和,放出热量,该反应的热化学方程式为________________________。的电子式为__________________。
Ⅱ.将氢化为有三种方法,对应的反应依次为:
①
②
③
(1)氢化过程中所需的高纯度可用惰性电极电解溶液制备,写出产生的电极名称______(填“阳极”或“阴极”),该电极反应方程式为________________________。
(2)已知体系自由能变,时反应自发进行。三个氢化反应的与温度的关系如图1所示,可知:反应①能自发进行的最低温度是____________;相同温度下,反应②比反应①的小,主要原因是________________________。
(3)不同温度下反应②中转化率如图2所示。下列叙述正确的是______(填序号)。
a.B点: b.:A点点 c.反应适宜温度:℃
(4)反应③的______(用,表示)。温度升高,反应③的平衡常数______(填“增大”、“减小”或“不变”)。
(5)由粗硅制备多晶硅过程中循环使用的物质除、和外,还有______(填分子式)。
【答案】 (1). (2). (3). 阴极 (4). 或 (5). 1000℃ (6). 导致反应②的小 (7). a、c (8). (9). 减小 (10). 、
【解析】
【分析】I.书写热化学方程式时一定要标注出各物质的状态,要将热化学方程式中焓变的数值与化学计量数对应。本题的反应温度需要标注为条件;
II.(1)惰性电极电解KOH溶液,实质是电解水,产生氢气的必为阴极,发生还原反应。
(2)“看图说话”,将反应①的纵、横坐标对应起来看,即可顺利找到最低温度。影响自由能变的因素主要是焓变和熵变,分析发现熵变对反应②反而不利,说明焓变影响大,为主要影响因素;
(3)据图判断化学平衡的建立和移动是分析的关键。注意时间是一个不变的量。
(4)此问是盖斯定律的简单应用,对热化学方程式直接进行加减即可。
【详解】I.参加反应的物质是固态的Si、气态的HCl,生成的是气态的SiHCl3和氢气,反应条件是300℃,配平后发现SiHCl3的化学计量数恰好是1,由此可顺利写出该条件下的热化学方程式:Si(s)+3HCl(g) SiHCl3(g)+H2(g) ∆H=-225kJ·ml-1;SiHCl3中硅与1个H、3个Cl分别形成共价单键,由此可写出其电子式为:,注意别漏标3个氯原子的孤电子对;
II.(1)电解KOH溶液,阳极发生氧化反应而产生O2、阴极发生还原反应才产生H2;阴极的电极反应式可以直接写成2H++2e-=H2↑,或写成由水得电子也可以:2H2O+2e-=H2↑+2OH-;
(2)由题目所给的图1可以看出,反应①(最上面那条线)当∆G=0时,对应的横坐标温度是1000℃;从反应前后气体分子数的变化来看,反应①的熵变化不大,而反应②中熵是减小的,可见熵变对反应②的自发更不利,而结果反应②的∆G更负,说明显然是焓变产生了较大的影响,即∆H2<∆H1导致反应②的∆G小(两个反应对应的∆H,一个为正值,一个为负值,大小比较很明显);
(3)图2给的是不同温度下的转化率,注意依据控制变量法思想,此时所用的时间一定是相同的,所以图示中A、B、C点反应均正向进行,D点刚好达到平衡,D点到E点才涉及平衡的移动。在到达平衡状态以前,正反应速率大于逆反应速率,a项正确,B点反应正向进行,正反应速率大于逆反应速率;b点错误,温度越高,反应速率越快,所以E点的正(或逆)反应速率均大于A点;c项正确,C到D点,SiHCl3的转化率较高,选择此温度范围比较合适,在实际工业生产中还要综合考虑催化剂的活性温度。
(4)将反应①反向,并与反应②直接相加可得反应③,所以∆H3=∆H2-∆H1,因∆H2<0、∆H1>0,所以∆H3必小于0,即反应③正反应为放热反应,而放热反应的化学平衡常数随着温度的升高而减小;
(5)反应①生成的HCl可用于流程中粗硅提纯的第1步,三个可逆反应中剩余的H2也可循环使用。
【点睛】①对于反应的吉布斯自由能大小比较及变化的分析,要紧紧抓住焓判据和熵判据进行分析。②判断图2中时间是一个不变的量,是看清此图的关键。明白了自变量只有温度,因变量是SiCl4的转化率,才能落实好平衡的相关知识的应用,如平衡的建立,平衡的移动以及平衡常数随温度变化的规律等。
实验现象
离子方程式
A
向氢氧化镁悬浊液中滴加氯化铵溶液,沉淀溶解
B
向沸水中滴加饱和氯化铁溶液得到红褐色液体
C
二氧化硫使酸性高锰酸钾溶液褪色
D
氧化亚铁溶于稀硝酸
A
B
C
D
混合浓硫酸和乙醇
配制一定浓度的溶液
收集气体
证明乙炔可使溴水褪色
2018年天津卷理综化学高考真题及答案解析(原卷+解析卷): 这是一份2018年天津卷理综化学高考真题及答案解析(原卷+解析卷),文件包含精编2018年全国普通高等学校招生统一考试化学天津卷及答案解析doc、精编2018年全国普通高等学校招生统一考试化学天津卷真题原卷doc等2份试卷配套教学资源,其中试卷共19页, 欢迎下载使用。
2018年北京卷理综化学高考真题及答案解析(原卷+解析卷): 这是一份2018年北京卷理综化学高考真题及答案解析(原卷+解析卷),文件包含精编2018年高考北京卷理综化学试题及答案解析doc、精编2018年高考北京卷理综化学试题真题原卷doc等2份试卷配套教学资源,其中试卷共24页, 欢迎下载使用。
2018年全国卷Ⅲ理综化学高考真题及答案解析(原卷+解析卷): 这是一份2018年全国卷Ⅲ理综化学高考真题及答案解析(原卷+解析卷),文件包含精编2018年高考全国卷Ⅲ理综化学试题解析精编版及答案解析doc、精编2018年高考全国卷Ⅲ理综化学试题解析精编版真题原卷doc等2份试卷配套教学资源,其中试卷共21页, 欢迎下载使用。












