

试卷 2020-2021学年浙教版科学中考第一轮复习分类题型训练(四十六):化学填空(6)
展开1.氢气是理想的清洁高能燃料,以水为原料生产氢气的方法有多种。
方法Ⅰ:电解水法,方法Ⅱ:光解水法。
我国科学家已研制出在新型高效光催化剂作用下,利用太阳能分解水制氢气。写出光分解水的化学方程式__________。
水在通过并接触催化剂表面时,分解的微观过程用示意图表示如下:(“○”表示氢原子,“●”表示氧原子,“▁”表示催化剂)。则水分解微观过程的正确顺序是 __________(填数字序号)。
2.有一包白色固体样品,可能由硫酸钠、氢氧化钠、碳酸钙、氯化钡、氯化镁中的一种或几种物质组成,为探究该样品的组成,某小组取适量样品按下列流程进行实验。
(1)滤液中溶质的成分有__________。
(2)若现象①“滤渣全部溶解”变为“滤渣部分溶解”,其他现象不变,则原样品中不能确定是否存在的物质是__________。
3.有一包白色粉末A,由CuSO4、CaCO3、BaCl2、Na2SO4、NaOH中的两种或两种以上的物质混合而成。为探究其组成,进行如下实验:
(1)取白色粉末A,向其中加入足量水,充分搅拌后过滤,得到白色沉淀B和无色滤液C;
(2)向白色沉淀B中加入足量稀盐酸,沉淀有部分溶解,并产生无色气体。
(3)向无色滤液C中通入一定量CO2,无现象。
则:原白色粉末中一定不含__________,白色沉淀B中加入足量稀盐酸反应方程式为__________。
4.已知镉(Cd)的金属活动性与铁、锌相近,镉元素在化合物中常显+2价。
(1)将镉丝插入下列溶液有明显现象的是__________(填序号)。
①NaCl溶液 ②HCl溶液 ③AgNO3溶液 ④NaOH溶液
(2)镍镉电池应用广泛,为了防止污染环境,将废旧镍镉电池中的镉回收的一种方法如下:
步骤 1:将废旧电池破碎成细颗粒后焙烧,将镉转化为氧化镉(CdO);
步骤 2:将含氧化镉的细颗粒和炭粉混合后,隔绝空气加热至1200℃,可得镉蒸气和一氧化碳。
其中使氧化镉变成镉的化学方程式是__________。
5.下列是光亮铁钉的系列变化。请回答问题:
(1)反应②中,光亮铁钉主要与空气中的 __________发生反应。
(2)若反应①和②所用的光亮铁钉质量相同,用ma、mb、mc分别代表光亮铁钉、红色铁钉、无锈铁钉,则它们的质量由大到小的顺序为 __________。
6.分类和对比是科掌学习中重要的思维方法。请回答:
(1)对下列符号进行分类:2N、N2、2Mg2+、SO2、2N2、SO42-,可依据微粒是否带电进行分
类,则带电的微粒是__________。
(2)小金在实验室做了如图所示的“对比实验”,盛装NaOH溶液的软塑料瓶变瘪的程度比盛水的软塑料瓶变瘪程度要大,其原因是:__________(用化学方程式表示)。
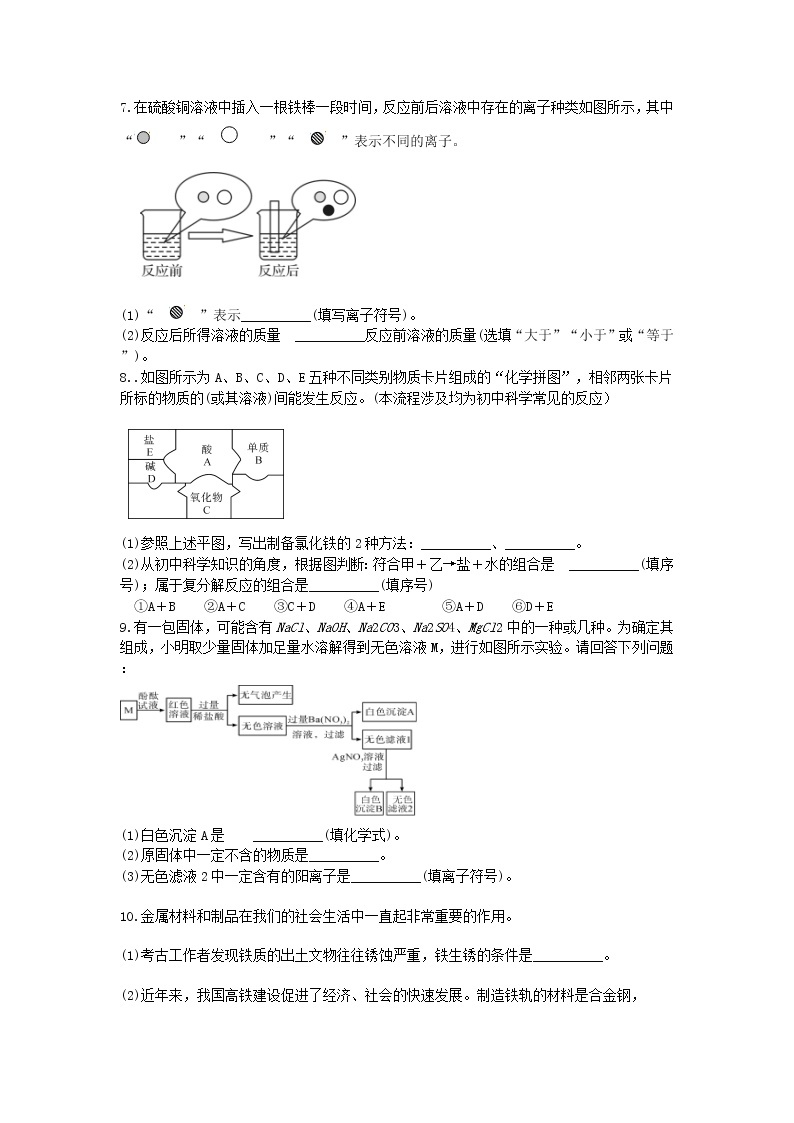
7.在硫酸铜溶液中插入一根铁棒一段时间,反应前后溶液中存在的离子种类如图所示,其中“ ”“ ”“ ”表示不同的离子。
(1)“ ”表示__________(填写离子符号)。
(2)反应后所得溶液的质量 __________反应前溶液的质量(选填“大于”“小于”或“等于”)。
8..如图所示为A、B、C、D、E五种不同类别物质卡片组成的“化学拼图”,相邻两张卡片所标的物质的(或其溶液)间能发生反应。(本流程涉及均为初中科学常见的反应)
(1)参照上述平图,写出制备氯化铁的2种方法:__________、__________。
(2)从初中科学知识的角度,根据图判断:符合甲+乙→盐+水的组合是 __________(填序号);属于复分解反应的组合是__________(填序号)
①A+B ②A+C ③C+D ④A+E ⑤A+D ⑥D+E
9.有一包固体,可能含有NaCl、NaOH、Na2CO3、Na2SO4、MgCl2中的一种或几种。为确定其组成,小明取少量固体加足量水溶解得到无色溶液M,进行如图所示实验。请回答下列问题:
(1)白色沉淀A是 __________(填化学式)。
(2)原固体中一定不含的物质是__________。
(3)无色滤液2中一定含有的阳离子是__________(填离子符号)。
10.金属材料和制品在我们的社会生活中一直起非常重要的作用。
(1)考古工作者发现铁质的出土文物往往锈蚀严重,铁生锈的条件是__________。
(2)近年来,我国高铁建设促进了经济、社会的快速发展。制造铁轨的材料是合金钢,
主要原因是合金钢具有__________的优越性能。
11.为了除去NaCl溶液中含有少量的MgCl2、CaCl2和Na2SO4等杂质,某小组同学选用Na2CO3溶液、稀盐酸、Ba(OH)2溶液三种试剂,按一定的顺序进行如图所示的实验。
回答下列问题:
(1)实验Ⅰ中加入试剂A除去的杂质是__________ ;
(2)滤液②中除Na+和Cl﹣外,还含有的离子是__________(填离子符号);
(3)实验Ⅲ中发生的中和反应的化学方程式是__________。
12.如图所示为甲烷与氧气反应的微观示意图,请通过比较、归纳,回答下列问题:
(1)甲烷、烷气、二氧化碳和水的化学性质不同 其原因是__________;
(2)烷分子、二氧化碳分子、水分子的相同点__________;
(3)根据上述示意图,请从微观角度描述有关化学变化的一个信息__________。
13.如图是同学们依据物质类别和物质中某种元素的化合价构建的初中常见物质间的转化关系坐标图(图中“→”表示物质间的转化),请据图回答下列问题:
(1)工业上可用化合反应来制备B,且反应时放出大量热,B的俗称为__________;
(2)已知金属铝可与E溶液中的溶质和溶剂反应生成偏铝酸钠(NaAlO2)和一种最轻的气体,写出该反应的化学方程式__________;E的固体露置在空气中一段时间后质量会增加,其原因有__________;
(3)H、G均可与F溶液反应,分别生成含该金属元素的两种盐溶液,则G与F溶液反应的化学方程式为__________;
14.下列是初中化学中常见的物质:铁、氢气、氧化铜、二氧化碳、硫酸、氢氧化钠、氯化铜。它们进行击鼓传花游戏,条件是相互之间能发生反应就可以进行传递。请把上述物质分别安排在A~G 的位置上,使花束能从A传到G。其中A 的固本俗称干冰。请回答:
(1)氢氧化钠应放在位置__________上。
(2)C和D反应的化学方程式为__________。上述物质除了发生从A到G的化学反应外,常温下还能相互发生化学反应的是__________(写化学式)。以上化学反应不包括__________基本反应类型。
15.如图所示,A是金属氧化物,B是一种金属单质,C是黄色溶液,D是浅绿色溶液,反应③是物质E与氧气、水发生的一个化合反应,请回答下列问题:
(1)写出试剂甲可能的化学式:__________。
(2)试剂乙中一定含有的离子:__________。
(3)写出化学变化①和②的化学方程式:
① __________。
② __________。
16.用相同质量的铁和锌跟一定量的稀硫酸反应,其反应过程如右图所示(图中横、纵坐标分别表示反应的时间t和产生氢气的质量m)。试回答:
(1)曲线A表示的是__________(填“铁粉”或“锌粉”)跟稀硫酸反应的情况;
(2)从图形可知铁、锌和稀硫酸中一定没有剩余的是__________。
17.小明将未经砂纸打磨的铝条放入盛有足量稀盐酸的密闭容器中,用压强传感器测得容器内气体压强和反应时间的变化曲线如下图所示,请回答下列问题:
(1)AB段发生反应的化学方程式是__________。
(2)CD段压强变化的主要原因是__________。
18.小金通过图示装置验证CO2能与NaOH发生化学反应。推动注射器活塞向充满CO2的集气瓶中注入过量的20%NaOH溶液,振荡集气瓶后打开止水夹。
(1)打开止水夹后观察到的现象是__________。
(2)反应后将集气瓶中混合物过滤,所得溶液中除含有Na2CO3外,还存在的溶质有__________(填名称)。
19.如图为某化学反应的微观示意图,图中“●”表示硫原子,“○”表示氧原子。甲物质的名称是__________;该反应的化学方程式是__________。
参考答案
1.2H2O==2H2↑+O2↑(光照、催化剂) ①④②⑤③
2.(1)NaCl、BaCl2、NaOH (2)MgCl2
3.CuSO4;BaCO3+2HCl=BaCl2+CO2↑+H2O
4.②③;CdO+C=1200℃隔离空气Cd↑+CO↑
5.(1)氧气、水(不写全不得分) (2)mb>ma>mc
6.(1)2Mg2+/(或者Mg2+)、SO42- (2)2NaOH+CO2=Na2CO3+H2O
7.(1)Fe2+ (2)小于
8.(1) 方程式略;方程式略 (2) 235 (3)2456
9.(1)BaSO4 ;(2)Na2CO3、MgCl2 (3)Na+、H+、Ba2+ (4)将上述实验中的过量稀盐酸改成稀硝酸
10.(1)铁同时与氧气和水接触 (2)硬度大
11.(1)MgCl2和Na2SO4 (2)OH﹣、CO32﹣ (3)NaOH+HCl=NaCl+H2O
12.构成物质的分子不同,分子是保持物质化学性质的微粒 都含有氧原子 分子分裂成原子,原子重组构成新分子(合理即可)
13.(1)熟石灰 (2)2Al+2H2O+2NaOH==2NaAlO2+3H2↑;会吸水潮解
14.(1)B(2)Fe+CuCl2=FeCl2+Cu;NaOH和H2SO4;化合反应
15.(1)HCl或H2SO4(2)OH-(3)①Fe2O3+3CO==2Fe+3CO2或Fe2O3+3H2==2Fe+3H2O②Fe+H2SO4=FeSO4+H2↑或Fe+2HCl=FeCl2+H2↑
16.(1)铁粉(2)稀硫酸
17.(1)Al2O3+6HCl=2AlCl3+3H2O (2)气体温度降低
18.(1)CaCl2溶液沿导管进入集气瓶,集气瓶内液体变浑浊 (2)氯化钠,氢氧化钠
19.二氧化硫;2SO2+O2====一定条件2SO3。
试卷 2020-2021学年浙教版科学中考第一轮复习分类题型训练(四十四):化学填空(4): 这是一份试卷 2020-2021学年浙教版科学中考第一轮复习分类题型训练(四十四):化学填空(4),共7页。
试卷 2020-2021学年浙教版科学中考第一轮复习分类题型训练(四十二):化学填空(2): 这是一份试卷 2020-2021学年浙教版科学中考第一轮复习分类题型训练(四十二):化学填空(2),共10页。
试卷 2020-2021学年浙教版科学中考第一轮复习分类题型训练(四十一):化学填空(1): 这是一份试卷 2020-2021学年浙教版科学中考第一轮复习分类题型训练(四十一):化学填空(1),共9页。试卷主要包含了请仔细观察如图,右图是某反应的微观示意图,根据下表回答问题等内容,欢迎下载使用。












