





高中化学人教版 (2019)必修 第一册第二节 离子反应优质课ppt课件
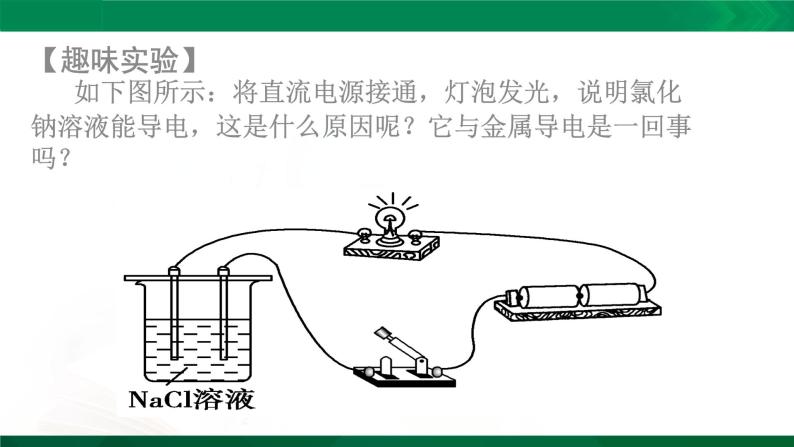
展开【趣味实验】 如下图所示:将直流电源接通,灯泡发光,说明氯化钠溶液能导电,这是什么原因呢?它与金属导电是一回事吗?
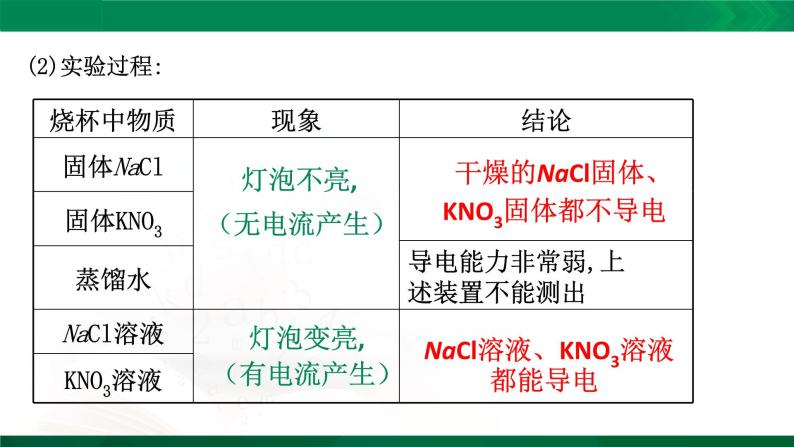
NaCl溶液、KNO3溶液
金属导电:有自由移动的电子。
【氯化钠在水溶液里导电】
3.电解质溶液导电的原因:电解质溶液中含有________________________。
理解概念时注意(做笔记)
①电解质、非电解质都是化合物; 单质和混合物(如溶液)既不属于电解质,又不属于非电解质②电解质导电有条件(水溶液或熔融状态)③ 电解质应是本身导电,而不是发生了化学反应后生成的物质导电(如SO2、CO2、NH3等)
1.讨论分析下列物质哪些是电解质?哪些是非电解质?
①金属铜 ②固态NaCl ③O2 ④H2SO4⑤碳棒 ⑥酒精水溶液 ⑦KOH水溶液⑧熔融状态的KNO3 ⑨葡萄糖 ⑩ 氨气
【思考交流】
1.铜丝、盐酸能导电,它们是电解质还是非电解质?
小结1:电解质和非电解质都是化合物
既不是电解质也不是非电解质
判断下列说法是否正确,并说明理由?
3.纯硫酸在熔融状态下不导电,所以硫酸不是电解质,这种说法正确吗?
小结2:电解质导电的条件是在水溶液力或熔融状态下,两个条件具备一个即可。
2.BaSO4、AgCl、CaCO3均难溶于水,它们是电解质吗?
难溶盐在熔融状态时可导电
4.SO2溶于水形成的溶液以及Na2O熔融状态下都能导电,这两种氧化物都是电解质吗?
小结3:在水溶液里或熔融状态下,本身直接电离出自由移动离子的化合物才是电解质。
5.NaCl晶体,液态HCl都不导电,所以它们不是电解质?
小结4:电解质导电是有条件的。 电解质并不一定能导电; 能导电的物质也不一定是电解质。
NaCl晶体,液态HCl在水溶液里都导电
【提示】电解质和非电解质判断方法
(1)看物质是否是化合物。
(2)看该物质在水溶液里或熔融状态下能否导电。
(3)看是否是物质本身电离而导电。
【电解质和非电解质的比较】
水溶液或熔融状态能导电
水溶液和熔融状态都不能导电
水溶液里或熔融状态下自身能发生电离
水溶液里和熔融状态下自身不能发生电离
酸:H2SO4、H2CO3碱:NaOH、NH3·H2O盐:NaCl、CaCO3④金属氧化物:Na2O、CaO、MgO⑤水
非金属氧化物:SO2、SO3、CO2、CO、P2O5非酸性气态氢化物:NH3部分有机物:蔗糖、酒精、CH4
用化学符号表示电离过程的式子。
②等号右边离子所带的电荷总数为0。
①等号两边各元素的原子个数要相等。
写出以下物质的电离方程式:
HNO3 H2SO4
NaOH Ca(OH)2
CuSO4 NH4Cl NaHCO3
书写电离方程式必须以事实为依据,不能臆造。 如NaHCO3溶液的电离方程式为:NaHCO3=Na++HCO3- NaHSO4溶液的电离方程式为:NaHSO4=Na++H++SO42-,
BaSO4,CaCO3等难溶于水的盐是否是强电解质?
是,因为溶于水的部分完全电离!
强电解质溶液的导电能力一定强于弱电解质溶液的导电能力?
导电能力主要要看溶液中自由移动离子的浓度大小和离子所带电荷的多少。
酸、碱、盐在水中的电离
“左”化学式, “右”离子符号
1、下列物质属于电解质的是( ) A.HCl B.CO2 C.盐酸 D.铜丝
2、下列物质的水溶液可以导电,但不属于电解质的是( ) A.NaOH B.CO2 C.NaCl D.CuSO4
3.下列物质中,导电性能最差的是( ) A.熔融的氢氧化钠 B.石墨棒 C.盐酸溶液 D.固态氯化钾
4、下列物质能导电,又是强电解质的是( ) A.熔融的NaOH B.液态HCl C.NaCl晶体 D.NH3·H2O
5、把0.05mlNaOH晶体分别加入到下列100mL液体中,溶液导电性变化较大的是( ) A.自来水 B.0.5ml/L盐酸 C.0.5ml/LH2SO4 D.0.5ml/LNaNO3
6.下列说法正确的是( )A.电离时生成的阳离子全部是氢离子的化合物叫做酸B.只有酸电离时,阳离子才是氢离子C.电离时生成的阴离子全部是氢氧根离子的化合物叫做碱D.所有的盐电离时都生成金属离子和酸根离子
7.某化学兴趣小组进行化学实验,按照图Ⅰ连接好线路发现灯泡不亮,按照图Ⅱ连接好线路发现灯泡亮,由此得出的结论正确的是( ) A.MgCl2是非电解质 B.MgCl2溶液是电解质 C.MgCl2在水溶液中电离出了可以自由移动的离子 D.MgCl2只有在溶液中才能导电
8.下列电离方程式中正确的是( ) A.BaCl2=Ba2++Cl- B.Al2(SO4)3=2Al3++3SO42- C.AlCl3=Al+3+3Cl- D.Ca(OH)2=Ca2++(OH)2-
必修 第一册第二节 离子反应课前预习课件ppt: 这是一份必修 第一册<a href="/hx/tb_c161973_t3/?tag_id=26" target="_blank">第二节 离子反应课前预习课件ppt</a>,共32页。PPT课件主要包含了考纲要求,电解质,电解质和非电解质,不一定,水溶液,熔融状态,电解质的电离等内容,欢迎下载使用。
人教版 (2019)必修 第一册第二节 离子反应备课ppt课件: 这是一份人教版 (2019)必修 第一册第二节 离子反应备课ppt课件,文件包含121电解质的电离分层作业解析版-上好课2022-2023学年高一化学同步备课系列人教版2019必修第一册docx、121电解质的电离分层作业原卷版-上好课2022-2023学年高一化学同步备课系列人教版2019必修第一册docx、121电解质的电离课件高一化学同步备课系列人教版2019必修第一册pptx等3份课件配套教学资源,其中PPT共0页, 欢迎下载使用。
化学必修 第一册第二节 离子反应课文配套课件ppt: 这是一份化学必修 第一册第二节 离子反应课文配套课件ppt,共21页。PPT课件主要包含了电解质和非电解质,归纳总结,电离方程式书写,练习+合作交流,从电离角度理解酸碱盐,酸的电离,碱的电离,盐的电离等内容,欢迎下载使用。













