




人教版 (2019)必修 第一册第二节 离子反应一等奖课件ppt
展开1.在学习电离和电离方程式的基础上,教材通过实验1-3的现象和分析,得出Na2SO4稀溶液与BaCl2稀溶液反应的微观实质,从而引出离子反应和离子方程式,并介绍离子方程式的书写步骤。然后,教材以"思考与讨论"的形式,得出中和反应的实质,引导学生深入认识离子反应。最后,教材说明酸、碱、盐在水溶液中发生复分解反应的微观实质,并总结这类离子反应发生的条件等。2.本节内容的特点是概念多、抽象,理论性强。在呈现方式上,教材一方面紧密结合实验引人概念,充分发挥实验在化学概念形成中的重要功能,如现象直观、易懂,有利于激发学习兴趣等;另一方面注重基于实验证据(宏观现象)进行分析和推理,逐步引导学生认识物质导电性及电解质在溶液中反应的本质特征(微观实质),建立电离与离子反应的概念模型,体会模型在解释化学现象、揭示现象的本质中所发挥的重要作用,发展化学学科核心素养。
通过分析酸、碱、盐之间的反应事实,认识离子反应,归纳离子反应发生的条件,正确书写这些反应的离子方程式。
“哑泉致哑”、“安乐泉解毒” 三国时期,诸葛亮在七擒孟获的过程中,蜀军由于误饮哑泉水、个个不能言语,生命危在旦夕,巧遇老叟,指点迷津——饮用万安溪安乐泉水、终于转危为安,渡过难关,哑泉水为何能致哑,万安溪安乐泉水又是什么灵丹妙药?
哑泉水中含有较多的硫酸铜,人喝了含铜盐较多的水就会中毒,致哑、呕吐、腹泻、最后虚脱、痉挛致死。而万安溪安乐泉水中含有较多的碱(一般味苦),在人体误食硫酸铜后大量饮用此泉水,其中的碱不仅中和胃酸,然后又会在肠胃中与硫酸铜发生离子反应: Cu2++2OH- = Cu(OH)2↓,致使原来会被人体吸收的可溶性铜盐变成不溶性的Cu(OH)2沉淀而被排出,因此有解毒作用。
思考:离子之间发生反应所需要具备的条件?
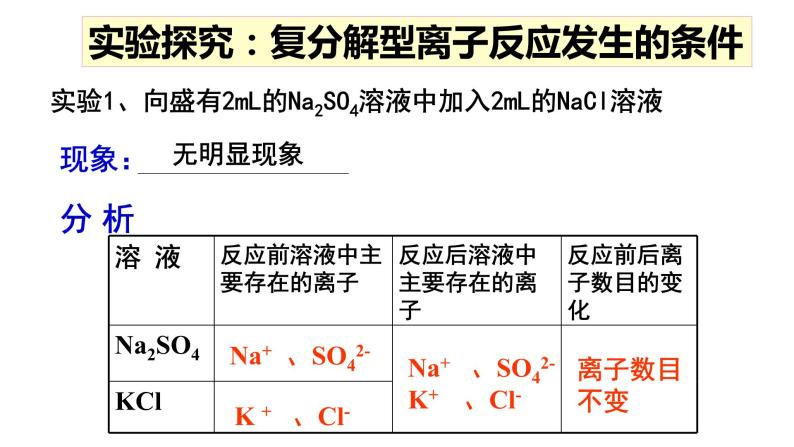
实验探究:复分解型离子反应发生的条件
实验1、向盛有2mL的Na2SO4溶液中加入2mL的NaCl溶液
Na+ 、SO42-
Na+ 、SO42- K+ 、Cl-
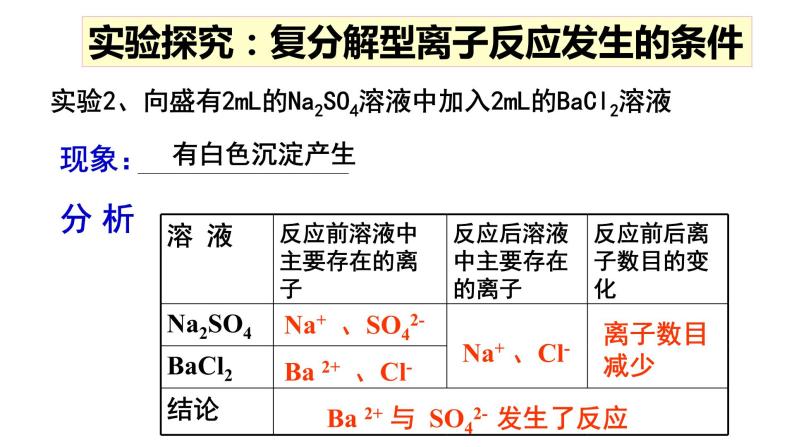
实验2、向盛有2mL的Na2SO4溶液中加入2mL的BaCl2溶液
Ba 2+ 、Cl-
Ba 2+ 与 SO42- 发生了反应
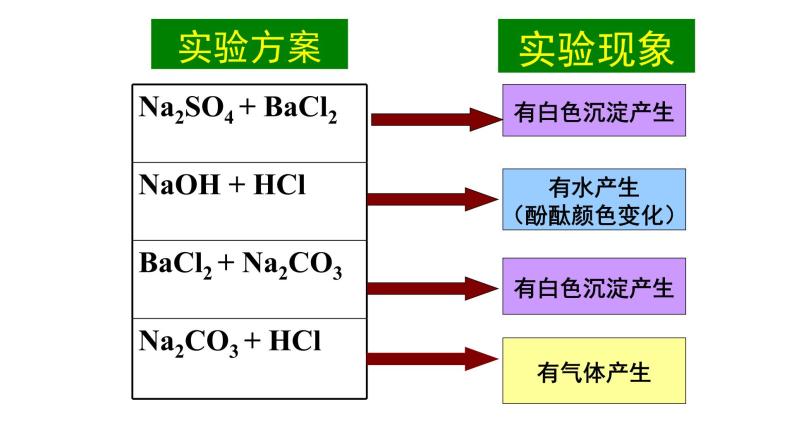
有水产生(酚酞颜色变化)
2.复分解型离子反应发生的条件:
1.电解质在水溶液中的反应其实是离子之间反应
特点:在水溶液中进行(中学阶段)
下列反应不属于离子反应的是( ) A. 实验室用氯酸钾制取氧气 B. 实验室用大理石和稀盐酸制取二氧化碳 C. 实验室用锌粒和稀硫酸制取氢气 D. 工业上用石灰石制取生石灰
电解质在水溶液中的反应
下列能发生离子反应的是( ) A. BaCl 2溶液与 NaOH溶液混合 B. AgNO3溶液与 NaCl溶液混合 C. Na2CO3溶液与Ca(OH)2溶液混合 D. NaCl溶液与 Ca(NO3)2溶液混合
1.定义:用实际参加反应的离子符号表示离子反应的式子。
(1)写:写出化学方程式(符合客观事实)
例:2AgNO3 + CuCl2 == 2AgCl↓+ Cu(NO3)2
(2)拆:把强酸、强碱、可溶性盐写成离子形式,其他物质一律用化学式表示。(注:拆是关键)
2Ag++2NO3-+Cu2++2Cl- == 2AgCl↓+Cu2++2NO3-
(3)删:等量删去方程式两边形式相同的离子:
(4)查:检查方程式并检查两边各元素的原子个数和电荷总数是否相 等(原子守恒和电荷守恒)
Ag+ + Cl- == AgCl↓
2Ag+ + 2Cl- == 2AgCl↓
注:离子方程式除了需要满足原子守恒还需要满足电荷守恒,并且系数也必须为最简整数比
强酸:HCl、HNO3、H2SO4等
强碱:NaOH、KOH、Ba(OH)2、Ca(OH)2等
(1)钾钠铵硝皆可溶;(2)氯盐不溶银、亚汞(AgCl、Hg2Cl2);(3)硫酸盐不溶钡和铅(BaSO4、PbSO4);微溶钙和银(4)碳酸盐、磷酸盐只溶钾钠铵;(碳酸氢盐一般都可溶)(5)碱类可溶钾钠铵钡。
练习3:根据以上书写步骤,请同学们交流讨论填写下表:
有的离子方程式可能出现某一侧所有物质均不能拆分的情况,例如③中所有生成物均不能拆分。
2HCO3- + 2H+ = 2H2O + 2CO2↑
(一定要将方程式的系数化到最简)
化学方程式表示的是一个具体的反应,离子方程式除表示具体反应外,还可以表示一类反应。
练习4:(1)表示可溶性钙盐和可溶性碳酸盐反应的离子方程式为: 。 (2)离子反应Ba2+ + SO42- = BaSO4↓表示的可能是哪类反应?
Ca2+ + CO32- = CaCO3↓
可溶性硫酸盐和可溶性钡盐的反应、硫酸和可溶性钡盐的反应
人教版 (2019)必修 第一册第二节 离子反应课堂教学课件ppt: 这是一份人教版 (2019)必修 第一册第二节 离子反应课堂教学课件ppt,共20页。PPT课件主要包含了实验1-3,离子反应,判断依据,发生的条件,1沉淀,2气体,4氧化还原反应,离子方程式,电解质在溶液中的反应,氢氧化铜溶于盐酸等内容,欢迎下载使用。
高中化学人教版 (2019)必修 第一册第二节 离子反应完美版ppt课件: 这是一份高中化学人教版 (2019)必修 第一册第二节 离子反应完美版ppt课件,共28页。PPT课件主要包含了学习目标,情境思考,实验探究,出现白色沉淀,实验分析,离子反应,Na+Cl-,Na2SO4,BaCl2,Na+等内容,欢迎下载使用。
化学必修 第一册第二节 离子反应课前预习课件ppt: 这是一份化学必修 第一册第二节 离子反应课前预习课件ppt,共31页。PPT课件主要包含了教学分析,学情分析,教学目标,教学重难点,教学过程,第2节离子反应,第2课时离子反应,支持阿伦尼乌斯等内容,欢迎下载使用。













