

江苏省海安高级中学2019-2020学年高一5月月考化学试题
展开高一年级阶段检测
化学(选修)试卷
注意:本试卷分第一部分选择题和第二部分非选择题,共100分,考试时间90分钟。请将答案填
写到答题卡上相应区域。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Al-27
S-32 Cl-35.5 Fe-56 Cu-64
第Ⅰ卷(选择题,共35 分)
一、单项选择题(本题包括10小题,每小题2分,共计20分。每小题只有一个选项符合题意。)
1.化学与生活、生产、环境等密切相关。下列说法错误的是
A.煤的液化、石油的裂化和油脂的皂化都属于化学变化
B.棉、丝、毛、油脂都是天然有机高分子化合物
C.海水淡化的方法主要有蒸馏法、电渗析法、离子交换法等
D.利用太阳能、风能和氢能等能源替代化石能源能有效改善空气质量
2.下列化学用语表达正确的是
A.N2的电子式: B.Cl-离子的结构示意图:
C.CH4分子的比例模型: D.质子数为92、中子数为146的铀(U)原子符号:
3.高温条件下,Al和Fe3O4反应生成Fe和Al2O3。下列说法正确的是
A.该反应过程中的能量变化如图所示
B.该反应条件下,Al的还原性弱于Fe
C.实验室进行该反应时常加入KClO3作催化剂
D.1molFe3O4参与反应转移8×6.02×1023个电子
4.下列有关化学反应速率和化学反应限度的叙述不正确的是[来源:Z_xx_k.Com]
A.Na与水反应时,增加水的质量,能明显增大原反应的化学反应速率
B.制取乙酸乙酯时加入浓硫酸作催化剂并加热,可加快酯化反应的速率
C.实验室制取H2时,常用锌粉代替锌粒或滴加几滴CuSO4溶液可加快反应速率
D.一定条件下进行合成氨反应:N2+3H22NH3,N2不可能完全转化为NH3
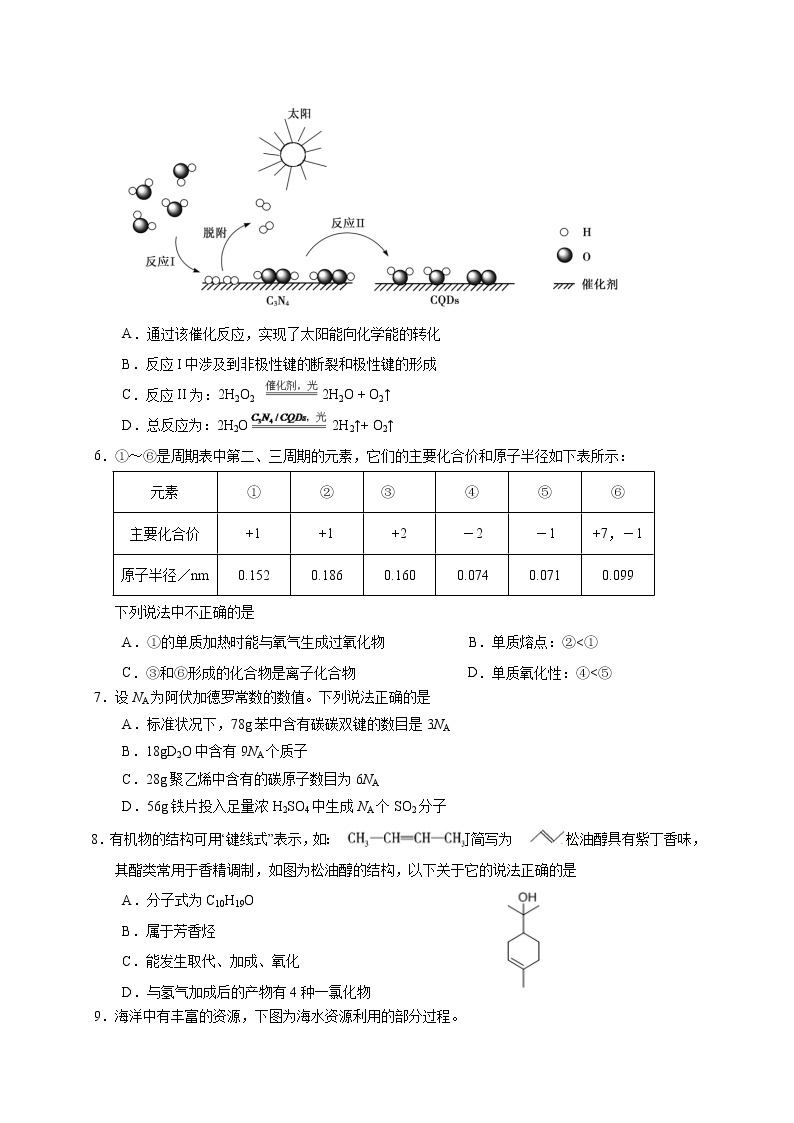
5.中国化学家研究出一种新型复合光催化剂(C3N4/CQDs),能利用太阳光高效分解水,原理如下
图所示。下列说法不正确的是[来源:学#科#网Z#X#X#K]
A.通过该催化反应,实现了太阳能向化学能的转化
B.反应I中涉及到非极性键的断裂和极性键的形成
C.反应II为:2H2O2 2H2O + O2↑
D.总反应为:2H2O 2H2↑+ O2↑
6.①~⑥是周期表中第二、三周期的元素,它们的主要化合价和原子半径如下表所示:
元素 | ① | ② | ③[来源:学科网ZXXK] | ④ | ⑤ | ⑥ |
主要化合价 | +1 | +1 | +2 | -2 | -1 | +7,-1 |
原子半径/nm | 0.152 | 0.186 | 0.160 | 0.074 | 0.071 | 0.099 |
下列说法中不正确的是
A.①的单质加热时能与氧气生成过氧化物 B.单质熔点:②<①
C.③和⑥形成的化合物是离子化合物 D.单质氧化性:④<⑤
7.设NA为阿伏加德罗常数的数值。下列说法正确的是
A.标准状况下,78g苯中含有碳碳双键的数目是3NA
B.18gD2O中含有9NA个质子
C.28g聚乙烯中含有的碳原子数目为6NA
D.56g铁片投入足量浓H2SO4中生成NA个SO2分子
8.有机物的结构可用“键线式”表示,如: 可简写为 。松油醇具有紫丁香味,其酯类常用于香精调制,如图为松油醇的结构,以下关于它的说法正确的是
A.分子式为C10H19O
B.属于芳香烃
C.能发生取代、加成、氧化
D.与氢气加成后的产物有4种一氯化物
9.海洋中有丰富的资源,下图为海水资源利用的部分过程。
下列有关说法正确的是
A.工业上通过电解饱和MgCl2溶液制取金属镁
B.含氮、磷的大量废水排入海洋,易引发赤潮
C.反应④的离子方程式为:Br2+SO2+2H2O=2HBr+2H++ SO42—
D.在第①步中除去粗盐中的SO、Ca2+、Mg2+、Fe3+等杂质,加入药品的顺序为Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
10.控制变量是科学研究的重要方法。不同条件下,用O2氧化一定浓度的FeCl2溶液过程中所测
的实验数据如图所示。下列分析或推测不合理的是
A.Fe2+的氧化率随时间延长而逐渐增大
B.由②和③可知,pH越大,Fe2+氧化速率越快
C.由①和③可知,温度越高,Fe2+氧化速率越快
D.氧化过程的离子方程式为:4Fe2++O2 +4H+ ==4Fe3+ +2H2O
二、不定项选择题(本题包括5小题,每小题3分,共计15分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题得0分;若正确答案包括两个选项,只选一个且正确的得1分,选两个且都正确的得满分,但只要选错一个,该小题就得0分。)
11.翡翠是由X、Y、Z、W四种短周期元素组成的矿物,可表示为XY[Z2W6],X、Y、W元素的简单离子的电子层结构相同,X的原子半径比Y的大,Z的单质是常见的半导体材料,W是地壳中含量最多的元素。下列说法正确的是
A.Y化合物中显+3价
B.X与W只能形成一种化合物
C.W的简单氢化物稳定性比Z的强
D.X的最高价氧化物对应的水化物碱性比Y的弱[来源:学&科&网]
12.下列是乙酸乙酯的制备、分离、提纯、性质验证的实验装置,下列有关说法正确的是
选项 | 功能 | 装置 | 实验的操作或评价 |
A | 制备 | a | 试管中NaHCO3溶液的作用:反应掉挥发的乙酸,溶解乙醇,有利于乙酸乙酯的收集 |
B | 蒸馏 | b | 应把温度计插入液面以下,以便准确测出各馏分的温度 |
C | 分液 | c | 打开分液漏斗的旋塞,让乙酸乙酯缓缓流入烧杯中 |
D | 水解 | d | 碱性条件下水解完全的标志为溶液不再分层 |
13.下列实验操作和现象与结论的关系不相符的是
| 操作和现象 | 结论 |
A | 将一小块钠分别投入盛有水和乙醇的小烧杯中,钠与乙醇反应要平缓得多 | 乙醇羟基中的氢原子不如水分子中的氢原子活泼 |
B | 在催化剂存在的条件下,石蜡油加强热生成的气体通入溴的四氯化碳溶液中,溶液褪色 | 石蜡油的分解产物中含有烯烃 |
C | 向盛有大理石的锥形瓶中滴加稀盐酸,产生无色气体 | 证明Cl的非金属性强于C |
D | 向蔗糖溶液中加入稀硫酸,水浴加热一段时间后,再加入新制Cu(OH)2悬浊液,用酒精灯加热,未见红色沉淀 | 蔗糖未水解 |
14.利用反应6NO2+8NH3=7N2+12H2O设计的电池装置如图所示,该装置既能有效消除氮氧化物
的排放减轻环境污染,又能充分利用化学能。下列说法正确的是
A.电极A上发生氧化反应,电极A为正极
B.电池工作时,OH—从右向左迁移
C.当有0.1molNO2被处理时,外电路中通过电子0.4mol
D.电极B的电极反应式为2NO2+8e—+8H+=N2+4H2O
15.硫酸钙可用生产疏酸、漂白粉等一系列物质。下列说法正确的是
A.由CO与H2合成CH3CH2OH的反应中,原子利用率为100%
B.向蔗糖中加入浓硫酸,蔗糖变黑并产生刺激性气味的气体,说明浓硫酸具有脱水性和强氧化性
C.二氧化硫和漂白粉都能使品红溶液褪色,两者漂白性质相同
D.图中所有反应均为氧化还原反应
第Ⅱ卷(非选择题 共65分)
16.(14分)现有A、B、C、D、E五种元素,它们的质子数依次增多。
①A的核电荷数大于2,可形成氢化物H2A,该氢化物在常温下是液体;
②A和B两元素可形成B2A3化合物,该化合物既能溶于强酸,又能溶于强碱;
③C+离子比B3+离子多8个电子;
④C与D元素可以形成化合物CD;
⑤CD的溶液中通入氯气后加淀粉溶液显蓝色;
⑥在周期表中E处于D的下一个周期,E单质可与冷水反应生成氢气,反应时E的单质与生成的氢气的物质的量之比为2:1。试回答:
(1)A元素在周期表中的位置为 ▲ 、E是 ▲ (填元素名称)。
(2) D的单质分子的结构式 ▲ ,C元素最高价氧化物的水化物的电子式 ▲ 。
(3)写出工业上冶炼B单质的化学方程式 ▲ 。
(4)写出CD的溶液中通入氯气的离子方程式 ▲ 。
(5)比较B、C、E三种元素形成的简单离子氧化性的强弱:(B、C、E离子用实际离子符号表示)氧化性 ▲ 。
17.(13分)CH4既是一种重要的能源,也是一种重要的化工原料。
(1)甲烷高温分解生成氢气和碳。在密闭容器中进行此反应时要通入适量空气使部分甲烷燃烧,其目的是 ▲ 。
(2)以CH4为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图甲所示,则通入a气体的电极名称为 ▲ ,通入b气体的电极反应式为 ▲ 。(质子交换膜只允许H+通过)
(3)在一定温度和催化剂作用下,CH4与CO2可直接转化成乙酸,这是实现“减排”的一种研究方向。
①在不同温度下,催化剂的催化效率与乙酸的生成速率如图乙所示,则该反应的最佳温度应控制在 ▲ 左右。
②该反应催化剂的有效成分为偏铝酸亚铜(CuAlO2,难溶物)。将CuAlO2溶解在稀硝酸中生成两种盐并放出NO气体,其离子方程式为 ▲ 。
(4)CH4还原法是处理NOx气体的一种方法。已知一定条件下CH4与NOx气体反应转化为N2和CO2,若标准状况下8.96L CH4可处理22.4L NOx气体,则x值为 ▲ 。
18.(12分)在某一容积为2L的恒容密闭容器中,A、B、C、D四
种气体物质发生可逆反应,其物质的量n(mol)随时间t(min)的变
化曲线如图所示。回答下列问题:
(1)该反应的化学方程式为 ▲ 。
(2)前2min内用A的浓度变化表示的化学反应速率
为 ▲ ,
4min时,v正(A) ▲ v逆(D) (填“>”“<”或“=”)。
(3)在2min时,图象发生改变的原因可能是 ▲ (填字母)
A.增大B的物质的量 B.降低温度
C.加入催化剂 D.减小A的物质的量
(4)能说明该反应已达到平衡状态的标志是 ▲ (填字母)。
A.消耗5mol B的同时生成4molD
B.反应速率4v(B) = 5v (D)
C.容器内D的浓度不再随时间而发生变化
D.容器内压强不再随时间而发生变化
E.容器内混合气体的密度不再随时间而发生变化
(5)由图示求得平衡时A的转化率为 ▲ 。
19.(16分)以淀粉为主要原料合成一种具有果香味的物质C和化合物D的合成路线如下图所示。
请回答下列问题:
(1)葡萄糖的结构简式为 ▲ ,B分子中的官能团名称为 ▲ 。
(2)反应⑦中物质X的分子式为 ▲ ,反应⑧的类型为 ▲ 。
(3)反应③的化学方程式为 ▲ 。
(4)反应⑤的化学方程式为 ▲ 。反应⑥用于实验室制乙烯,为除去其中可能混有的SO2应选用的试剂是 ▲ 。
(5)已知D的相对分子量为118,其中碳、氢两元素的质量分数分别为40.68%、5.08%,其余为氧元素,则D的分子式为 ▲ 。
(6)检验反应①进行程度,需要的试剂有 ▲ 。
A.新制的Cu(OH)2悬浊液 B.碘水
C.NaOH溶液 D.FeCl3溶液
(7)乙烯的同系物丙烯(CH2=CH-CH3)可以通过加聚反应生成高分子化合物,其结构简式
是 ▲ 。
20.(10分) 海洋是一个巨大的资源宝库。在海洋中生长的海带,富含碘元素。某同学设计以下实验方案,从海带中提取I2。
(1)灼烧海带时,除需酒精灯与三脚架外,还需要用到的实验仪器是 ▲ 。
(2)向滤液中加入双氧水和稀硫酸发生反应的离子方程式是 ▲ 。
(3)试剂a可以是 ▲ (填序号)。
A.酒精 B.四氯化碳
C.裂化汽油 D.苯
(4)I-和IO3-在酸性条件下生成I2的离子方程式是 ▲ 。
(5)上图中,含I2的溶液经3步转化为I2的悬浊液,其目的是 ▲ 。
第二学期阶段检测
高一化学参考答案及评分建议
一、单项选择题(本题包括10小题,每小题2分,共20分)
1.B 2.C 3.D 4.A 5.B 6.A 7.B 8.C 9.B 10.B
二、不定项选择题(本题包括5小题,每小题3分,共15分。对1得1分,有错不得分。)
11.AC 12.D 13.CD 14.BC 15.B
16.(共14分,每空2分)
(1) 第2周期ⅥA族 铯 (2) I—I
(3) 2Al2O3(熔融)4Al+3O2↑
(4)2I-+Cl2 ═ I2+2Cl- Al3+>K+>Cs+
17.(共13分,第(4)问3分,其余每空2分)
(1)提供CH4分解所需的能量
(2)负极 O2+4H++4e-=2H2O
(3)250℃ 3CuAlO2+16H++NO3—=3Cu2++3Al3++8H2O+NO↑
(4)1.6 (3分)
18.(共12分,每空2分)
(1)4A(g)+5B(g)6C(g)+4D(g) (2) 0.1mol/(L•min) =
(3) C (4) CD (5) 32%
19.(共16分,第(1)(2)问每空1分,其余每空2分)
(1)CH2OH(CHOH)4CHO (1分) 羧基(1分)
(2)Br2 (1分) 取代反应(1分)
(3) 2CH3CH2OH + 2O22CH3CHO + 2H2O (2分)
(4) CH3CH2OH+ CH3COOH CH3COOCH2CH3 + H2O (2分)
NaOH溶液(2分)
(5) C4H6O4(2分) (6)ABC (2分) (7) (2分)
20.(共10分,每空2分)
(1)坩埚、泥三角 (2)2I-+ H2O2 + 2H+ = I2 + 2H2O
(3)BD (4)5I-+IO3-+6H+ = 3I2 + 3H2O (5)富集碘元素








