





人教版 (2019)必修 第二册第一节 硫及其化合物教课内容课件ppt
展开第一节 硫及其化合物 第一课时 单质硫
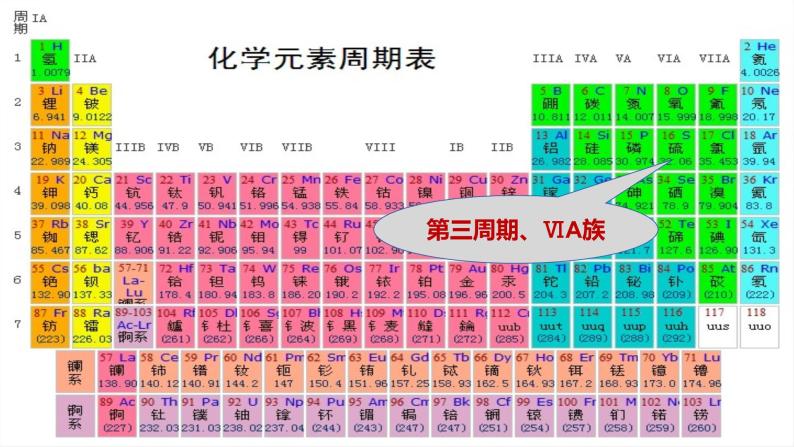
硫是一种重要的非金属元素,位于元素周期表的第三周期,VIA族。
硫原子的最外层有6个电子,在化学反应中容易得到2个电子,形成-2价的硫的化合物。与同主族的氧元素相比,硫元素的原子多一个电子层,得点子的能力相对较弱,而失电子能力则相对较强,硫元素的非金属性比氧元素弱。这也是我们在富含氧气的地表附近找到含硫化合物中,硫常常为+4价或+6价,而氧为-2价的原因。硫元素的原子半径比氯原子半径大,硫原子得电子能力比氯原子弱,硫化氢的稳定性比氯化氢弱。
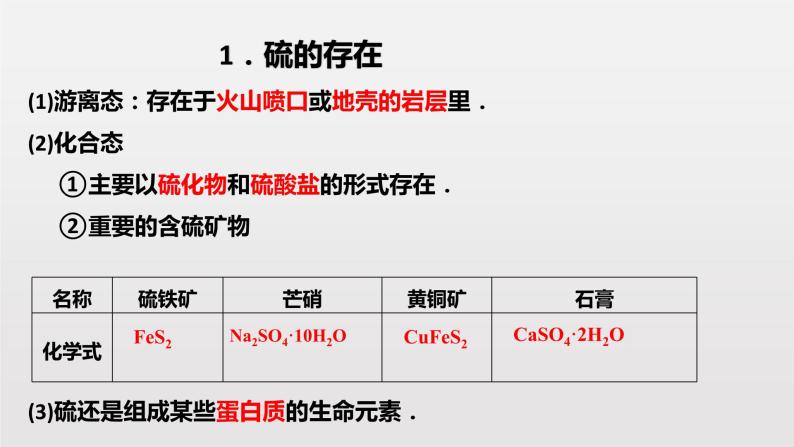
1.硫的存在(1)游离态:存在于火山喷口或地壳的岩层里.(2)化合态①主要以硫化物和硫酸盐的形式存在.②重要的含硫矿物
Na2SO4·10H2O
(3)硫还是组成某些蛋白质的生命元素.
单质硫的图片
印尼东爪哇外南梦,卡瓦伊真火山喷出的气体通过火山口内的喷气孔形成硫磺,当地很多青壮年男子冒险去火山口采硫磺矿谋生。这些硫矿被运到当地工厂加工,在硫化橡胶、漂白糖等工业步骤中使用。
2.物理性质:黄色晶体,俗称硫黄,质脆,易研成粉末。不溶于水,微溶于酒精,易溶于CS2.熔沸点低(112.8℃, 444.6 ℃)密度比水大(约为2 g/cm3 )
试管内壁附着硫怎样洗掉?
提示:用CS2洗涤——硫单质易溶于CS2
BaSO4Na2SO4
+4 +4 SO2、SO32—
-2 -2H2S、 S2—
①与金属反应,能跟大多数金属反应
注意:硫与变价金属反应时,得到低价金属硫化物
Hg +S = HgS (黑色)(常温下反应 ,除汞)
2Ag +S = Ag2S (黑色)(银器变黑)
③ 与强氧化剂反应(如浓硫酸): ________________________________,表现 性。
④ 与碱溶液反应: ________________________________________,表现 。
硫单质的化学性质总结硫的化学性质比较活泼,能与许多金属单质及非金属单质发生化学反应。如:
用于制硫酸、化肥、火柴及杀虫剂等,还用于制造黑火药、烟花爆竹、硫化橡胶等。
单质硫具有一定的杀菌效果
(1) 单质硫燃烧时,产物只能是SO2,无论O2的量是否 充足,均不会生成SO3。 (2) 汞蒸气有毒,实验室里不慎洒落一些汞,可撒上硫粉进行处理(Hg+ S=HgS)。 (3) 实验室中,残留在试管内壁上的硫可用CS2溶解除去,也可用热的NaOH溶液除去。
硫与银、汞的反应及其应用 一般说来,S不能使具有可变化合价的金属显高价,且S与大多数金属的反应需在加热条件下才能完成,但是S与Hg、Ag等不活泼金属的反应在常温下就能进行,且能使Hg显高价。①利用Ag和S的反应可以鉴别出真假银:用一布条沾上少量硫黄粉末在待鉴别的器皿表面用力摩擦,若摩擦处出现黑斑则说明是真银,否则为假银。②利用Hg和S的反应可以消除温度计、气压计、血压计等被打破后汞的毒害,所以若汞不慎洒落在地面上,要立即打开门窗通风,并尽量设法收集起来,残余的部分可覆盖硫粉处理,以免汞蒸气中毒。
1.下列物质中,不能由单质直接化合生成的是( ) ①CuS ②FeS ③SO3 ④H2S ⑤FeCl2 A.①③⑤ B.①②③⑤ C.①②④⑤ D.全部
2.下列关于硫的说法不正确的是( )A.试管内壁附着的硫可用二硫化碳溶解除去B.游离态的硫存在于火山喷口附近或地壳的岩层里C.单质硫既有氧化性,又有还原性D.硫在过量纯氧中的燃烧产物是三氧化硫
解析 硫单质或含硫物质在空气中燃烧时应生成SO2,而不能直接生成SO3。
温馨提示:实验室除去试管内壁附着硫的两种方法:(1)物理法:加二硫化碳(CS2)溶解;(2)化学法:加氢氧化钠溶液溶解。3S+6NaOH 2Na2S+Na2SO3+3H2O 硫既表现氧化性,又表现还原性。
3.下列说法不正确的是( )A.硫是一种难溶于水的黄色固体B.硫与铁反应生成硫化亚铁C.单质硫既有氧化性,又有还原性D.硫在过量纯氧中的燃烧产物是三氧化硫
4.除去试管壁上附着的硫,可采用的方法是( )A.通入氢气后加热B.伸入灼热的铁丝 C.用水洗涤D.用二硫化碳洗涤后再用水洗
解析 硫与氢气反应需要加热,实验操作复杂,且产物硫化氢有毒;硫与铁反应需要加热,其产物硫化亚铁固体会附着在试管壁上;硫难溶于水,微溶于酒精,易溶于二硫化碳,试管壁上的硫可用二硫化碳溶解而除去。
5.根据硫的性质,回答下列问题:(1)单质间发生化合反应,能否生成Fe2S3或CuS?
提示 不能。单质硫与变价金属铁或铜化合只能生成FeS或Cu2S。
(2)铁与硫反应生成FeS,与氯气反应生成FeCl3,能否说明氯气的氧化性比硫强?提示 能。氯气将铁氧化为+3价,而硫只能将铁氧化为+2价。
人教版 (2019)必修 第二册第一节 硫及其化合物背景图课件ppt: 这是一份人教版 (2019)必修 第二册第一节 硫及其化合物背景图课件ppt,共16页。PPT课件主要包含了还原性,课堂巩固,二氧化硫,知识拓展,SO2,可逆反应,生成物,反应物,同一条件,正反应等内容,欢迎下载使用。
高中化学人教版 (2019)必修 第二册第一节 硫及其化合物集体备课ppt课件: 这是一份高中化学人教版 (2019)必修 第二册第一节 硫及其化合物集体备课ppt课件,共34页。PPT课件主要包含了化合态硫,硫的晶体等内容,欢迎下载使用。
高中化学人教版 (2019)必修 第二册第一节 硫及其化合物教案配套课件ppt: 这是一份高中化学人教版 (2019)必修 第二册第一节 硫及其化合物教案配套课件ppt,共28页。PPT课件主要包含了5硫酸的用途,硫的转化等内容,欢迎下载使用。













