






第26讲 化学平衡常数及转化率 反应方向及调控(课件)-2024年高考化学一轮复习(新教材新高考)
展开1、全面、系统复习回顾基本知识。了解知识规律的来龙去脉,透彻理解概念的内涵外延,让学生经历教材由薄变厚的过程。要正确理解基础,不是会做几个简单题就叫基础扎实。对于一轮复习,基础就是像盖房子一样,需要着力做好两件大事:一是夯实地基,二是打好框架。2、扎实训练学科基本技能、理解感悟学科基本方法。一轮复习,要以教材为本,全面细致的回顾课本知识,让学生树立“教材是最好的复习资料”的观点,先引导学生对教材中所涉及的每个知识点进行重新梳理,对教材中的概念、定理、定律进一步强化理解。3、培养学生积极的学习态度、良好的复习习惯和运用科学思维方法、分析解决问题的能力。落实解题的三重境界:一是“解”,解决问题。二是“思”,总结解题经验和方法。三是“归”,回归到高考能力要求上去。解题上强化学生落实三个字:慢(审题),快(书写),全(要点全面,答题步骤规范)。 4、有计划、有步骤、有措施地指导学生补齐短板。高三复习要突出重点,切忌主次不分,无的放矢。要在“精讲”上下足功夫。抓住学情,讲难点、重点、易混点、薄弱点;讲思路、技巧、规范;讲到关键处,讲到点子上,讲到学生心里去。
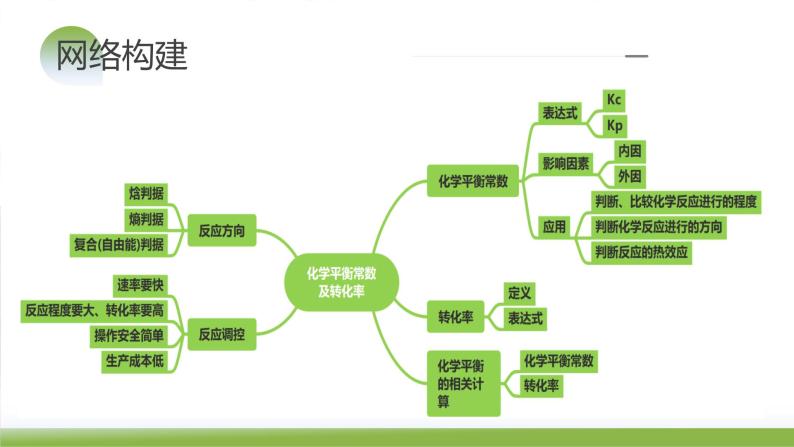
第26讲 化学平衡常数及转化率反应方向及调控
知识梳理 题型归纳
考点要求考题统计考情分析物质的组成、性质、分类2023**卷**题,**分2022**卷**题,**分2021**卷**题,**分……传统文化中的性质与变化2023**卷**题,**分2022**卷**题,**分2021**卷**题,**分
在一定温度下,当一个可逆反应达到化学平衡时,生成物浓度幂之积与反应物浓度幂之积的比值是一个常数,用符号K表示。
知识点1 化学平衡常数
【易错提醒】①固体和纯液体的浓度视为常数,通常不计入平衡常数表达式中,但水蒸气要写入。②计算时,代入平衡常数表达式的浓度是平衡浓度。
a.分压定律:混合气体的总压等于相同温度下各组分气体的分压之和。p(A)+p(B)+p(C)+p(D)+……=p
(3)化学平衡常数与化学方程式书写形式的关系
①正、逆反应的平衡常数互为倒数。
②若化学方程式中各物质的化学计量数都扩大或缩小至原来的n倍,则化学平衡常数变为原来的n次幂或次幂。
③两方程式相加得到新的化学方程式,其化学平衡常数是两反应平衡常数的乘积。
④关于H2O的浓度问题a.稀水溶液中进行的反应,虽然H2O参与反应,但是H2O只作为溶剂,不能代入平衡常数表达式。b.H2O的状态不是液态而是气态时,则需要代入平衡常数表达式。
⑤代入平衡常数表达式的是平衡浓度,而不是任意时刻的浓度,更不能将物质的量代入。
⑥同一化学反应,可以用不同的化学方程式表示,每个化学方程式都有自己的平衡常数表达式及相应的平衡常数。因此,要注意使用与化学方程式相对应的平衡常数。
(1)K值越大,反应物的转化率越大,正反应进行的程度越大,当K>105时,反应可接近完全。
(2)对于同反应,K只受温度影响,与反应物或生成物的浓度变化无关,与压强变化、是否使用催化剂无关,温度升高,ΔH<0,K值减小,ΔH>0,K值增大。
(3)对于不同的反应,K除受温度影响外,还与反应物本身的性质有关。
4.速率常数与平衡常数的关系
①反应速率常数通过量化化学反应速率,来表示反应的快慢;其影响因素包括温度和反应物性质等。
②平衡常数属于平衡程度的标志,表示反应进行的最大限度;平衡常数只受温度的影响,而与反应物的浓度无关。
知识点2 化学平衡常数的应用
一般来说,一定温度下的一个具体的可逆反应:
1.判断、比较可逆反应进行的程度
【特别提醒】K值大小与反应程度的关系
2.判断正在进行的可逆反应是否达到平衡或反应进行的方向
3.判断可逆反应的热效应
4.计算平衡体系中的相关量
根据相同温度下,同一反应的平衡常数不变,计算反应物或生成物的浓度、转化率等。
(2)固体和纯液体的浓度视为恒定常数,不出现在平衡常数表达式中。
(1)计算平衡常数利用的是物质的平衡浓度,而不是任意时刻浓度,也不能用物质的量。
(3)催化剂能加快化学反应速率,但对化学平衡无影响,也不会改变平衡常数的大小。
(4)一般K>105时,认为该反应基本进行完全;K<10-5时,一般认为该反应很难进行;而K在10-5~105反应被认为是典型的可逆反应。
考向1 考查化学平衡常数的含义
考向2 考查化学平衡常数的应用
“三段式”法是有效解答化学平衡计算题的“万能钥匙”。解题时,要注意清楚条理地列出起始量、转化量、平衡量,按题目要求进行计算,同时还要注意单位的统一。
1.分析三个量:起始量、变化量、平衡量。
知识点1 三段式计算模式
(1)对于同一反应物,起始量-变化量=平衡量。
(2)对于同一生成物,起始量+变化量=平衡量。
(3)各转化量之比等于各反应物的化学计量数之比。
3.计算方法:三段式法
1.化学平衡常数的计算
(1)根据化学平衡常数表达式计算
知识点2 有关化学平衡计算方法和技巧
①同一可逆反应中,K正·K逆=1。
③几个可逆反应方程式相加,得总方程式,则总反应的平衡常数等于各分步反应平衡常数之积。
④水溶液中进行的反应,必须拆成离子方程式再计算平衡常数。
(2)依据化学方程式计算平衡常数
4.压强平衡常数的计算技巧
第二步,计算各气体组分的物质的量分数或体积分数;
第四步,根据平衡常数计算公式代入计算。
第一步,根据“三段式”法计算平衡体系中各物质的物质的量或物质的量浓度;
第三步,根据分压计算公式求出各气体物质的分压,某气体的分压=气体总压强×该气体的体积分数(或物质的量分数);
(2)计算Kp的答题模板
5.转化率大小变化分析技巧
判断反应物转化率的变化时,不要把平衡正向移动与反应物转化率提高等同起来,要视具体情况而定。常见有以下几种情形:
考向1 考查平衡常数的计算
考向2 考查转化率的计算
(1)含义:在一定条件下,不需要借助外力作用就能自动进行的过程。
知识点1 化学反应的方向
①体系趋向于从高能状态转变为低能状态(体系对外部做功或释放热量)。
②在密闭条件下,体系有从有序转变为无序的倾向性(无序体系更加稳定)。
在一定条件下无需外界帮助就能自发进行的反应称为自发反应。
3.判断化学反应方向的依据
研究表明,对于化学反应而言,绝大多数放热反应都能自发进行,且反应放出的热量越多,体系能量降低得也越多,反应越完全。可见,反应的焓变是制约化学反应能否自发进行的因素之一。
①研究表明,除了热效应外,决定化学反应能否自发进行的另一个因素是体系的混乱度。大多数自发反应有趋向于体系混乱度增大的倾向。
a.熵的含义:熵是衡量一个体系混乱度的物理量,用符号S表示。
同一条件下,不同物质有不同的熵值,同一物质在不同状态下熵值也不同,一般规律是S(g)>S(l)>S(s)。
b.熵变的含义:熵变是反应前后体系熵的变化,用ΔS表示,化学反应的ΔS越大,越有利于反应自发进行。
(3)综合判断反应方向的依据
①ΔH-TΔS<0,反应能自发进行。
②ΔH-TΔS=0,反应达到平衡状态。
③ΔH-TΔS>0,反应不能自发进行。
(1)促进有利的化学反应:通过控制反应条件,可以加快化学反应速率,提高反应物的转化率,从而促进有利的化学反应进行。
知识点2 化学反应的调控
1.控制反应条件的目的
(2)抑制有害的化学反应:通过控制反应条件,也可以减缓化学反应速率,减少甚至消除有害物质的产生或控制副反应的发生,从而抑制有害的化学反应继续进行。
2.控制反应条件的基本措施
(1)控制化学反应速率的措施
通过改变反应体系的温度、溶液的浓度、气体的压强(或浓度)、固体的表面积以及使用催化剂等途径调控反应速率。
(2)提高转化率的措施
通过改变可逆反应体系的温度、溶液的浓度、气体的压强(或浓度)等改变可逆反应的限度,从而提高转化率。
(2)反应特点:①反应为可逆反应;②正反应是气体体积减小的反应;③ΔH<0。
3.工业合成氨的条件选择
(3)从反应快慢和反应限度两个角度选择反应条件
(4)综合考虑——选择适宜的生产条件
②压强:10~30 MPa
①温度:400~500℃
⑤采用循环操作提高原料利用率
考向1 考查化学反应方向的判定
考向2 考查化学反应的调控
【变式训练】(2023·上海徐汇·统考一模)不符合硫酸工业生产实际的是A.沸腾炉中加入碾碎的硫铁矿B.接触室中的反应条件为高温高压C.催化氧化时通过热交换器充分利用能量D.吸收塔中用98.3%的浓硫酸吸收SO3
第49讲 化学反应的方向与调控-【精梳精讲】2024年高考化学大一轮精品复习课件(新教材): 这是一份第49讲 化学反应的方向与调控-【精梳精讲】2024年高考化学大一轮精品复习课件(新教材),共34页。PPT课件主要包含了复习目标,内容索引,真题演练明确考向,专项突破,归纳整合,自发过程,⑤食盐溶解于水,①镁条燃烧,②酸碱中和,常温下自发等内容,欢迎下载使用。
第49讲 化学反应的方向与调控-2024年高考化学一轮复习高频考点精讲(新教材新高考)课件PPT: 这是一份第49讲 化学反应的方向与调控-2024年高考化学一轮复习高频考点精讲(新教材新高考)课件PPT,共38页。PPT课件主要包含了高考化学一轮复习策略,复习目标,化学反应的方向,考点一,易错辨析,考点二,真题演练等内容,欢迎下载使用。
2024年高考化学一轮复习(新高考版) 第8章 第49讲 化学反应的方向与调控: 这是一份2024年高考化学一轮复习(新高考版) 第8章 第49讲 化学反应的方向与调控,文件包含2024年高考化学一轮复习新高考版第8章第49讲化学反应的方向与调控pptx、2024年高考化学一轮复习新高考版第8章第49讲化学反应的方向与调控docx、第8章第49讲化学反应的方向与调控docx、第8章第49练化学反应的方向与调控docx等4份课件配套教学资源,其中PPT共60页, 欢迎下载使用。












