


第46讲 物质制备综合实验探究-【高效备考】2024年高考化学一轮复习讲义+分层练习
展开1.掌握物质制备型实验方案设计的原则。
2.掌握解答物质制备型实验综合题的思维模型。
必备知识
考点一 无机物的制备
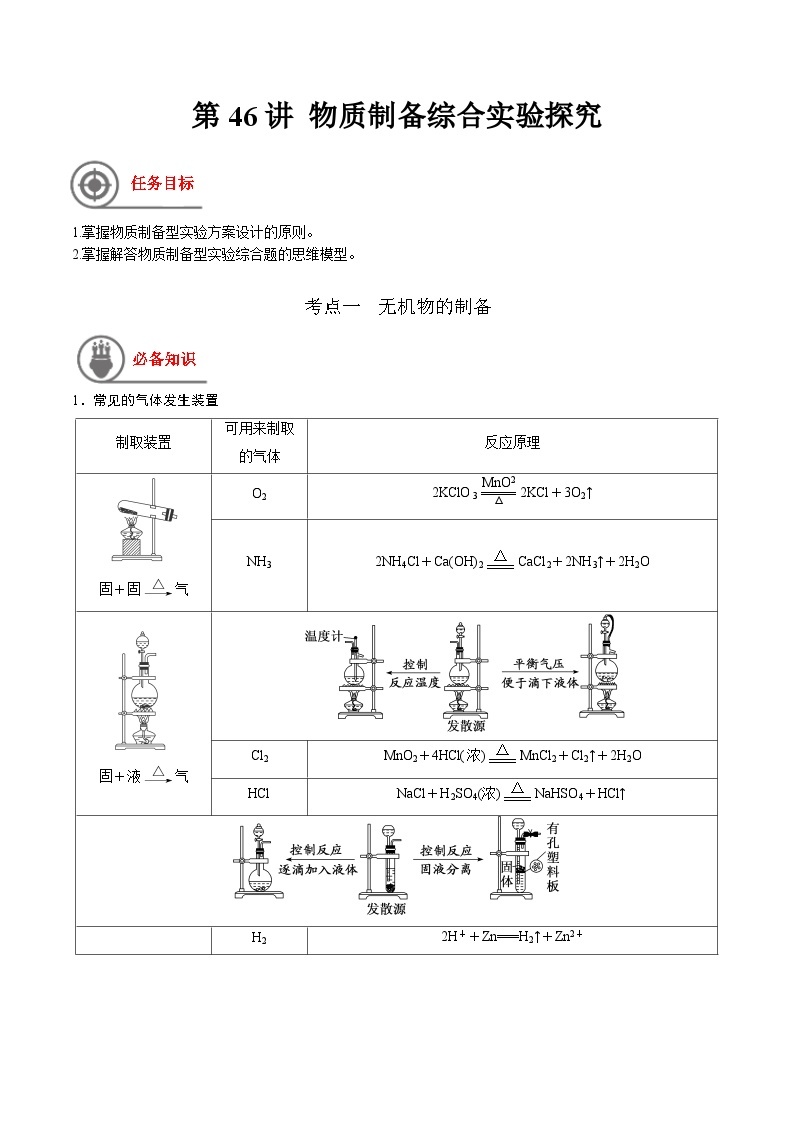
1.常见的气体发生装置
2.气体的净化
(1)设计原则:根据主要气体及杂质气体的性质差异来选择除杂试剂及除杂装置。
(2)吸收剂的选择
吸收剂的选择应根据被提纯气体的性质和杂质的性质来确定,一般情况如下:
①易溶于水的气体杂质可用水吸收;
②酸性杂质可用碱性物质吸收;
③碱性杂质可用酸性物质吸收;
④水为杂质时,可用干燥剂吸收;
⑤能与杂质发生反应生成沉淀(或可溶物)的物质也可作为吸收剂。
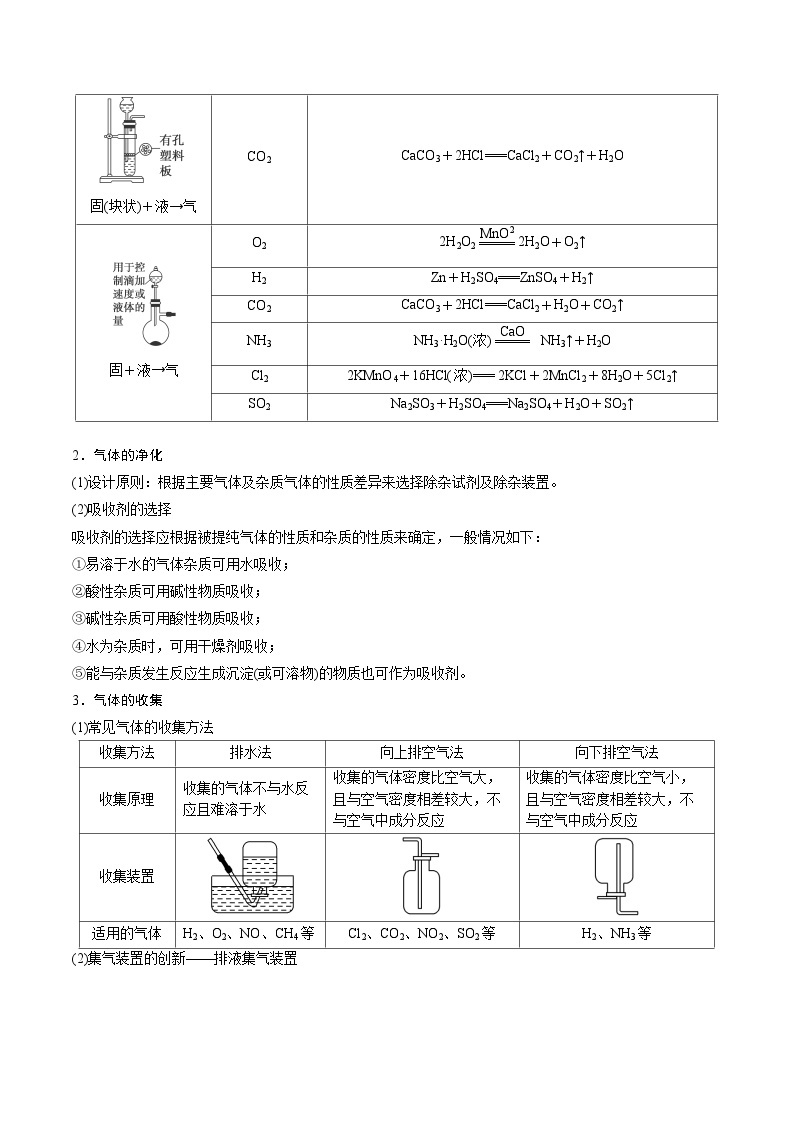
3.气体的收集
(1)常见气体的收集方法
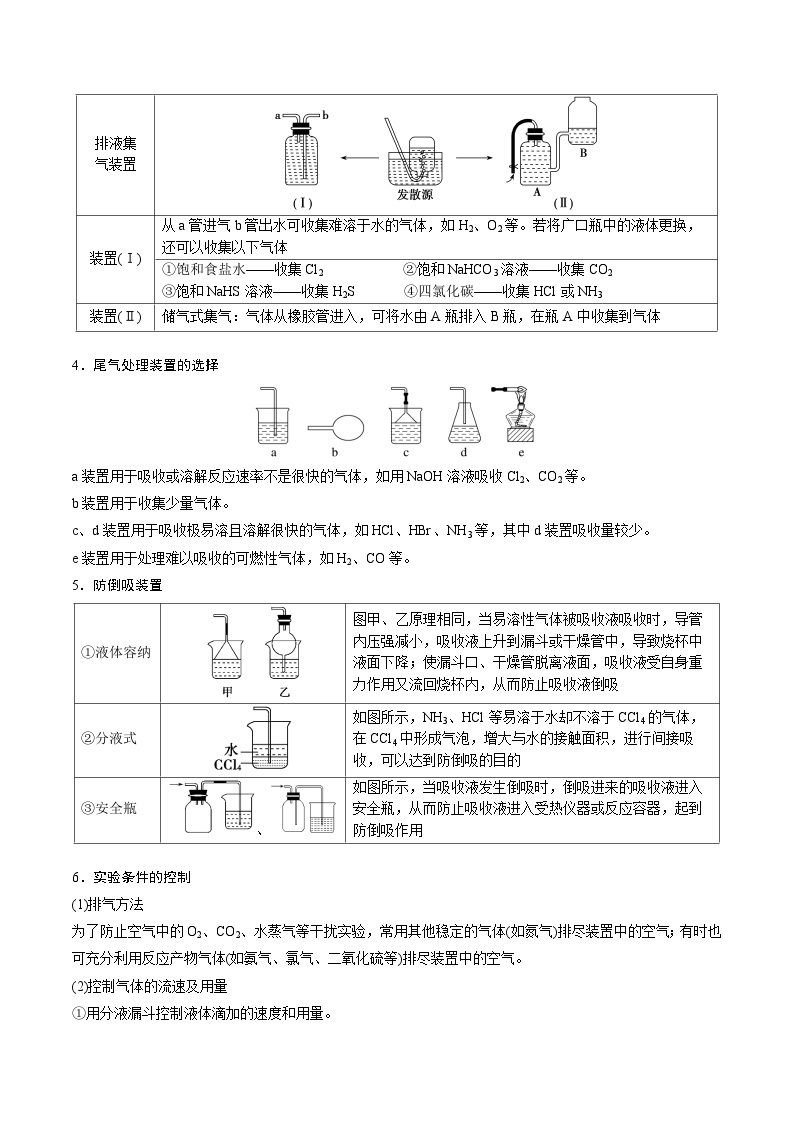
(2)集气装置的创新——排液集气装置
4.尾气处理装置的选择
a装置用于吸收或溶解反应速率不是很快的气体,如用NaOH溶液吸收Cl2、CO2等。
b装置用于收集少量气体。
c、d装置用于吸收极易溶且溶解很快的气体,如HCl、HBr、NH3等,其中d装置吸收量较少。
e装置用于处理难以吸收的可燃性气体,如H2、CO等。
5.防倒吸装置
6.实验条件的控制
(1)排气方法
为了防止空气中的O2、CO2、水蒸气等干扰实验,常用其他稳定的气体(如氮气)排尽装置中的空气;有时也可充分利用反应产物气体(如氨气、氯气、二氧化硫等)排尽装置中的空气。
(2)控制气体的流速及用量
①用分液漏斗控制液体滴加的速度和用量。
②观察气泡,控制气流速度,如图甲,可通过观察气泡得到N2、H2的体积比约为1∶3的混合气体。
③平衡气压,如图乙,用长玻璃管平衡气压,防堵塞。
(3)压送液体
根据装置的密封性,让反应生成气体或消耗气体,产生压强差,将液体压入或倒流入另一反应容器。
(4)温度控制
①控制低温的目的:减少某些反应物或产物分解,如H2O2、NH4HCO3等;减少某些反应物或产物挥发,如盐酸、氨水等;防止某些物质水解,避免副反应发生等。
②采取加热的目的:加快反应速率或使平衡移动,加速溶解等。
③常考的温度控制方式
a.水浴加热:均匀加热,反应温度在100 ℃以下。
b.油浴加热:均匀加热,反应温度在100~260 ℃之间。
c.冰水冷却:使某物质液化、降低产物的溶解度;减少其他副反应,提高产品纯度等。
d.保温:如真空双层玻璃容器等。
7. 无机物制备实验题的解题模型
要点突破
1.碳酸镧[La2(CO3)3]可用于治疗高磷酸盐血症。某化学小组用如图装置模拟制备碳酸镧,反应为2LaCl3+6NH4HCO3===La2(CO3)3↓+6NH4Cl+3CO2↑+3H2O。下列说法正确的是( )
A.从左向右接口的连接顺序:F→B,A→D,E←C
B.装置X中盛放的试剂为饱和Na2CO3溶液
C.实验开始时应先打开W中分液漏斗的旋转活塞
D.装置Z中用干燥管的主要目的是增大接触面积,加快气体溶解
【答案】A。
【解析】氨气极易溶于水,则采用防倒吸装置,E←C;制取的二氧化碳需除去HCl杂质,则F→B,A→D,A正确;装置X的作用为除去HCl杂质,盛放的试剂为饱和NaHCO3溶液,B错误;实验开始时应先打开Y中分液漏斗的旋转活塞,使溶液呈碱性,吸收更多的二氧化碳,C错误;装置Z中用干燥管的主要目的是防止氨气溶于水时发生倒吸,D错误。
2.利用废蚀刻液(含FeCl2、CuCl2及FeCl3)制备碱性蚀刻液[Cu(NH3)4Cl2溶液和FeCl3·6H2O的主要步骤:用H2O2氧化废蚀刻液,制备氨气,制备碱性蚀刻液[CuCl2+4NH3===Cu(NH3)4Cl2]、固液分离,用盐酸溶解沉淀并制备FeCl3·6H2O。下列有关实验说法正确的是( )
A.用H2O2氧化废蚀刻液的离子方程式为:2H++2Fe2++H2O2===2Fe3++2H2O
B.用装置甲可以制备Cu(NH3)4Cl2并沉铁
C.用装置乙可以分离Cu(NH3)4Cl2溶液和Fe(OH)3
D.用装置丁由FeCl3溶液制备FeCl3·6H2O需要经蒸发浓缩、冷却结晶、过滤洗涤等步骤
【答案】A。
【解析】A.H2O2具有强的氧化性,可用H2O2氧化废蚀刻液中的Fe2+,反应的离子方程式为:2H++2Fe2++H2O2===2Fe3++2H2O,A正确;B.氨气易溶于水,注意防止倒吸,所以要选用乙装置,氨气与溶液反应生成Cu (NH3)4Cl2和氢氧化铁,B错误;C.用装置丙可以分离可溶性Cu(NH3)4Cl2溶液和难溶性的固态Fe(OH)3,C错误;D.由FeCl3溶液制备FeCl3·6H2O需要在蒸发皿中蒸干,不能在烧杯中进行,D错误;故合理选项是A。
3.某化学小组同学利用一定浓度的H2O2溶液制备O2,再用O2氧化C2H5OH,并检验氧化产物。
Ⅰ.制备O2
该小组同学设计了如下气体发生装置(夹持装置省略)
(1)甲装置中主要仪器的名称为___________。
(2)乙装置中,用粘合剂将MnO2制成团,放在多孔塑料片上,连接好装置,气密性良好后打开活塞K1,经长颈漏斗向试管中缓慢加入3% H2O2溶液至___________。欲使反应停止,关闭活塞K1即可,此时装置中的现象是___________。
(3)丙装置可用于制备较多O2,催化剂铂丝可上下移动。制备过程中如果体系内压强过大,安全管中的现象是___________,此时可以将铂丝抽离H2O2溶液,还可以采取的安全措施是___________。
(4)丙装置的特点是___________(填序号)。
a.可以控制制备反应的开始和结束
b.可通过调节催化剂与液体接触的面积来控制反应的速率
c.与乙装置相比,产物中的O2含量高、杂质种类少
Ⅱ.氧化C2H5OH
该小组同学设计的氧化C2H5OH的装置如图(夹持装置省略)
(5)在图中方框内补全干燥装置和干燥剂。___________
Ⅲ.检验产物
(6)为检验上述实验收集到的产物,该小组同学进行了如下实验并得出相应结论。
实验①~③中的结论不合理的是___________(填序号),原因是___________。
【答案】(1)分液漏斗 锥形瓶
(2)刚好没过MnO2固体 试管内的H2O2溶液被压入长颈漏斗中,与MnO2分离
(3)液面上升 打开弹簧夹K2 (4)ab
(5)(6 ① 乙醇也能使酸性KMnO4溶液褪色
【解析】用双氧水和催化剂制取氧气。制得的氧气经干燥后进入盛有乙醇的圆底烧瓶中,和热的乙醇一起进入硬质玻璃管中,在铜的催化作用下发生乙醇的催化氧化反应生成乙醛。生成的乙醛进入试管中,被冷凝收集。(1)根据仪器构造可知,甲装置中主要仪器的名称为分液漏斗和锥形瓶;(2)乙装置是启普发生器的简易装置,可以随时控制反应的发生和停止。用粘合剂将MnO2制成团,放在多孔塑料片上,连接好装置,气密性良好后打开活塞K1,经长颈漏斗向试管中缓慢加入3% H2O2溶液至刚好没过MnO2固体,此时可以产生氧气,氧气通过导管导出。欲使反应停止,关闭活塞K1,此时由于气体还在产生,使容器内压强增大,可观察到试管内的H2O2溶液被压入长颈漏斗中,与MnO2分离;(3)丙装置用圆底烧瓶盛装H2O2溶液,可用于制备较多O2,催化剂铂丝可上下移动可以控制反应速率。制备过程中如果体系内压强过大,H2O2溶液会被压入安全管中,可观察到安全管中液面上升,圆底烧瓶中液面下降。此时可以将铂丝抽离H2O2溶液,使反应速率减慢,还可以打开弹簧夹K2,使烧瓶内压强降低;(4)a项,催化剂铂丝可上下移动可以控制制备反应的开始和结束,a正确;b项,催化剂与液体接触的面积越大,反应速率越快,可通过调节催化剂与液体接触的面积来控制反应的速率,b正确;c项,丙装置用圆底烧瓶盛装H2O2溶液,与乙装置相比,可用于制备较多O2,但产物中的O2含量和杂质种类和乙中没有区别,c错误;故选ab;(5)氧气可以用浓硫酸干燥,所以可以用一个洗气瓶,里面盛装浓硫酸干燥氧气,如图;(6)实验①不合理,因为乙醇有挥发性,会混入生成的乙醛中,乙醇也能使酸性高锰酸钾溶液褪色,所以酸性高锰酸钾溶液褪色不能证明产物中含有乙醛。
必备知识
考点二 氯气的实验室制法及性质实验
1.有机综合实验中的常用装置及注意问题
(1)常用装置
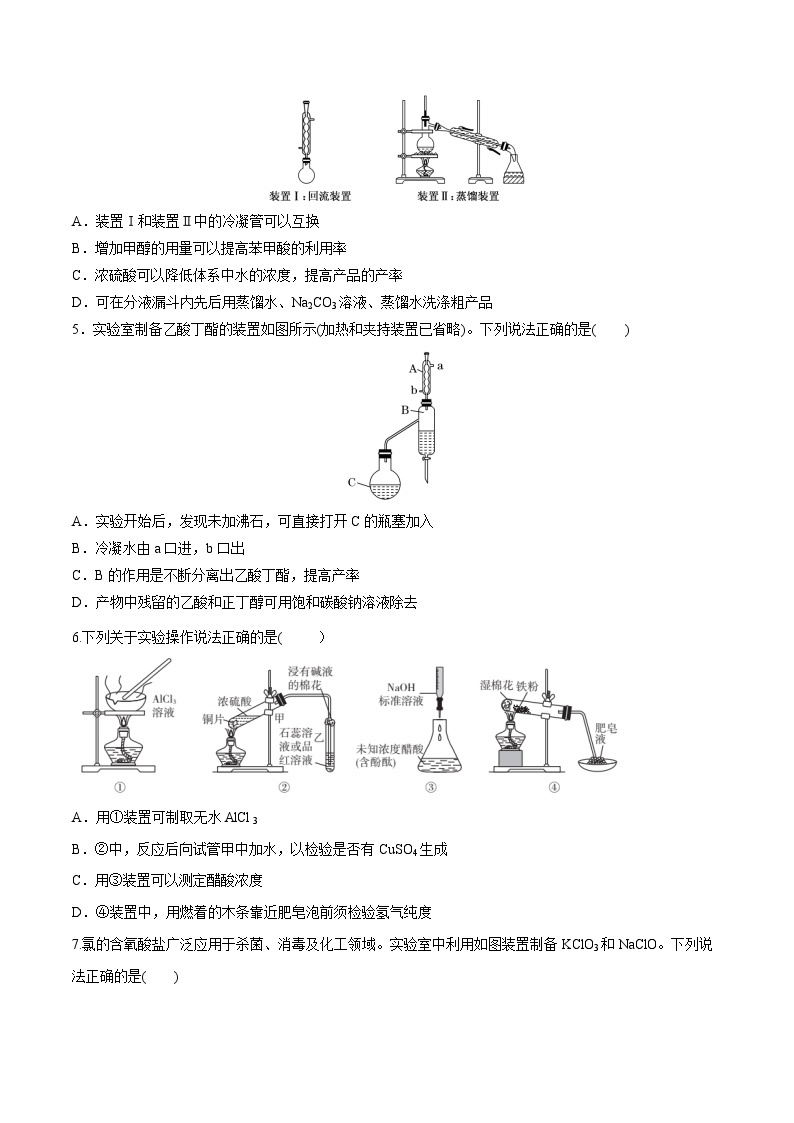
①反应装置:有机物易挥发,常采用冷凝回流装置减少有机物的挥发,提高原料的利用率和产物的产率。
②蒸馏装置:利用有机物沸点的不同,用蒸馏的方法可以实现分离。
(2)注意问题:
2.解答有机物制备实验题的思维流程
要点突破
1.如图是利用丙醇制取丙烯,再用丙烯制取1,2-二溴丙烷的装置,反应过程中装置①中有刺激性气味的气体生成,且会看到装置①中溶液变黑。下列说法不正确的是( )
A.加热时若发现装置①中未加碎瓷片,应冷却后补加
B.装置②的试管中可盛放NaOH溶液以除去副产物
C.装置④中的现象是溶液橙色变浅直至无色
D.反应后可用分液漏斗从装置④的混合物中分离出1,2二溴丙烷,并回收CCl4
【答案】C
【解析】由题给流程可知,向甲苯、苯胺、苯甲酸的混合溶液中加入盐酸,盐酸将微溶于水的苯胺转化为易溶于水的苯胺盐酸盐,分液得到水相Ⅰ和有机相Ⅰ;向水相中加入氢氧化钠溶液将苯胺盐酸盐转化为苯胺,分液得到苯胺粗品①;向有机相中加入水洗涤除去混有的盐酸,分液得到废液和有机相Ⅱ,向有机相Ⅱ中加入碳酸钠溶液将微溶于水的苯甲酸转化为易溶于水的苯甲酸钠,分液得到甲苯粗品②和水相Ⅱ;向水相Ⅱ中加入盐酸,将苯甲酸钠转化为苯甲酸,经结晶或重结晶、过滤、洗涤得到苯甲酸粗品③。A.苯胺分子中含有的氨基能与盐酸反应,但不能与氢氧化钠溶液反应,故A错误;B.由分析可知,得到苯胺粗品①的分离方法为分液,得到苯甲酸粗品③的分离方法为结晶或重结晶、过滤、洗涤,获取两者的操作方法不同,故B错误;C.由分析可知,苯胺粗品、甲苯粗品、苯甲酸粗品依次由①、②、③获得,故C正确;D.由分析可知,①、②为液相,③为固相,都不是两相混合体系,故D错误;故选C。
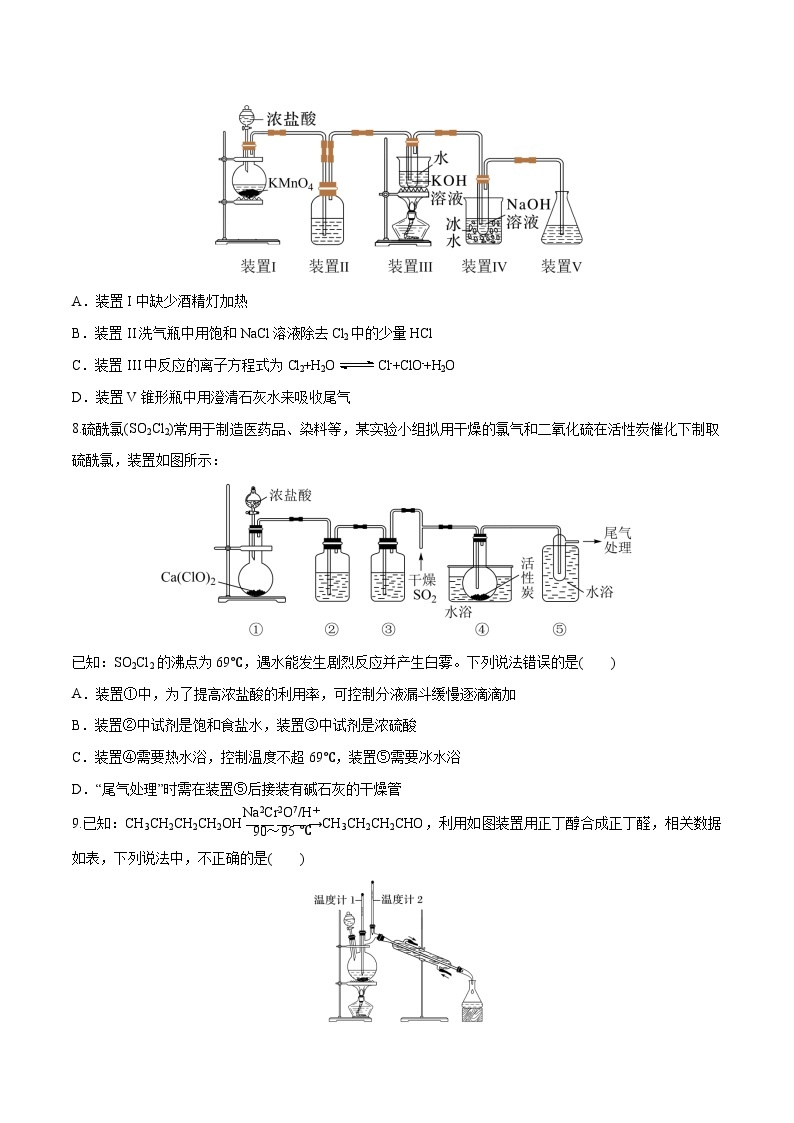
2.实验室制备溴苯的反应装置如图所示,关于实验操作或叙述错误的是( )
A.向圆底烧瓶中滴加苯和溴的混合液前需先打开K
B.实验中装置b中的液体逐渐变为浅红色
C.装置c中碳酸钠溶液的作用是吸收溴化氢
D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯
【答案】D
【解析】苯和溴均易挥发,苯与液溴在溴化铁作用下发生剧烈的放热反应,释放出溴化氢气体(含少量苯和溴蒸气),先打开K,后加入苯和液溴,避免因装置内气体压强过大而发生危险,A项正确;四氯化碳用于吸收溴化氢气体中混有的溴单质,防止溴单质与碳酸钠溶液反应,四氯化碳呈无色,吸收红棕色溴蒸气后,液体呈浅红色,B项正确;溴化氢极易溶于水,倒置漏斗防倒吸,碳酸钠溶液呈碱性,易吸收溴化氢,发生反应为Na2CO3+HBr===NaHCO3+NaBr,NaHCO3+HBr===NaBr+CO2↑+H2O,C项正确;反应后的混合液中混有苯、液溴、溴化铁和少量溴化氢等,提纯溴苯的正确操作是①用大量水洗涤,除去可溶性的溴化铁、溴化氢和少量溴;②用氢氧化钠溶液洗涤,除去剩余的溴等物质;③用水洗涤,除去残留的氢氧化钠;④加入干燥剂除去水,过滤;⑤对有机物进行蒸馏,除去杂质苯,从而提纯溴苯,分离溴苯,不用“结晶”的方法,D项错误。
3.香豆素是维生素K拮抗剂。实验室中采用水杨醛和乙酸酐来合成香豆素:
已知某些有机物的性质见下表:
香豆素的制备装置如图所示。
回答下列问题:
(1)装置中需要安装的温度计1的量程是:___________(填字母)。
a.100℃ b.150℃ c.250℃ d.500℃
(2)仪器b的名称是___________,装置采用空气冷凝,而不采用水冷凝的原因是___________。
(3)Y形接头上安装温度计进行监控,当温度达到118℃时,可由分水器下方及时放出冷凝液,该冷凝液的成分是___________(填化学式),这样做的目的是___________。
(4)在制取的香豆素中发现含有少量的水杨酸(),用化学方程式表示其产生的原因:___________________________________。
【答案】(1)c
(2) (空气)冷凝管 蒸气的温度较高,用空气冷凝可防止冷凝管通水冷却导致玻璃温差过大而炸裂
(3) CH3COOH 防止乙酸过多时流回烧瓶,会抑制反应原理中第一步反应的正向进行
(4)2+O22
【解析】水杨醛和乙酸酐在醋酸钠/150-200℃条件下发生反应生成和乙酸,故使用分水器分离出乙酸,促进此步正向进行。然后发生失水反应生成香豆素和乙酸。 (1)温度计1测量的为混合液的反应温度,根据反应条件可得温度计1的量程是250℃。(2)仪器b为(空气)冷凝管,采用空气冷凝,而不采用水冷凝的原因为蒸气的温度较高,用空气冷凝可防止冷凝管通水冷却导致玻璃温差过大而炸裂。(3)乙酸的沸点为118℃,故当温度达到118℃时,可由分水器下方及时放出冷凝液,该冷凝液的成分是CH3COOH,防止乙酸过多时流回烧瓶,会抑制反应原理中第一步反应的正向进行。(4)水杨醛氧化为水杨酸的化学方程式为2 +O22
制取装置
可用来制取的气体
反应原理
固+固气
O2
2KClO3eq \(=====,\s\up11(MnO2),\s\d4(△))2KCl+3O2↑
NH3
2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O
固+液气
Cl2
MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O
HCl
NaCl+H2SO4(浓)NaHSO4+HCl↑
固(块状)+液→气
H2
2H++Zn===H2↑+Zn2+
CO2
CaCO3+2HCl===CaCl2+CO2↑+H2O
固+液→气
O2
2H2O2eq \(=====,\s\up7(MnO2))2H2O+O2↑
H2
Zn+H2SO4===ZnSO4+H2↑
CO2
CaCO3+2HCl===CaCl2+H2O+CO2↑
NH3
NH3·H2O(浓)eq \(=====,\s\up7(CaO)) NH3↑+H2O
Cl2
2KMnO4+16HCl(浓)=== 2KCl+2MnCl2+8H2O+5Cl2↑
SO2
Na2SO3+H2SO4===Na2SO4+H2O+SO2↑
收集方法
排水法
向上排空气法
向下排空气法
收集原理
收集的气体不与水反应且难溶于水
收集的气体密度比空气大,且与空气密度相差较大,不与空气中成分反应
收集的气体密度比空气小,且与空气密度相差较大,不与空气中成分反应
收集装置
适用的气体
H2、O2、NO、CH4等
Cl2、CO2、NO2、SO2等
H2、NH3等
排液集
气装置
装置(Ⅰ)
从a管进气b管出水可收集难溶于水的气体,如H2、O2等。若将广口瓶中的液体更换,还可以收集以下气体
①饱和食盐水——收集Cl2 ②饱和NaHCO3溶液——收集CO2
③饱和NaHS溶液——收集H2S ④四氯化碳——收集HCl或NH3
装置(Ⅱ)
储气式集气:气体从橡胶管进入,可将水由A瓶排入B瓶,在瓶A中收集到气体
①液体容纳
图甲、乙原理相同,当易溶性气体被吸收液吸收时,导管内压强减小,吸收液上升到漏斗或干燥管中,导致烧杯中液面下降;使漏斗口、干燥管脱离液面,吸收液受自身重力作用又流回烧杯内,从而防止吸收液倒吸
②分液式
如图所示,NH3、HCl等易溶于水却不溶于CCl4的气体,在CCl4中形成气泡,增大与水的接触面积,进行间接吸收,可以达到防倒吸的目的
③安全瓶
、
如图所示,当吸收液发生倒吸时,倒吸进来的吸收液进入安全瓶,从而防止吸收液进入受热仪器或反应容器,起到防倒吸作用
实验序号
检验试剂和反应条件
现象
结论
①
酸性KMnO4溶液
紫红色褪去
产物含有乙醛
②
新制Cu(OH)2,加热
生成砖红色沉淀
产物含有乙醛
③
微红色含酚酞的NaOH溶液
微红色褪去
产物可能含有乙酸
温度计水银球的位置
若要控制反应温度,温度计的水银球应插入反应液中;
若要选择收集某温度下的馏分,则温度计的水银球应放在蒸馏烧瓶支管口附近。
冷凝回流
有机化合物易挥发,因此在反应中通常要采用冷凝回流装置,以减少有机化合物的挥发,提高原料的利用率和产物的产率。如图1、图3中的冷凝管,图2中的长玻璃管B的作用都是冷凝回流。
冷凝管的选择
球形冷凝管只能用于冷凝回流,直形冷凝管既能用于冷凝回流,又能用于冷凝收集馏分。
冷凝管的进出水方向
下口进上口出
加热方法的选择
酒精灯的火焰温度一般在400~500 ℃,所以需要温度不太高的实验都可用酒精灯加热,例如乙酸乙酯的制取、石油的蒸馏等实验等。若温度要求更高,可选用酒精喷灯或电炉加热。
除上述加热方式外还可以根据加热的温度要求选择水浴、油浴、沙浴加热,水浴加热的温度不超过100 ℃
防暴沸
加沸石或碎瓷片,防止溶液暴沸,若开始忘加沸石,需冷却后补加。
常见的用于干燥有机物的药品
无水氯化钙、无水硫酸镁、无水硫酸钙、无水碳酸钾等;
根据题给信息,初步判定物质性质
有机物制备中一般会给出相应的信息,通常会以表格的形式给出,表格中的数据主要是有机化合物的密度、沸点和在水中的溶解性,在分析这些数据时要多进行横向和纵向的比较。密度主要是与水比较,沸点主要是表中各物质间的比较,溶解性主要是判断溶还是不溶。主要是根据这些数据选择分离、提纯的方法
注意仪器名称和作用
所给的装置图中有一些不常见的仪器,要明确这些仪器的作用,特别是无机制备实验中不常见的三颈烧瓶、球形冷凝管等
关注有机反应条件
大多数有机反应副反应较多,且为可逆反应,因此设计有机物制备实验方案时,要注意控制反应条件,尽可能选择步骤少、副产物少的反应(由于副产物多,需要进行除杂、净化)。另外,若为两种有机物参加的可逆反应,应考虑多加一些廉价的有机物,以提高另一种有机物的转化率和生成物的产率
有机物
熔点/℃
沸点/℃
溶解性
香豆素
69
297~299
溶于乙醇,不溶于冷水,较易溶于热水
水杨醛
-7
197
微溶于水,溶于乙醇
乙酸酐
-73
139
溶于水形成乙酸,热的乙酸酐可溶解乙酸钠
乙酸
16.7
118
溶于乙醇、水
第48讲 物质性质、化学反应综合实验探究-【高效备考】2024年高考化学一轮复习讲义+分层练习: 这是一份第48讲 物质性质、化学反应综合实验探究-【高效备考】2024年高考化学一轮复习讲义+分层练习,文件包含第48讲物质性质化学反应综合实验探究分层练习-高效备考2024年高考化学一轮复习讲义+分层练习原卷版docx、第48讲物质性质化学反应综合实验探究讲义-高效备考2024年高考化学一轮复习讲义+分层练习原卷版docx、第48讲物质性质化学反应综合实验探究分层练习-高效备考2024年高考化学一轮复习讲义+分层练习解析版docx、第48讲物质性质化学反应综合实验探究讲义-高效备考2024年高考化学一轮复习讲义+分层练习解析版docx等4份试卷配套教学资源,其中试卷共67页, 欢迎下载使用。
第47讲 物质的检测综合实验探究-【高效备考】2024年高考化学一轮复习讲义+分层练习: 这是一份第47讲 物质的检测综合实验探究-【高效备考】2024年高考化学一轮复习讲义+分层练习,文件包含第47讲物质的检测综合实验探究分层练习-高效备考2024年高考化学一轮复习讲义+分层练习原卷版docx、第47讲物质的检测综合实验探究讲义-高效备考2024年高考化学一轮复习讲义+分层练习原卷版docx、第47讲物质的检测综合实验探究分层练习-高效备考2024年高考化学一轮复习讲义+分层练习解析版docx、第47讲物质的检测综合实验探究讲义-高效备考2024年高考化学一轮复习讲义+分层练习解析版docx等4份试卷配套教学资源,其中试卷共69页, 欢迎下载使用。
第9讲 物质的分离和提纯-【高效备考】2024年高考化学一轮复习讲义+分层练习: 这是一份第9讲 物质的分离和提纯-【高效备考】2024年高考化学一轮复习讲义+分层练习,文件包含第9讲物质的分离和提纯分层练习-高效备考2024年高考化学一轮复习讲义+分层练习原卷版docx、第9讲物质的分离和提纯讲义-高效备考2024年高考化学一轮复习讲义+分层练习原卷版docx、第9讲物质的分离和提纯分层练习-高效备考2024年高考化学一轮复习讲义+分层练习解析版docx、第9讲物质的分离和提纯讲义-高效备考2024年高考化学一轮复习讲义+分层练习解析版docx等4份试卷配套教学资源,其中试卷共44页, 欢迎下载使用。












