

北京市密云二中2023-2024学年高二上学期10月月考化学试卷+
展开可能用到的相对原子质量:
H-1 C-12 N-14 O-16 Na-23 S-32 Cl-35.5 Fe-56 Cu-64
第一部分 选择题 (共42分)
请在每小题列出的四个选项中,选出最符合题目要求的一项。
1.下列做法能减缓化学反应速率的是( )
A.把食物放在冰箱里冷藏
B.用H2O2溶液制O2时,通常加入少量的MnO2
C.利用乙醇和乙酸制备乙酸乙酯,加入浓硫酸并加热
D.用浓度较大的盐酸溶解石灰石
2. 我国科学家利用如下反应实现了低温制氢。CO(g) + H2O(g)CO2(g) + H2(g),一定温度下,在密闭容器中,当CO、H2O、CO2、H2的浓度不再变化时,下列说法正确的是( )
A. CO和H2O全部转化为CO2和H2 B. 该反应已达化学平衡状态
C. 正、逆反应速率相等且等于零 D. CO、H2O、CO2、H2的浓度一定相等
3. 下列化学用语或图示表达不正确的是( )
A. N2的结构式:N≡N
B. Na+的结构示意图:
C. S在元素周期表中的位置:第三周期,ⅥA族
D. CO2的电子式:
4. 下列物质的应用中,利用了氧化还原反应的是( )
A. 用石灰乳脱除烟气中的SO2 B. 用明矾[KAl(SO4)2⋅12H2O]处理污水
C. 用盐酸去除铁锈(主要成分Fe2O3⋅xH2O) D. 用84消毒液(有效成分NaClO)杀灭细菌
5. 下列离子方程式与所给事实不相符的是( )
A. Cl2制备84消毒液(主要成分是NaClO):Cl2+2OH-=Cl-+ClO-+H2O
B. 食醋去除水垢中的CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑
C. 利用覆铜板制作印刷电路板:2Fe3++Cu=2Fe2++Cu2+
D. Na2S去除废水中的Hg2+:Hg2++S2-=HgS↓
6.抗坏血酸(即维生素C)有较强的还原性,具有抗氧化作用,是常用的食品抗氧化剂。
下列有关抗坏血酸的说法不正确的是( )
A.在空气中可发生氧化反应
B.能使酸性KMnO4溶液褪色
C.抗坏血酸与脱氢抗坏血酸互为同分异构体
D.分子中的官能团有羟基、酯基和碳碳双键
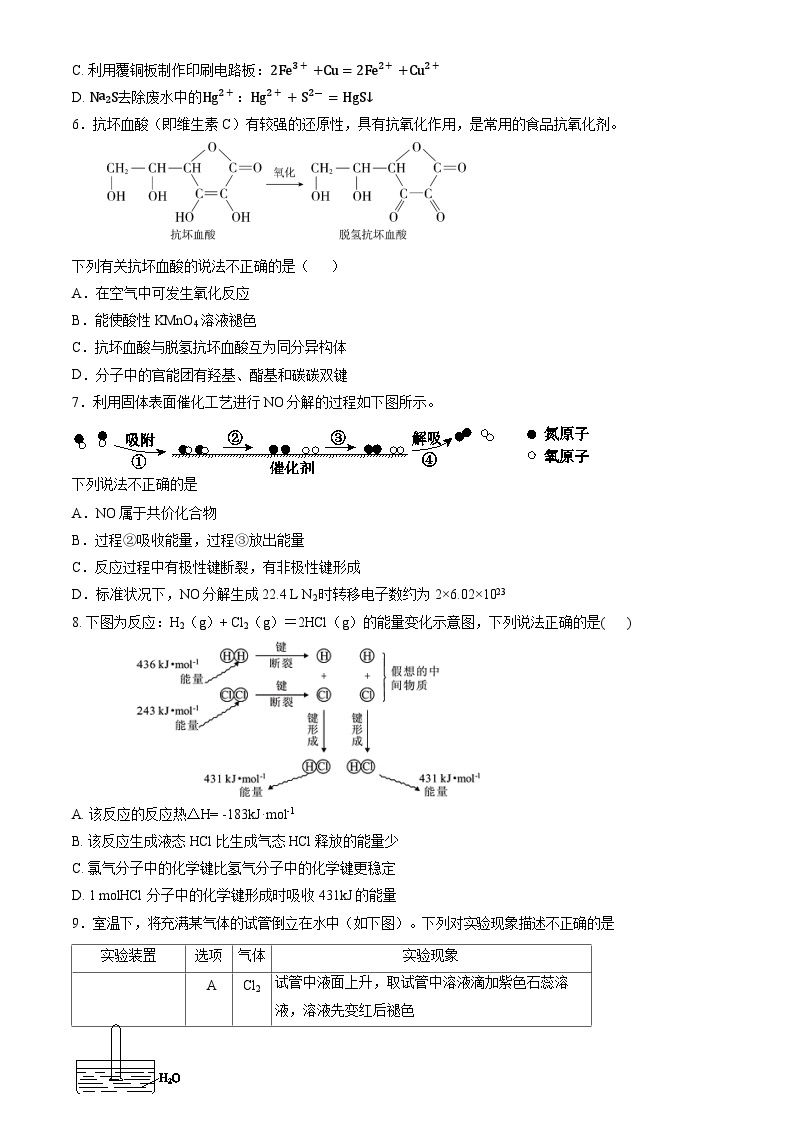
7.利用固体表面催化工艺进行NO分解的过程如下图所示。
下列说法不正确的是
8. 下图为反应:H2(g)+ Cl2(g)=2HCl(g)的能量变化示意图,下列说法正确的是( )
A. 该反应的反应热△H= -183kJ·ml-1
B. 该反应生成液态HCl比生成气态HCl释放的能量少
C. 氯气分子中的化学键比氢气分子中的化学键更稳定
D. 1 mlHCl分子中的化学键形成时吸收431kJ的能量
9.室温下,将充满某气体的试管倒立在水中(如下图)。下列对实验现象描述不正确的是
10. 下列说法正确的是( )
A. 凡是放热反应都是自发的,因为吸热反应都是非自发的
B. 自发反应的熵一定增大,非自发反应的熵一定减小
C. 反应2Mgs+CO2g=Cs+2MgOs能自发进行,则该反应的ΔH<0
D. 常温下,反应C(s)+CO2(g)⇌2CO(g)不能自发进行,则该反应的ΔH<0
11.下列实验中,不能达到实验目的的是( )
12. 离子化合物Na2O2和CaH2与水的反应分别为①2Na2O2+2H2O=4NaOH+O2↑;②CaH2+2H2O=Ca(OH)2+2H2↑。下列说法正确的是( )
A. Na2O2、CaH2中均有非极性共价键
B. ①中水发生氧化反应,②中水发生还原反应
C. Na2O2中阴、阳离子个数比为1:2,CaH2中阴、阳离子个数比为2:1
D. 当反应①和②中转移的电子数相同时,产生的O2和H2的物质的量相同
13. 一定温度下,向10mL 0.40ml/L H2O2溶液中加入适量FeCl3溶液,不同时刻测得生成O2的体积(已折算为标准状况)如下表所示。资料显示,反应分两步进行:①2Fe3++H2O2=2Fe2++O2↑ + 2H+,②H2O2+ 2Fe2++ 2H+=2H2O+2Fe3+,反应过程中能量变化如下图所示。下列说法正确的是( )
A. Fe2+是该反应过程的催化剂
B. 0~10min的平均反应速率:v(H2O2)=0.02ml·L-1·min-1
C. 反应2H2O2(aq)=2H2O(l)+O2(g)在无催化剂时的活化能为E1
D. 反应2H2O2(aq)=2H2O(l)+O2(g)的△H=E1-E2< 0
14. 炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成对环境有不良影响的活化氧,反应过程的能量变化如图。下列说法正确的是( )
A. 生成活化氧的总反应是吸热反应
B. 反应过程中存在氧氧键的断裂和碳氧键的生成
C. 反应前后只有氧元素的化合价发生改变
D. 无水条件下更有利于生成活化氧
15.NO2的储存和还原技术能有效降低柴油发动机在空气过量时排放的NO2,原理如图1
所示。用H2模拟尾气中还原性气体研究了Ba(NO3)2的催化还原过程,如图2所示。
图1 图2
下列说法不正确的是( )
A.反应①为4NO2 + O2 + 2BaO == 2Ba(NO3)2
B.储存和还原技术也能降低尾气排放的NO
C.0~12.5 s内,氢气的消耗速率为v(H2) = 1.6 × 10﹣4 ml/(L·s)
D.反应②分两步进行, 第一步反应消耗的H2与Ba(NO3)2的物质的量之比是1:8
16. 我国科研人员提出了以Ni / Al2O3为催化剂,由CO2和H2转化为产品CH4的反应历程,其示意图如下:
下列说法不正确的是( )
A. 催化剂可有效提高反应物的平衡转化率
B. 总反应方程式为:CO2+4H2⇌CH4+2H2O
C. 在反应历程中,H—H键与C=O键断裂吸收能量
D. 反应过程中,催化剂参与反应,改变反应路径,降低反应的活化能
17. Ni可活化C2H6放出CH4,其反应历程如图所示:
下列关于活化历程的说法正确的是( )
A. 该转化过程△H>0
B. 该反应过程中,最大能垒(活化能)为204.32kJ⋅ml-1
C. 在此反应过程中Ni的成键数目未发生变化
D. 整个过程中,Ni是该反应的催化剂
18. 在恒容密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)⇌Ni(CO)4(g),已知该反应平衡常数与温度的关系如表:
下列说法不正确的是( )
A.上述生成Ni(CO)4(g)的反应为放热反应
B. 升高温度,CO的平衡转化率减小
C. 80℃时,测得c(CO)=0.5ml⋅L-1,c[Ni(CO)4]=1ml⋅L-1,则反应达到平衡状态
D. 25℃时,反应Ni(CO)4(g)⇌Ni(s)+4CO(g)的平衡常数为2×10-5ml⋅L-3
19. 一定温度下,在容积恒为1L的容器中通入一定量N2O4,发生反应N2O4(g)⇌2NO2(g)△H>0,体系中各组分浓度随时间(t)的变化如下表。下列说法正确的是( )
A. 0~60s,N2O4的平均反应速率为v=0.04ml/(L⋅min)
B. 升高温度,反应的化学平衡常数值减小
C. 80s时,再充入NO2、N2O4各0.12ml,平衡不移动
D. 若压缩容器使压强增大,达新平衡后混合气颜色比原平衡时浅
20. Fe3O4(s)与CO(g)主要发生如下反应。
①Fe3O4(s) + CO(g) 3FeO(s) + CO2(g) ΔH1 = +19.3 kJ·ml-1
②Fe3O4(s) + 4CO(g) 3Fe(s) + 4CO2(g) ΔH2
反应的还原产物与温度密切相关。其它条件一定时,Fe3O4(s)和CO(g)反应达平衡时,
CO(g)的体积分数随温度的变化关系如下图所示。下列说法不正确的是( )
A. 反应FeO(s) + CO(g) Fe(s) + CO2(g)的焓变为13(ΔH2 -ΔH1)
B. 根据图像推测,ΔH2应当小于0
C. 反应温度越高,Fe3O4主要还原产物中铁元素的价态越低
D. 温度高于1040℃时,Fe3O4(s)和CO(g)发生的主要反应的化学平衡常数K>4
21.小组同学探究盐溶液对反应Fe 3++ SCN- [Fe(SCN)] 2+(血红色)的影响。
将2 mL 0.01 ml·L-1的FeCl3溶液与2 mL 0.02 ml·L-1的KSCN溶液混合,分别加入等量的试剂①~④,测得平衡后体系的透光率如下图所示。
已知:i.溶液血红色越深,透光率越小,其它颜色对透光率的影响可忽略
ii.Fe3++4Cl-[FeCl4]-(黄色)
下列说法不正确的是( )
A. 注入试剂①后溶液透光率增大,可能是因为反应Fe 3++ SCN- [Fe(SCN)] 2+ 平衡逆向移动引起的
B. 透光率③比②高,可能是阳离子种类或溶液pH导致的
C. 透光率④比③高,可能发生了反应[Fe(SCN)]2+ + 4Cl- [FeCl4] -+ SCN-
D. 若要证明试剂③中Cl-对平衡体系有影响,还应使用0.04 ml·L-1的K2SO4溶液进行实验
第二部分 非选择题 (共58分)
22.(10分)工业合成氨技术开创了人工固氮的重要途径,但能耗高、碳排放量大。开发
温和条件下合成氨的新工艺意义重大。
(1)氮的固定有以下常见方式:
生物固氮:N2NH3
工业合成氨:N2 + 3H22NH3
通过雷电固氮: (写出反应方程式)
(2)断开氮分子中的N≡N键,需要 能量(填“吸收”或“释放”)。
(3)高温不利于提高工业合成氨中N2的平衡转化率。
① 生产中依然选择高温合成氨,目的是 。
② 针对反应速率与平衡产率的矛盾,我国科学家提出了采用M—LiH(M表示金属)复
合催化剂的解决方案。做对比实验,测得反应速率如下图所示。
资料:用单位时间内每克催化剂所获得的NH3的物质的量表示反应速率
a.无LiH,催化效率最高的金属是 。
b.有LiH,反应速率明显增大。文献报道了
M—LiH可能的催化过程如下:
ⅰ.N2 == 2N(在M表面解离)
ⅱ.N + LiH == LiNH
ⅲ. 。
在较低压强、较低温度下合成了NH3,这是合成氨反应研究中的重要突破。
(4)最近,我国科研人员报道了一种氯化镁循环法,可进一步降低能耗。该方法的总反应为2N2 + 6H2O == 4NH3 + 3O2。转化关系如下:
① A是 。
② 科研人员将X与Mg315N2混合反应,证实了氮化镁中氮元素能转化为氨。不考虑其他副反应,产物中= 。
23.(10分) “绿水青山就是金山银山”,近年来,绿色发展、生态保护成为我国展示给世界的一张新“名片”。
Ⅰ.汽车尾气是造成大气污染的重要原因之一,减少氮的氧化物在大气中的排放是环境保护的重要内容之一。请回答下列问题:
(1)已知:N2(g)+O2(g)2NO(g) ΔΗ1=+180.5 kJ·ml-1
C(s)+O2(g)CO2(g) ΔH2=-393.5 kJ·ml-1
2C(s)+O2(g)2CO(g) ΔH3=-221 kJ·ml-1
若某反应的平衡常数表达式为K=c(N2)⋅c2(CO2)c2(NO)⋅c2(CO),则此反应的热化学方程式为________。
(2)N2O5在一定条件下可发生分解反应:2N2O5(g)4NO2(g)+O2(g),一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是______(填字母)。
A. NO2和O2的浓度之比保持不变 B. 容器中压强不再变化
C. 2v正(NO2)=v逆(N2O5) D. 气体的密度保持不变
Ⅱ.甲醇、乙醇来源丰富,价格低廉,运输贮存方便,都是重要的化工原料,有着重要的用途和应用前景,可以用多种方法合成。
(3)已知CO2(g)+3H2(g)CH3OH(g)+H2O(g),将CO2和H2按物质的量之比1:3充入容积为2.0 L的恒容密闭容器中,如图1表示压强为0.1 MPa和5.0 MPa下CO2转化率随温度的变化关系。
①a、b两点化学反应速率分别用va、vb表示,则va ___ vb(填“大于”“小于”或“等于”)。
②写出a点对应的平衡常数表达式K=_____________。
(4)在1.0 L恒容密闭容器中投入1 ml CO2和2.75 ml H2发生反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g),实验测得不同温度及压强下,平衡时甲醇的物质的量变化如图2所示,下列说法正确的是______(填字母)。
A.该反应的正反应为放热反应
B.压强大小关系为p1
D.在p2及512K时,图中N点 v正
①图3中投料比相同,温度T3>T2>T1,则该反应的焓变ΔH_____ 0(填“>”或“<”)。
②m=3时,恒压条件下各物质的物质的量分数与温度的关系如图4所示,则曲线b代表的物质为______________(填化学式)。
24.(8分)钢铁行业酸洗工艺产生的废液主要含有FeCl2和HCl。以空气和钢铁酸洗废
液为原料可以合成Fe2(OH)nCl6-n。工业上常加入NaNO2,以提高反应速率。
(1)向酸洗废液中加入少量NaNO2,并通入空气。
前期发生的反应:
= 1 \* ROMAN I.HCl + NaNO2 === HNO2 + NaCl
= 2 \* ROMAN II.HCl + HNO2 + FeCl2 === FeCl3 + NO + H2O
后期转化过程如图:
已知:
i.催化剂加快反应的一种方式是自身参与反应最终又生成,自身的质量和化学性质并不发生改变。
ii.室温下可发生反应Fe2+ + NO === [Fe(NO)]2+,[Fe(NO)]2+ 受热可再分解为Fe2+和NO。
①反应 = 4 \* ROMAN IV的化学方程式是 。
②下列说法正确的是_____(填字母)。
a.由反应 = 2 \* ROMAN II可以判断此条件下HNO2的氧化性强于Fe3+
催化剂
b.加入NaNO2的主要目的是得到NO,作为后期反应的催化剂
c.后期转化过程的总反应可表示为 4FeCl2 + O2 + (4-2n)HCl ===== 2Fe2(OH)nCl6-n + (2-2n)H2O
= 3 \* GB3 ③反应过程中需控制温度在80 ℃左右。温度不能太低的原因是_____(写出两点)。
(2)为了测定产品的质量,用以下方法测定产品中铁元素的质量分数:
取a g产品,加入一定量的硫酸,充分反应后加入蒸馏水稀释,得到100 mL 待测液。取20 mL待测液,加入足量KI溶液,充分反应后再与c ml/L Na2S2O3溶液反应,恰好消耗v mL Na2S2O3溶液。
已知:
i.Na2S2O3 与I2的反应为:I2 + 2S2O2- 3=== 2I- + S4O2- 6
ii.溶液酸性较强时Na2S2O3不稳定,可发生反应:
Na2S2O3 + H2SO4 === Na2SO4 + SO2↑ + S↓ + H2O
①加入硫酸不能过多,主要原因有两点:
硫酸过多时,溶液中c(H+)浓度过大,会加快O2将I-氧化为I2,从而造成误差。写
出O2氧化I- 的离子方程式_____。
b._____。
②产品中铁元素的质量分数为_____。
25. (11分) 氯气可用于制取漂白剂和自来水消毒。
(1)下图是实验室制备氯气的制备和除杂装置
①A为氯气发生装置。A中反应方程式是_______(锰被还原为)。
②将除杂装置B补充完整并标明所用试剂_______。
(2)“84”消毒液也可用于漂白,其工业制法是控制在常温条件下,将氯气通入NaOH溶液中,反应的离子方程式为_______。
(3)同学们探究“84”消毒液在不同pH下使红纸褪色的情况,做了如下实验:
步骤1:将5mL市售“84”消毒液稀释100倍,测得稀释后溶液的;
步骤2:将稀释后溶液各20mL分别加入3个洁净的小烧杯中;
步骤3:用溶液将3个烧杯内溶液的pH分别调至10、7和4(溶液体积变化忽略不计)。
步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如下:
已知,溶液中、HClO和物质的量分数随溶液pH变化的关系如下图所示:
①由实验现象可得以下结论:溶液pH在4~10范围内,pH越大,红纸褪色_______。
②结合图像进行分析,b、c两烧杯中实验现象出现差异的原因是_______。
(4)由于氯气会与自来水中的有机物发生反应生成对人体有害的物质,人们尝试研究并使用新的自来水消毒剂,如气体就是一种新型高效含氯消毒剂。
①一种制备的方法是用通入硫酸酸化的溶液中,反应的离子方程式为_______。
②另一种制备的方法是用与盐酸反应,同时有生成,产物中体积约占,每生成,转移_______。
③在杀菌消毒过程中会产生副产物亚氯酸盐,需将其转化为除去。下列试剂中,可将转化为的是_______(填字母序号)。
a. b. c. d.KI
26.(10分)碳中和是目前社会备受关注的重要议题,碳中和是指CO2的排放总量和减少总量相当,对于改善环境,实现绿色发展至关重要。
(1)将燃煤产生的CO2回收再利用,可有效减少碳排放总量。以CO2和H2O为原料制备HCOOH和O2的原电池装置如图所示。其中,电极a作__________(填“正极”或“负极”);CO2 __________(填“得到”或“失去”)电子生成HCOOH;电池内部,H+的移动方向为 __________(填“a→b”或“b→a”)。
(2)以TiO2为催化剂的光热化学循环分解CO2反应为碳中和提供了一条新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
①上述过程,能量变化形式主要由太阳能转化为__________。
②根据上述信息可知,利用TiO2催化分解2mlCO2g生成2mlCOg和1mlO2g时需要 __________(填“吸收”或“放出”)556kJ能量。
(3)为发展低碳经济,科学家提出可以用氧化锆锌作催化剂,将CO2转化为重要有机原料CH3OH,该反应的化学方程式为CO2g+3H2gCH3OHg+H2Og。在容积为2L的恒温密闭容器中,充入1mlCO2和3mlH2,CO2和CH3OH的物质的量随时间变化的曲线如图所示。分析图中数据,回答下列问题。
①反应在0∼2min内,vCO2= __________ ml·L-1·min-1。
②2min时,反应是否达到化学平衡? __________(填“是”或“否”);4min时,正反应速率 __________逆反应速率(填“>”“<”或“=”);6min时,将容器的容积变为3L,此时化学反应速率 __________(填“增大”、“减小”或“不变”)。
③对于上述反应,下列叙述正确的是__________。
a.当各气体的物质的量不再改变时,该反应已达平衡状态。
b.当该反应达到平衡后,nCO2:nH2:nCH3OH:nH2O=1:3:1:1。
c.由图可知,2min时CH3OH的生成速率大于6min时CH3OH的分解速率。
d.提高反应的温度,可以实现CO2的完全转化
27.(9分) 研究不同pH时CuSO4溶液对H2O2分解的催化作用。
资料:a.Cu2O为红色固体,难溶于水,能溶于硫酸,生成Cu和Cu2+。
b.CuO2为棕褐色固体,难溶于水,能溶于硫酸,生成Cu2+和H2O2。
c.H2O2有弱酸性:H2O2⇌H++HO2-,HO2-⇌H++O22-。
(1)经检验生成的气体均为O2,Ⅰ中CuSO4催化分解H2O2的化学方程式是________。
(2)对Ⅲ中棕褐色沉淀的成分提出2种假设:ⅰ.CuO2,ⅱ.Cu2O和CuO2的混合物。
为检验上述假设,进行实验Ⅳ:过滤Ⅲ中的沉淀,洗涤,加入过量硫酸,沉淀完全溶解,溶液呈蓝色,并产生少量气泡。
①若Ⅲ中生成的沉淀为CuO2,其反应的离子方程式是_______________________。
②依据Ⅳ中沉淀完全溶解,甲同学认为假设ⅱ不成立,乙同学不同意甲同学的观点,理由是______________________________________________。
③为探究沉淀中是否存在Cu2O,设计如下实验:
将Ⅲ中沉淀洗涤、干燥后,取ag固体溶于过量稀硫酸,充分加热。冷却后调节溶液pH,以PAN为指示剂,向溶液中滴加cml/L EDTA溶液至滴定终点,消耗EDTA溶液VmL。V=_________,可知沉淀中不含Cu2O,假设ⅰ成立。[已知:Cu2++EDTA=EDTA-Cu2+,M(CuO2)=96 g/ml,M(Cu2O)=144 g/ml]
(3)结合方程式,运用化学反应原理解释Ⅲ中生成的沉淀多于Ⅱ中的原因______。
(4)研究Ⅰ、Ⅱ、Ⅲ中不同pH时H2O2分解速率不同的原因。
实验Ⅴ:在试管中分别取1 mL pH=2、3、5的1 ml/L Na2SO4溶液,向其中各加入0.5 mL 30% H2O2溶液,三支试管中均无明显现象。
实验Ⅵ:________________________________________(填实验操作和现象),说明CuO2能够催化H2O2分解。
(5)综合上述实验,Ⅰ、Ⅱ、Ⅲ中不同pH时H2O2的分解速率不同的原因是 。
试卷说明
1.本试卷共18页,分为两个部分。第一部分(选择题)21道小题,共42分;
第二部分(非选择题)6道大题,共58分。
2.考试时间为90分钟,全卷共100分。请将答案填写在答题卡的相应位置,
必须用黑色字迹的笔作答。
A.NO属于共价化合物
B.过程 = 2 \* GB3 ②吸收能量,过程 = 3 \* GB3 ③放出能量
C.反应过程中有极性键断裂,有非极性键形成
D.标准状况下,NO分解生成22.4 L N2时转移电子数约为2×6.02×1023
实验装置
选项
气体
实验现象
A
Cl2
试管中液面上升,取试管中溶液滴加紫色石蕊溶液,溶液先变红后褪色
B
SO2
试管中液面上升,取试管中溶液滴加紫色石蕊溶液,溶液先变红后褪色
C
NO2
试管中液面逐渐上升,停止后,向试管中再缓缓通入一定量的O2,试管中的液面会继续上升
D
NH3
试管中液面迅速上升,取试管中溶液滴加酚酞溶液,溶液显红色
验证氨水有
挥发性
检验NaHCO3
分解产生的CO2
实验室制取
少量氨气
验证NaOH在水的作
用下发生电离
A
B
C
D
t/min
0
3
6
10
V(O2)/mL
0
9.9
17.2
22.4
温度/℃
25
80
230
平衡常数/ml-3⋅L3
5×104
2
1.9×10-5
t/s
0
20
40
60
80
c(N2O4)/(ml/L)
0.100
0.062
0.048
0.040
0.040
c(NO2)/(ml/L)
0
0.076
0.104
0.120
0.120
烧杯
溶液的pH
现象
a
10
10min后,红纸基本不褪色;4h后红纸褪色
b
7
10min后,红纸颜色变浅;4h后红纸褪色
c
4
10min后,红纸颜色变得更浅;4h后红纸褪色
编号
实验
现象
Ⅰ
向1 mL pH=2的1 ml/L CuSO4溶液中加入0.5 mL 30% H2O2溶液
出现少量气泡
Ⅱ
向1 mL pH=3的1 ml/L CuSO4溶液中加入0.5 mL 30% H2O2溶液
立即产生少量棕黄色沉淀,出现较明显气泡
Ⅲ
向1 mL pH=5的1 ml/L CuSO4溶液中加入0.5 mL 30% H2O2溶液
立即产生大量棕褐色沉淀,产生大量气泡
北京市密云区第二中学2023-2024学年高二上学期期中考试(选考)化学试卷含答案: 这是一份北京市密云区第二中学2023-2024学年高二上学期期中考试(选考)化学试卷含答案,共19页。试卷主要包含了本试卷共14页,分为两个部分,已知反应等内容,欢迎下载使用。
北京市陈经纶中学2023-2024学年高二上学期12月月考化学试卷: 这是一份北京市陈经纶中学2023-2024学年高二上学期12月月考化学试卷,共1页。
赤峰二中2023-2024学年高二上学期第一次月考化学(含答案): 这是一份赤峰二中2023-2024学年高二上学期第一次月考化学(含答案),共14页。试卷主要包含了单选题,填空题,实验题等内容,欢迎下载使用。












