


【寒假作业】(人教版2019)高中化学 高一寒假巩固提升训练 巩固测试卷02-练习.zip
展开一、选择题:本题共18小题,每小题3分,共54分。每小题只有一个选项符合题目要求。
1.(2023下·福建泉州·高一校联考期中)化学与人类历史、生产生活密切相关。下列有关说法不正确的是
A. “爆竹声中一岁除,春风送暖入屠苏”,爆竹的燃放涉及氧化还原反应
B.人类可以利用铝热反应的原理焊接铁轨,也可以冶炼金属V、Cr、Mg等
C.家用铝制器皿不宜用来蒸煮或长时间盛装酸性或碱性的食物
D.指南针是我国的四大发明之一,制造指南针的磁性物质是Fe3O4
【答案】B
【解析】A.爆竹的燃放中有氧气参与,涉及氧化还原反应,A正确;
B.铝热反应放出大量的热能用来焊接铁轨,也可用铝热反应冶炼金属V、Cr,但无法用铝热反应冶炼镁,B错误;
C.铝能与酸或碱反应,家用铝制器皿不宜用来蒸煮或长时间盛装酸性或碱性的食物,C正确;
D.指南针的磁性物质为四氧化三铁,D正确;
故选B。
2.(2023上·辽宁丹东·高一统考期中)分类是认识物质的常用方法,下表中对于相关物质的分类全部正确的一组为
【答案】D
【解析】A.CO属于不成盐氧化物,不是碱性氧化物,A错误;
B.Cl2不属于非电解质,Fe3O4为纯净物,空气为混合物,B错误;
C.Na2O2不属于碱性氧化物,盐酸属于混合物,C错误;
D.各物质分类正确,D正确;
故选D。
3.(2023下·河南郑州·高一统考期末)高铁列车上的烟雾传感器,其主体是有镅()放射源的电离室。下列关于的说法正确的是
A.电子数为146B.质量数为336
C.中子数为241D.质子数为95
【答案】D
【分析】原子符号左下角为质子数,左上角为质量数,质量数等于质子数与中子数的和。原子核外电子数等于原子核内质子数,据此分析解答。
【解析】A.Am是95号元素,则原子核内质子数等于95,由于原子核外电子数等于原子核内质子数,所以其核外电子数为95,A错误;
B.原子符号左上角为质量数,则的质量数为241,B错误;
C.原子符号左下角为质子数,左上角为质量数,质量数等于质子数与中子数的和,则的中子数为241-95=146,C错误;
D.原子符号左下角为质子数,则的质子数为95,D正确;
故选D。
4.(2023上·安徽安庆·高一校考期中)有关3BrF3+5H2O=HBrO3+Br2+9HF+O2↑反应的叙述正确的是
A.还原剂和氧化剂的个数比为3:2
B.HBrO3和HF是还原产物
C.生成1个O2,该反应的电子转移数是5
D.O2的氧化性比BrF3强
【答案】A
【分析】根据反应方程式,BrF3中F显-1价,Br显+3价,H2O中H显+1价,O显-2价,HBrO3中Br显+5价,Br2中Br显0价,O2中O显0价,据此分析;
【解析】A.根据分析可知此反应中还原剂和氧化剂的个数比为3:2,A正确;
B.HBrO3是溴元素化合价升高得到的产物,为氧化产物,HF既不是氧化产物也不是还原产物,B错误;
C.,故生成1个O2,该反应的电子转移数是6,C错误;
D.上述反应中BrF3做氧化剂,O2是氧化产物,氧化剂的氧化性>氧化产物,故O2的氧化性比BrF3弱,D错误;
故选A。
5.(2023上·上海·高一复旦附中校考期中)新型冠状病毒可以通过气溶胶传播,气溶胶属于胶体的一种,下列关于胶体的叙述正确的是
A.依据分散剂的状态可将分散系分为溶液、胶体和浊液
B.胶体的本质特征是具有丁达尔效应
C.雾是气溶胶,在阳光下可以观察到丁达尔效应
D.胶体带电荷,而溶液呈电中性
【答案】C
【解析】A.将分散系分为溶液、胶体和浊液,依据的是分散质粒子的直径大小,A不正确;
B.胶体的本质特征是分散质粒子直径的大小,胶体区别于溶液的方法是丁达尔效应,B不正确;
C.雾是气溶胶,对光能产生散射作用,在阳光下,气溶胶可以观察到丁达尔效应,C正确;
D.胶体呈电中性,胶粒带电荷,溶液呈电中性,溶液中的离子也带电荷,D不正确;
故选C。
6.(2023下·四川宜宾·高一统考期末)下列物质中,含有共价键和离子键的是
A.B.C.D.
【答案】B
【解析】A.水中含有极性共价键,A错误;
B.氢氧化钾中含有离子键和共价键,B正确;
C.氧化钠中含有离子键,C错误;
D.次氯酸中含有极性共价键,D错误;
故选B。
7.(2023上·湖南邵阳·高一校考期中)下列反应的离子方程式书写正确的是
A.钠与水反应:Na + 2H2O = Na++2OH-+ H2↑
B.将氯气通入NaOH溶液:Cl2+2OH-=H2O+C1-+ClO-
C.向碳酸氢钠溶液中滴入盐酸: +2H+ = H2O+CO2↑
D.氢氧化铁与稀硫酸反应:OH-+H+ = H2O
【答案】B
【解析】A.钠与水反应生成氢氧化钠和氢气,反应的离子方程式为2Na + 2H2O =2Na++2OH-+ H2↑,故A错误;
B.氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,反应的离子方程式为Cl2+2OH-=H2O+C1-+ClO-,故B正确;
C.碳酸氢钠溶液与盐酸反应生成氯化钠、二氧化碳和水,反应的离子方程式为HCO +H+ = H2O+CO2↑,故C错误;
D.氢氧化铁与稀硫酸反应生成硫酸铁和水,反应的离子方程式为Fe(OH)3+3H+ =Fe3++3H2O,故D错误;
故选B。
8.(2023上·山东济宁·高一统考期中)氯水中存在多种物质,它们在不同反应中表现出不同性质。下列结论正确的是
A.加入有色布条,片刻后有色布条褪色,说明有存在
B.溶液呈浅黄绿色,且有刺激性气味,说明有存在
C.先加入盐酸酸化,再加入溶液,生成白色沉淀,说明有存在
D.加入溶液,氯水的浅黄绿色消失,说明有存在
【答案】B
【解析】A.次氯酸具有漂白性,使有色布条褪色的物质是HClO,故A错误;
B.氯气是黄绿色气体,且有刺激性气味,如果氯水溶液呈黄绿色,且有刺激性气味,说明有Cl2分子存在,故B正确;
C.加入盐酸酸化的AgNO3溶液产生白色沉淀,说明有Cl-存在,加盐酸酸化引入氯离子,不能证明氯水中是否含有氯离子,故C错误;
D.氯水中氯气与氢氧化钠反应生成氯化钠、次氯酸钠,氯水浅黄绿色消失,不能说明有HClO分子存在,故D错误;
故选B。
9.(2023上·湖北鄂州·高一校联考期中)下列关于气体摩尔体积的说法中,正确的是
A.1 ml由H2、N2组成的混合气体在标准状况下的体积约为22.4 L
B.若气体摩尔体积为22. 4 L/ml,则该气体一定处于标准状况
C.常温常压下,32 g O2所占的体积约为22.4 L
D.在标准状况下,11.2 L N2中含有0. 5 ml氮原子
【答案】A
【解析】A.在标准状况下 ,气体摩尔体积约为22.4 L/ml,1 ml混合气体在标准状况下的体积约为22. 4 L,A项正确;
B.若气体摩尔体积为22. 4 L/ml,不能确定一定处于标准状况,B项错误;
C.常温常压下,气体摩尔体积大于22.4 L/ml,C项错误;
D.在标准状况下,11.2 L N2的物质的量为0.5 ml,0.5 ml N2含有1 ml氮原子,D项错误。
故选A。
10.(2023上·山东枣庄·高一校考期中)下列实验操作正确的是
【答案】C
【解析】A.氯化铁水解生成氢氧化铁和氯化氢,水解吸热且生成的氯化氢易挥发,所以直接加热不能得到无水氯化铁,选项A错误;
B.浓硫酸溶于水放热,需要首先在烧杯中稀释浓硫酸并冷却后再转移至容量瓶中,选项B错误;
C.定容时胶头滴管悬于容量瓶上方滴加蒸馏水,视线与刻度线、凹液面的最低点相切,操作正确,选项C正确;
D.碳酸氢钠受热易分解,要比较碳酸氢钠和碳酸钠的热稳定性,需要把碳酸钠放在大试管中,碳酸氢钠放在小试管中,选项D错误;
故选C。
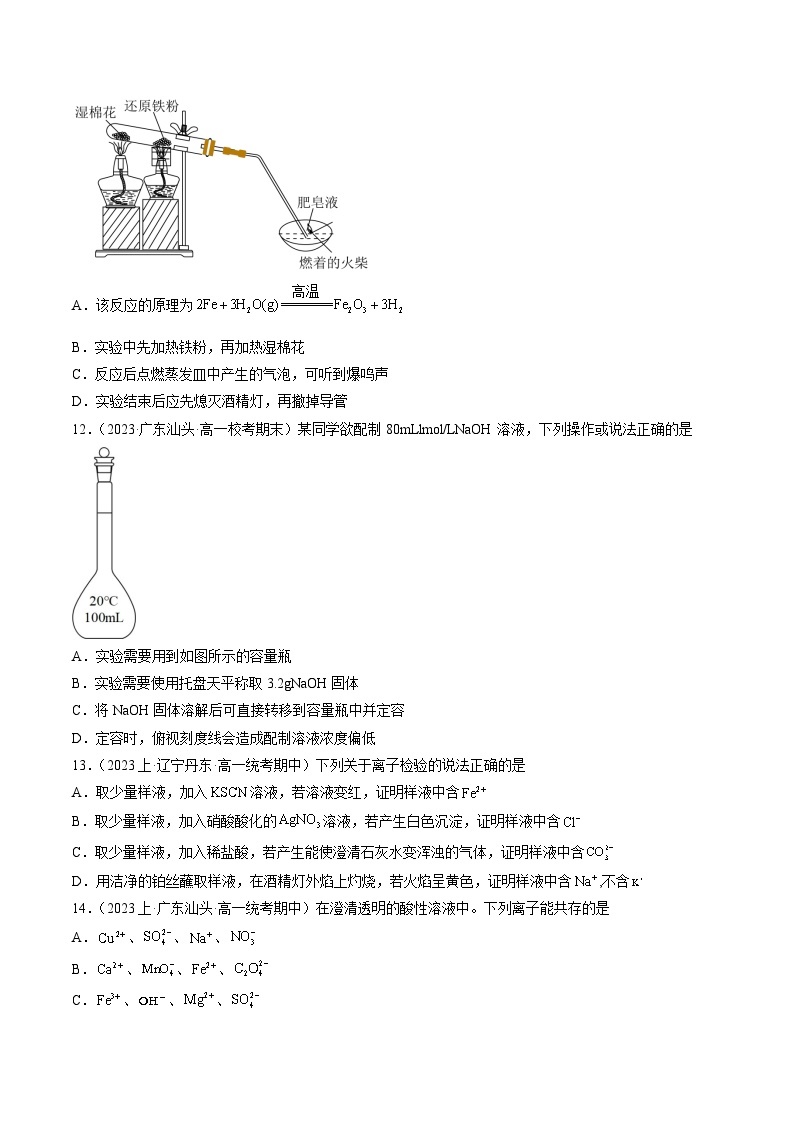
11.(2023上·辽宁丹东·高一统考期中)某同学设计了如图所示的装置,进行还原铁粉与水蒸气反应的实验探究.下列说法正确的是
A.该反应的原理为
B.实验中先加热铁粉,再加热湿棉花
C.反应后点燃蒸发皿中产生的气泡,可听到爆鸣声
D.实验结束后应先熄灭酒精灯,再撤掉导管
【答案】C
【解析】A.反应的化学方程式为:,故A错误;
B.实验中应该先加热湿棉花,产生水蒸气,再加热铁粉,故B错误;
C.加热时试管内铁粉红热,点燃肥皂泡,因混有空气可听到爆鸣声,故C正确;
D.实验结束后为防止倒吸应该先撤导管后熄灭酒精灯,故D错误。
故选C。
12.(2023·广东汕头·高一校考期末)某同学欲配制80mLlml/LNaOH溶液,下列操作或说法正确的是
A.实验需要用到如图所示的容量瓶
B.实验需要使用托盘天平称取3.2gNaOH固体
C.将NaOH固体溶解后可直接转移到容量瓶中并定容
D.定容时,俯视刻度线会造成配制溶液浓度偏低
【答案】A
【解析】A.实验室没有80mL容量瓶,配制80mL溶液需要使用100mL容量瓶,故A正确;
B.需要称取NaOH的质量为1.00ml/Lx0.10Lx40g/ml=4.0g,故B错误;
C.NaOH溶于水放出热量,在小烧杯中稀释后,需要冷却至室温再转移到容量瓶中,故C错误;
D.定容时,俯视刻度线会造成配制溶液体积偏小,溶液浓度偏高,故D错误;
故选A。
13.(2023上·辽宁丹东·高一统考期中)下列关于离子检验的说法正确的是
A.取少量样液,加入溶液,若溶液变红,证明样液中含
B.取少量样液,加入硝酸酸化的溶液,若产生白色沉淀,证明样液中含
C.取少量样液,加入稀盐酸,若产生能使澄清石灰水变浑浊的气体,证明样液中含
D.用洁净的铂丝蘸取样液,在酒精灯外焰上灼烧,若火焰呈黄色,证明样液中含,不含
【答案】B
【解析】A.Fe3+遇KSCN变为红色,故A错误;
B.向某溶液中加入硝酸酸化的硝酸银溶液有白色沉淀出现,白色沉淀为AgCl,则原溶液含,故B正确;
C.向某无色溶液中加入盐酸产生能使澄清石灰水变浑浊的气体,产生的无色气体可能为二氧化碳或二氧化硫,则溶液中可能含有、、、等,故C错误;
D.观察钾的焰色试验应该透过蓝色钴玻璃,故D错误;
故选B。
14.(2023上·广东汕头·高一统考期中)在澄清透明的酸性溶液中。下列离子能共存的是
A.、、、
B.、、、
C.、、、
D.、、、
【答案】A
【解析】A.澄清透明的酸性溶液中,、、、均可大量共存,A正确;
B.澄清透明的酸性溶液中,、会氧化、,故不能大量共存,B错误;
C.澄清透明的酸性溶液中,不能大量存在,C错误;
D.澄清透明的酸性溶液中,会结合氢离子生成弱电解质醋酸,D错误;
故选A。
15.(2023下·广东东莞·高一统考期末)铝热反应可冶炼金属铁:,能量变化如图所示,下列说法正确的是
A.铝热反应也可用于冶炼金属Mg
B.工业上常用电解熔融Al2O3制备铝单质
C.铝热反应需要高温条件,故铝热反应为吸热反应
D.能量变化必然伴随化学反应发生
【答案】B
【解析】A.镁的活泼性比铝强,不能用铝热反应冶炼金属Mg,A错误;
B.工业上常用电解熔融Al2O3制备铝单质,B正确;
C.铝热反应需要高温条件,但铝热反应为放热反应,C错误;
D.能量变化不一定伴随化学反应发生,如浓硫酸稀释过程放热,但并没有化学反应发生,D错误;
故选B。
16.(2023下·北京东城·高一统考期末)关于元素周期律的应用,下列推测合理的是
A.根据硝酸属于强酸,预测磷酸也属于强酸
B.根据氯的非金属性强于硫,预测盐酸的酸性强于硫酸
C.根据钾的金属性强于钠,预测钾与水的反应比钠与水的反应更容易
D.根据溴水能和碘化钾溶液发生反应,预测溴水也能和氯化钾溶液反应
【答案】C
【解析】A.同主族元素从上至下非金属性逐渐减弱,元素的非金属性越强,其最高价氧化物的水化物的酸性越强,氮的非金属性强于磷,则硝酸的酸性强于磷酸,硝酸属于强酸,磷酸属于中强酸,故A错误;
B.元素的非金属性越强,其最高价氧化物的水化物的酸性越强,根据氯的非金属性强于硫,预测高氯酸的酸性强于硫酸,故B错误;
C.元素的金属性越强,越容易和水(或酸)反应,根据钾的金属性强于钠,预测钾与水的反应比钠与水的反应更容易,故C正确;
D.同主族元素从上至下非金属性逐渐减弱,氯的非金属性强于溴,所以溴水不能和氯化钾溶液反应,故D错误,
故选C。
17.(2023上·辽宁大连·高一校考期中)探究铁及其化合物的性质,下列方案设计、现象和结论都正确的是
【答案】D
【解析】A.往FeCl2溶液中加入Cu片,铜活泼性小于铁,二者不能发生反应,故A错误;
B.往FeCl3溶液中滴加KSCN溶液,再加入少量KCl固体,溶液先变成红色,后不会变浅,KCl电离出的氯离子和钾离子不参与反应,KCl固体也不会稀释溶液,故B错误;
C.铁锈的成分为Fe2O3,用盐酸浸泡带有铁锈的铁钉生成Fe3+离子,再与铁反应生成Fe2+离子,滴加K3[Fe(CN)6]溶液生成蓝色沉淀,故C错误;
D.向沸水中逐滴加5~6滴饱和FeCl3溶液,持续煮沸,液体先变成红褐色,形成胶体,然后析出红褐色沉淀,胶体发生聚沉,故D正确;
故选D。
18.(2023下·安徽亳州·高一亳州二中校考期末)我国科学家分析月壤成分发现含有X、Y、Z、W、M五种主族元素,其原子序数依次增大且都不大于20,Y、Z、W同周期且Z、M同主族;X与W形成的化合物是光导纤维的基本原料,在潜水艇中Y2X2可以用作供氧剂。下列说法正确的是
A.离子半径的大小顺序:Z>Y>X
B.最简单气态氢化物稳定性X>W
C.最高价氧化物对应水化物碱性Y>Z>M
D.化合物Y2X2中只有离子键
【答案】B
【分析】我国科学家分析月壤成分发现含有X、Y、Z、W、M五种主族元素,其原子序数依次增大且都不大于20,Y、Z、W同周期;X与W形成的化合物是光导纤维的基本原料,则X为O,W为Si,在潜水艇中Y2X2可以用作供氧剂,则Y为Na,Z、M同主族,则Z为Mg,M为Ca。
【解析】A.根据同电子层结构核多径小,则离子半径的大小顺序:X >Y>Z,故A错误;
B.氧的非金属性比硅非金属性强,则最简单气态氢化物稳定性X>W,故B正确;
C.同周期从左到右金属性逐渐减弱,同主族从上到下金属性逐渐增大,金属性越强,其最高价氧化物对应水化物的碱性越强,因此最高价氧化物对应水化物碱性M>Y>Z,故C错误;
D.化合物Y2X2(Na2O2)中有离子键、非极性键,故D错误。
故选B。
二、非选择题:本题共4小题,共46分。
19.(2023上·福建泉州·高一校考期中)(12分)回答下列问题:
I.双氧水和84消毒液是生活中常用的两种消毒剂。
(1)某同学设计如下实验研究的性质,能证明有还原性的实验是 (填序号)。
(2)某届奥运会期间,由于工作人员将84消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种原因可能是NaClO与反应产生促进藻类快速生长。
该反应说明氧化性:NaClO (填“>”或“<”),当参加反应的NaClO和的物质的量之比为1∶1时,该反应的还原产物为 。
Ⅱ.高铁酸钠()(其中氧元素是-2价)是一种新型的净水剂,可以通过下述反应制取:
(3)①用双线桥法在化学方程式中标出电子转移的情况。
②请完成方程式的配平:
Ⅲ.汽车剧烈碰撞时,安全气囊中发生反应。
(4)若氧化产物比还原产物多1.75 ml,则转移的电子数为 (为阿伏加德罗常数的值),被氧化的N原子的物质的量为 。
【答案】(1)1
(2)> NaCl
(3)
(4) 1.25NA 3.75ml
【解析】(1)实验1,过氧化氢将酸性高锰酸钾还原自身被氧化生成氧气,体现还原性;实验2过氧化氢将碘离子氧化为碘单质,体现氧化性;
(2)过氧化氢中的氧元素由-1价被氧化为0价做还原剂,则次氯酸钠做氧化剂,可以得出次氯酸钠的氧化性强于过氧化氢;由可知当参加反应的NaClO和的物质的量之比为1∶1时,该反应的还原产物为NaCl;
(3)在反应中,铁元素从+3价被氧化到+6价,氯元素由+1价被还原为-1价,则双线桥为,根据得失电子守恒可以配平:;
(4)10mlNaN3和2mlKNO3参加反应,则生成的16mlN2中有15ml N2由NaN3被氧化而来是氧化产物,1ml N2由KNO3被还原而来是还原产物,氧化产生物比还原产物多14ml,此时转移电子数为10NA,则有,可求得、。
20.(2023上·安徽安庆·高一校考期中)(10分)现有mg某X2气体,它的摩尔质量为Mg/ml,阿伏伽德罗常数用NA表示,则:
(1)该气体的物质的量为 ml。
(2)一个X原子的质量为 g。
(3)该气体在标准状况下的体积为 L。
(4)相同状况下,若X2与氮气以体积比为1:4混合,该混合气体相对氢气密度为14.4,则X2的相对分子质量为 。
(5)若标准状况下X2的密度为1.25g/L,则X原子最外层有 个电子。
【答案】(1)
(2)
(3)
(4)32
(5)5
【解析】(1)mg该气体的物质的量=ml;
(2)设该气体为1ml,则一个分子的质量为g,而该分子是双原子分子,故一个X原子质量=g;
(3)标况下,该气体的体积==L;
(4)相同状况下,若X2与氮气以体积比1:4混合,则X2与氮气的物质的量比为1:4,由于气体的密度之比等于其相对分子质量之比,则混合气体的平均相对分子质量为14.4×2=28.8,混合气体的平均摩尔质量=,解得M=32g/ml,X2的相对分子质量为32;
(5)若标况下X2的密度为1.25 g/L,X2的摩尔质量=1.25 g/L×22.4L/ml=28g/ml,X的相对原子质量为14,猜测为氮原子,氮原子最外层电子数为5。
21.(2023上·湖南株洲·高一校考期末)某学习小组为认识铁及其化合物的性质和分散系的性质做了如下一系列综合实验。运用所学知识,回答下列问题:
(1)可利用 来区分胶体和溶液。
(2)向盛有溶液的试管中滴加溶液,请描述发生的现象 。
(3)铁粉与水蒸气在高温条件下反应的化学方程式是 。
(4)电子工业中,人们常用溶液腐蚀覆铜板来制作印刷电路板。现欲配制溶液,回答下列问题:
①配制该溶液时所需玻璃仪器除烧杯、玻璃棒、胶头滴管、量筒外,还需 。
②使用托盘天平称量的质量为 g。
③定容时,若仰视容量瓶刻度线会使配制的溶液浓度 (填“偏大”“偏小”或“不变”)。
(5)实验室模拟用溶液腐蚀铜板并从废液中回收和溶液流程如图所示:
①请写出溶液与铜反应的离子方程式 。
②试剂在反应中体现 (填“氧化性”或“还原性”)。
③Z可选用的试剂有 (填序号)。
A.硝酸 B.酸性高锰酸钾溶液 C.过氧化氢 D.氯气
【答案】(1)丁达尔效应
(2)先生成白色絮状沉淀,沉淀迅速变为灰绿色,最终变为红褐色
(3)3Fe+4H2O(g)Fe3O4+4H2
(4) 100mL容量瓶 3.25 偏小
(5) 2Fe3++Cu=Cu2++2Fe2+ 还原性 CD
【分析】小问(5)中氯化铁与铜反应生成含有亚铁离子和铜离子的废液,废液中加入过量的Fe,Fe和铜离子反应生成亚铁离子和铜,滤渣中含有Cu和过量的Fe,再加入过量HCl,Fe与HCl反应生成FeCl2,过滤得到铜,FeCl2与之前的滤液合并加入Cl2生成FeCl3重新利用。
【解析】(1)氢氧化铁胶体具有丁达尔效应,而氯化铁溶液没有,可利用丁达尔效应区分氢氧化铁胶体和氯化铁溶液。
(2)向硫酸亚铁溶液中滴加NaOH溶液,亚铁离子与氢氧根离子反应生成白色的氢氧化亚铁沉淀,氢氧化亚铁立即被氧化生成红褐色的氢氧化铁沉淀,现象为先生成白色絮状沉淀,沉淀迅速变为灰绿色,最终变为红褐色。
(3)铁粉与水蒸气在高温条件下反应生成四氧化三铁和氢气,反应的化学方程式为3Fe+4H2O(g)Fe3O4+4H2。
(4)①配制80mL0.2ml/L的FeCl3溶液,需要使用100mL的容量瓶,故还需要的玻璃仪器为100mL容量瓶。
②100mL0.2ml/L的FeCl3的物质的量为0.02ml,FeCl3的质量为0.02ml×162.5g/ml=3.25g。
③定容时仰视容量瓶刻度线,导致溶液的体积偏大,所配制的FeCl3的浓度偏小。
(5)①FeCl3溶液与铜反应,铁离子与铜反应生成亚铁离子和铜离子,反应的离子方程式为2Fe3++Cu=Cu2++2Fe2+。
②根据分析可知,试剂X为Fe,Fe与Cu2+反应生成Fe2+和Cu,Fe在反应中失电子体现还原性。
③Z的主要作用为将亚铁离子氧化成铁离子,同时不能引入新的杂质。
A.硝酸可将亚铁离子氧化成铁离子,但是引入了新的杂质,A错误;
B.酸性高锰酸钾可将亚铁离子氧化成铁离子,但是引入了杂质Mn2+,B错误;
C.过氧化氢可将亚铁离子氧化成铁离子,同时没有引入新杂质,C正确;
D.氯气可将亚铁离子氧化成铁离子,同时没有引入新杂质,D正确;
故选CD。
22.(2023上·黑龙江牡丹江·高一校考期末)(12分)下表列出了①~⑩十种元素在周期表中的位置:
请按要求回答下列问题:
(1)上述元素中,金属性最强的是 (填元素名称),最高价氧化物对应水化物酸性最强的是 (写出酸的化学式)。
(2)由④、⑤、⑦、⑧四种元素形成的简单离子半径由大到小的顺序是: 。(用离子符号表示)
(3)由元素③形成的单质的电子式为 ,由元素⑥和⑨形成化合物乙,请用电子式表示物质乙的形成过程 。
(4)由元素①、③、④、⑧形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为 。
(5)请用一个化学方程式证明元素⑧和⑨的非金属性强弱关系 。
(6)可以比较⑤、⑥两元素金属性强弱的实验是_________。
A.比较这两种元素最高价氧化物对应的水化物的碱性
B.将⑤的单质投入到⑥的盐溶液中
C.将这两种元素的单质分别放入冷水中
D.比较这两种元素的单质与酸反应时失电子的数目
【答案】(1)钾
(2)
(3)
(4)
(5)
(6)AC
【分析】由元素在周期表的位置可知,①~⑩分别为H、C、N、O、Na、Mg、Al、S、Cl、K;
【解析】(1)同一周期从左到右金属性逐渐减弱,同一主族从上到下金属性逐渐增强,金属性最强的是钾;非金属越强,最高价氧化物对应的水化物的酸性越强,非金属性最强的是氧,其次是氯,但是氧无正价,所以最高价氧化对应的水化物酸性越强的HClO4;
(2)④、⑤、⑦、⑧分别为O、Na、Al、S,对应的离子分别为O2-、Na+、Al3+、S2-,半径比较先看层数,层数越多半径越大,O2-、Na+、Al3+为2层,S2-为三层,层数一样,核内质子数越多半径越小,简单离子半径由大到小的顺序是:;
(3)由元素③形成的单质为氮气,氮气分子中存在氮氮叁键,电子式为;由元素⑥和⑨形成化合物乙为氯化镁,氯化镁是由氯离子和镁离子构成的化合物,电子式表示物质乙的形成过程为;
(4)由元素氢、氮、氧、硫形成的一种离子化合物,其水溶液显强酸性,则为酸式盐硫酸氢铵,该化合物的化学式为;
(5)非金属性强的元素单质能生成非金属性较弱的单质,二者非金属性比较可以通过单质间的置换反应来比较,,故反应可以为:;
(6)金属性越强对应最高价氧化物对应的水化物的碱性越强,金属性Na大于Mg,氢氧化钠的碱性强于氢氧化镁,A项符合题意;将Na的单质投入到镁的盐溶液中,钠直接与水反应生产氢氧化钠和氢气,生成的氢氧化钠和镁离子生成氢氧化镁沉淀,不能表明金属性强弱,B项不符合题意;可以根据与水反应的难易或剧烈程度比较,C项符合题意;金属性强弱与失去电子难易有关,与失去电子数目多少无关,D项不符合题意;故选AC。
选项
碱性氧化物
非电解质
混合物
纯净物
A
血液
液氯
B
空气
C
乙醇
浓硫酸
盐酸
D
胶体
A.制备无水氯化铁
B.配制一定物质的量浓度的硫酸溶液
C.配制一定物质的量浓度的溶液
D.比较 和的热稳定性大小
实验方案
现象
结论
A
往FeCl2溶液中加入Cu片
溶液逐渐变蓝
Fe2+的氧化能力比Cu2+强
B
往FeCl3溶液中滴加KSCN溶液,再加入少量KCl固体
溶液先变成红色,后红色变浅
KCl稀释了溶液,红色变浅
C
用盐酸浸泡带有铁锈的铁钉,滴加K3[Fe(CN)6]溶液
有特征蓝色沉淀
铁锈的主要成分为FeO
D
向沸水中逐滴加5~6滴饱和FeCl3溶液,持续煮沸
液体先变成红褐色,然后析出红褐色沉淀
Fe3+先水解得Fe(OH)3胶体,再聚集成Fe(OH)3沉淀
序号
实验
实验现象
1
向5%溶液中滴加酸性溶液
a.溶液紫色褪去;b.有大量气泡产生
2
向5%溶液中滴加淀粉碘化钾溶液
c.溶液变蓝
族周期
ⅠA
0
1
①
ⅡA
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
2
②
③
④
3
⑤
⑥
⑦
⑧
⑨
4
⑩
【寒假作业】(人教版2019)高中化学 高一寒假巩固提升训练 预习检测卷-练习.zip: 这是一份【寒假作业】(人教版2019)高中化学 高一寒假巩固提升训练 预习检测卷-练习.zip,文件包含寒假作业人教版2019高中化学高一寒假巩固提升训练预习检测卷原卷版docx、寒假作业人教版2019高中化学高一寒假巩固提升训练预习检测卷解析版docx等2份试卷配套教学资源,其中试卷共26页, 欢迎下载使用。
【寒假作业】(人教版2019)高中化学 高一寒假巩固提升训练 第08讲 乙醇与乙酸-练习.zip: 这是一份【寒假作业】(人教版2019)高中化学 高一寒假巩固提升训练 第08讲 乙醇与乙酸-练习.zip,文件包含寒假作业人教版2019高中化学高一寒假巩固提升训练第08讲乙醇与乙酸原卷版docx、寒假作业人教版2019高中化学高一寒假巩固提升训练第08讲乙醇与乙酸解析版docx等2份试卷配套教学资源,其中试卷共29页, 欢迎下载使用。
【寒假作业】(人教版2019)高中化学 高一寒假巩固提升训练 第02讲 氮及其化合物-练习.zip: 这是一份【寒假作业】(人教版2019)高中化学 高一寒假巩固提升训练 第02讲 氮及其化合物-练习.zip,文件包含寒假作业人教版2019高中化学高一寒假巩固提升训练第02讲氮及其化合物原卷版docx、寒假作业人教版2019高中化学高一寒假巩固提升训练第02讲氮及其化合物解析版docx等2份试卷配套教学资源,其中试卷共36页, 欢迎下载使用。