
第30讲 化学反应速率与限度(含解析)-2024年江苏省普通高中学业水平合格性考试复习
展开1.化学反应速率是表示化学反应过程进行 的物理量。
通常用单位时间内反应物 或生成物 来表示。
单位: 或 。
根据定义可知道计算公式v= = ,只取正值。
化学反应速率之比= 。
2.影响化学反应速率的因素
(1)内因: 。
(2)外界条件:
①增大反应物的浓度,反应速率 ;
②有气体参加的反应,增大压强,反应速率 ;
③升高温度(任何反应,无论吸热还是放热),反应速率 ;
④使用(正)催化剂,反应速率 ;
⑤其他:增大反应物接触面积,反应速率 ;形成原电池后,反应速率 。
3.可逆反应
(1)定义:在同一条件下,既能向 方向进行,同时又能向 方向进行的反应,叫做可逆反应。
(2)特点:各反应物、生成物同时存在,反应不能进行到底。可逆反应有一定限度,反应物不可能 转化为生成物,即反应物的转化率不可能是 。
4.化学反应限度标志
(1)正反应速率与逆反应速率 但不等于 。
(2)混合体系中各组分的浓度 。
【激活思维】
问题1:能加快化学反应速率的措施有哪些?
问题2:可逆反应达到平衡时,表示反应停止,且反应物已完全转化为生成物?
@真题回放
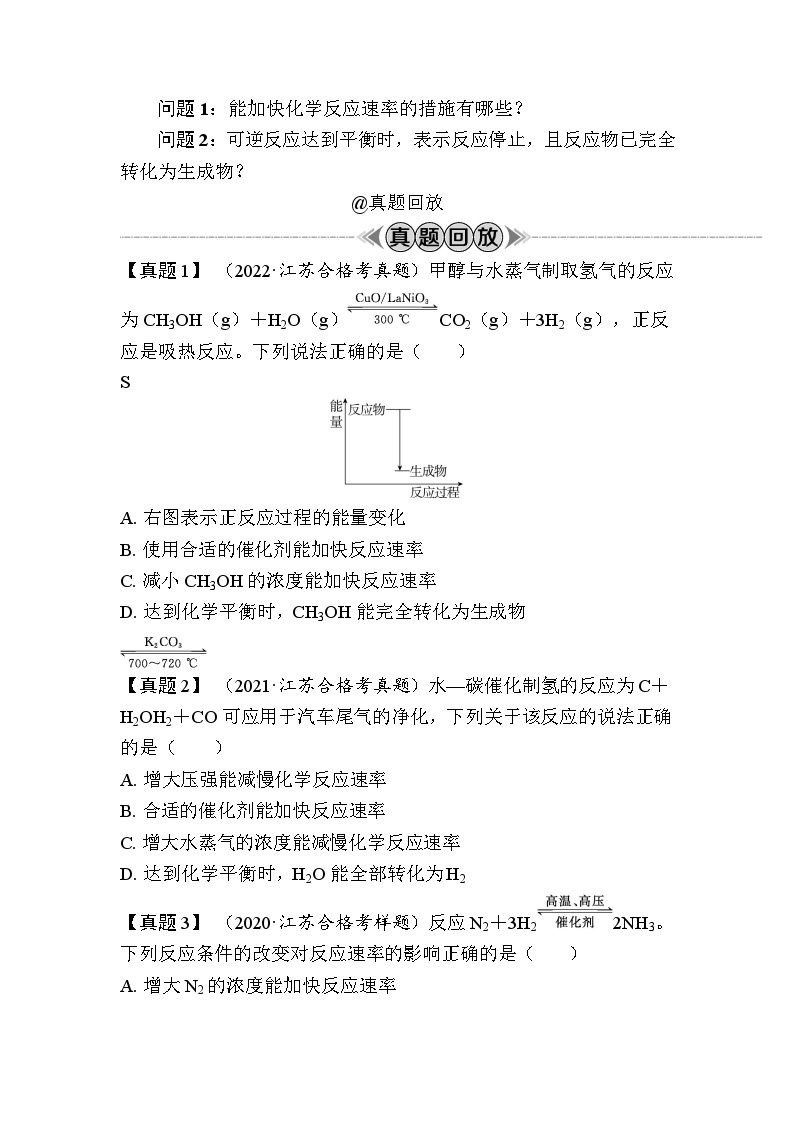
【真题1】 (2022·江苏合格考真题)甲醇与水蒸气制取氢气的反应为CH3OH(g)+H2O(g)CO2(g)+3H2(g),正反应是吸热反应。下列说法正确的是( )
S
A.右图表示正反应过程的能量变化
B.使用合适的催化剂能加快反应速率
C.减小CH3OH的浓度能加快反应速率
D.达到化学平衡时,CH3OH能完全转化为生成物
【真题2】 (2021·江苏合格考真题)水—碳催化制氢的反应为C+H2OH2+CO可应用于汽车尾气的净化,下列关于该反应的说法正确的是( )
A.增大压强能减慢化学反应速率
B.合适的催化剂能加快反应速率
C.增大水蒸气的浓度能减慢化学反应速率
D.达到化学平衡时,H2O能全部转化为H2
【真题3】 (2020·江苏合格考样题)反应N2+3H22NH3。下列反应条件的改变对反应速率的影响正确的是( )
A.增大N2的浓度能加快反应速率
B.减小H2的浓度能加快反应速率
C.升高温度能减慢反应速率
D.添加催化剂对反应速率无影响
【真题4】 (2020·江苏学测合格考)反应2NO+2CON2+2CO2可应用于汽车尾气的净化,下列关于该反应的说法正确的是( )
A.升高温度能减慢反应速率
B.减小CO浓度能加快反应速率
C.使用恰当的催化剂能加快反应速率
D.达到化学平衡时,NO能100%转化为产物
【真题5】 (2019·江苏学测合格考)CO2+4H2CH4+2H2O是CO2综合利用的一种方法。下列关于该反应的说法正确的是( )
A.适当升温能加快反应速率
B.催化剂对反应速率无影响
C.达到平衡时,正反应速率为0
D.达到平衡时,CO2能100%转化为CH4
@过关检测
1.(2023·铜山合格考模拟)下列反应条件的改变对3Cl2+8NH3N2+6NH4Cl反应速率的影响正确的是( )
A.增大Cl2的浓度能加快反应速率
B.减小N2的浓度能加快反应速率
C.降低温度能加快反应速率
D.及时将生成的NH4Cl移出可加快反应速率
2.(2023·盐城合格考模拟)反应2NO2(g)N2O4(g)在一定体积的密闭容器中进行。下列说法正确的是( )
A.升高温度能减慢反应速率
B.减小NO2浓度能加快反应速率
C.缩小反应容器的体积能加快反应速率
D.达到化学平衡状态时,NO2全部转化为N2O4
3.(2023·南京六校合格考模拟)H2和CO2反应生成H2O和CH4的反应为4H2 +CO22H2O+CH4。下列关于该反应的说法正确的是( )
A.合适的催化剂能加快反应速率
B.适当升高温度会减慢化学反应速率
C.增大CO2的浓度能减慢化学反应速率
D.达到化学平衡时,CO2能全部转化为CH4
4.(2023·连云港合格考模拟)氯气与水反应的化学方程式为Cl2+H2OHCl+HClO,可用于自来水消毒。下列关于该反应的说法正确的是( )
A.升高温度能减慢反应速率 B.增大Cl2的浓度能加快反应速率
C.增大压强,对该反应的速率没有影响 D.达到化学平衡时,Cl2能100%转化
5.(2023·南京合格考模拟)关于反应6NO+4NH35N2+6H2O,下列说法正确的是( )
A.升高温度能够加快反应速率
B.降低NO浓度能够加快反应速率
C.使用催化剂不影响反应的速率
D.加入足量的NH3可以使NO 100%转化为N2
6.(2023·如皋合格考模拟)关于合成氨反应(N2+3H22NH3),下列说法正确的是( )
A.增加N2的浓度能加快反应速率
B.降低体系温度能加快反应速率
C.使用催化剂不影响反应速率
D.若反应在密闭容器中进行,N2和H2能100%转化为NH3
7.(2023·沛县合格考模拟)对于反应Cl2+H2OHCl+HClO,下列说法正确的是( )
A.增大压强,能使Cl2完全转化为盐酸和次氯酸
B.降低温度能增大反应速率
C.平衡时,仍有Cl2和H2O反应生成HCl和HClO
D.增加Cl2的浓度可能降低反应速率
8.(2023·海安合格考模拟)下列关于SO2催化氧化生成SO3的反应:2SO2(g)+O2(g)2SO3(g)的说法正确的是( )
A.降低温度能加快反应速率
B.减小SO2的浓度能加快反应速率
C.使用V2O5作催化剂同时增大正、逆反应的速率
D.2 ml SO2和1.5 ml O2通过接触室,可生成2 ml SO3
9.(2023·如皋合格考模拟)对于放热反应2SO2+O22SO3,下列说法正确的是( )
A.升高温度可以提高反应速率 B.断开O2中的氧氧键放出能量
C.反应物的总能量小于生成物的总能量 D.增大O2的浓度能使SO2完全转化
10.(2023·扬州合格考模拟)关于反应CO(g)+H2O(g)CO2(g)+H2(g)的说法正确的是( )
A.减小H2O(g)浓度能加快反应速率
B.使用Fe2O3/Au催化剂可加快反应的速率
C.使用Fe2O3/Au催化剂可实现原料的100%转化
D.达到化学平衡时,正、逆反应的速率为0
11.(2023·扬州合格考模拟)一定温度下,向某恒容密闭容器中充入2 ml SO2和1 ml O2,在催化剂作用下发生反应:2SO2(g)+O2(g)2SO3(g),下列说法正确的是( )
A.使用催化剂可实现SO2的100%转化
B.以SO2或O2浓度的变化均可表示反应速率,两者的数值相等
C.达到平衡状态时,SO2与SO3物质的量之比为1∶1
D.达到平衡状态时,SO2的浓度不再发生变化
12.(2022·沛县合格考模拟)臭氧是理想的烟气脱硝剂,其脱硝反应为2NO2(g)+O3(g)N2O5(g)+O2(g)。下列有关说法正确的是( )
A.增大压强可增大反应速率 B.升高温度可减小反应速率
C.达到平衡时,v(正)=v(逆)=0 D.达到平衡时,NO2转化率为100%
13.(2022·盐城合格考模拟)工业上H2可以发生反应:CO+2H2CH3OH,下列有关说法不正确的是( )
A.增大H2的浓度,可加快反应速率 B.使用合适催化剂,可加快反应速率
C.达到平衡时,正反应速率与逆反应速率相等 D.达到平衡时,CO可以完全转化
14.(2022·扬州合格考模拟)关于碘蒸气与氢气反应:I2+H22HI,下列说法错误的是( )
A.使用合适的催化剂可以加快反应速率 B.升高温度可以增大反应速率
C.增大I2浓度可以使H2转化率达到100% D.增大I2浓度可以增大反应速率
15.(2022·扬州合格考模拟)CO2(g)+3H2(g)CH3OH(g)+H2O(g)是CO2综合利用的一种方法。下列关于该反应的说法正确的是( )
A.升高温度能加快反应速率
B.催化剂对反应速率无影响
C.减小H2浓度能加快反应速率
D.达到化学平衡时,CO2能100%转化为CH3OH
16.(2021·盐城合格考模拟)工业制备硫酸过程中存在如下反应:2SO2+O22SO3。下列关于该反应的说法错误的是( )
A.一定条件下SO2能100%转化为SO3 B.升高温度能加快反应速率
C.使用合适的催化剂能加快反应速率 D.增大O2的浓度能加快反应速率
17.(2021·海安合格考模拟)某工厂的一种无害化处理反应为6NO+4NH35N2+6H2O。下列关于该反应的说法正确的是( )
A.增大NH3浓度能减慢反应速率 B.降低温度能加快反应速率
C.使用催化剂能加快反应速率 D.NO与NH3能100%转化为产物
第30讲 化学反应速率与限度
【考点填空】
1.快慢 浓度的减少 浓度的增加 ml/(L·s) ml/(L·min) 化学计量数之比
2.(1)反应物的性质
(2)①加快 ②加快 ③加快 ④加快 ⑤加快 加快
3.(1)正反应 逆反应 (2)完全 100%
4.(1)相等 零 (2)不变
问题1:增大浓度、升高温度、增大压强、加合适的催化剂、增大反应物接触面积、构成原电池。
问题2:错误。达到平衡时,反应仍在进行,只是v(正)=v(逆)。可逆反应中,反应物不可能完全转化为生成物,反应物的转化率达不到100%。
【真题回放】
1.B 解析:A项,正反应是吸热反应,则生成物的总能量大于反应物的总能量,与图示不吻合,错误;B项,催化剂可以加快反应速率,正确;C项,减小物质的浓度,减慢反应速率,错误;D项,可逆反应中,反应物不可能完全转化为生成物,错误。
2.B 解析:A项,对于有气体参加的反应,压强越大,反应速率越快,错误;B项,催化剂可以加快反应速率,正确;C项,增大反应物浓度,可以加快化学反应速率,错误;D项,该反应为可逆反应,反应物不可能完全转化为生成物,错误。
3.A 解析:A项,增大N2的浓度,化学反应速率加快,正确;B项,减小H2的浓度,反应速率减慢,错误;C项,升温,反应速率加快,错误;D项,催化剂会改变反应速率,错误。
4.C 解析:A项,升高温度,反应速率加快,错误;B项,CO浓度减小,反应速率变慢,错误;C项,使用恰当的催化剂可以加快反应速率,正确;D项,可逆反应中,反应物的转化率不可能达到100%,错误。
5.A 解析:A项,温度越高,反应速率越快,正确;B项,正催化剂可以加快反应速率,错误;C项,达到平衡的可逆反应,反应并没有停止,只是正、逆反应速率相等,错误;D项,可逆反应中,反应物不可能完全转化为生成物,即反应物的转化率达不到100%,错误。
【过关检测】
1.A 解析:A项,其他条件不变,增大反应物氯气的浓度可以加快反应速率,正确;B项,减小生成物氮气的浓度,反应速率减慢,错误;C项,温度降低,反应速率减慢,错误;D项,移走产物,产物浓度减小,反应速率减慢,错误。
2.C 解析:A项,温度越高,反应速率越快,错误;B项,浓度减小,反应速率变慢,错误;C项,缩小容器的体积,即为增大压强,可以加快反应速率,正确;D项,可逆反应中,反应物不可能全部转化为生成物,错误。
3.A 解析:A项,催化剂可以加快反应速率,正确;B项,升温可以加快反应速率,错误;C项,增大浓度,可以加快反应速率,错误;D项,可逆反应中,反应物不可能完全转化为生成物,错误。
4.B 解析:A项,升温能加快反应速率,错误;B项,增大浓度可以加快反应速率,正确;C项,Cl2为气体,增大压强,可以加快反应速率,错误;D项,可逆反应中反应物的转化率不可能达到100%,错误。
5.A 解析:A项,升温可以加快反应速率,正确;B项,浓度减小,反应速率减慢,错误;C项,催化剂可以改变反应速率,错误;D项,可逆反应中,反应物的转化率不可能达到100%,错误。
6.A 解析:A项,增加浓度,会加快反应速率,正确;B项,降低温度,会减慢反应速率,错误;C项,催化剂可以加快反应速率,错误;D项,可逆反应中,反应物的转化率不可能达到100%,错误。
7.C 解析:A项,该反应为可逆反应,Cl2不可能完全转化为生成物,错误;B项,降温,反应速率减慢,错误;C项,可逆反应达到平衡时,反应物和产物均同时存在,正确;D项,增大反应物浓度,反应速率加快,错误。
8.C 解析:A项,温度升高,反应速率加快,错误;B项,反应物浓度减小,反应速率变慢,错误;C项,催化剂可以加快正反应和逆反应的速率,正确;D项,2 ml SO2不可能完全转化为2 ml SO3,错误。
9.A 解析:A项,升温可以加快反应速率,正确;B项,断开化学键,需要吸收能量,错误;C项,放热反应中反应物的能量大于生成物的能量,错误;D项,可逆反应中,反应物不可能完全转化,错误。
10.B 解析:A项,减小反应物浓度,反应速率减慢,错误;B项,催化剂可以加快反应速率,正确;C项,可逆反应即使加入催化剂,也不能使反应物的转化率达到100%,错误;D项,达到平衡时,正、逆反应速率相等,但不等于0,反应仍在进行中,错误。
11.D 解析:A项,可逆反应中,反应物的转化率不可能达到100%,错误;B项,SO2和O2的速率之比为2∶1,错误;C项,平衡状态时,SO2与SO3的物质的量之比无法确定,因为SO2的转化率是不确定的,错误;D项,平衡状态时,各组分的浓度不再变化,显然SO2的浓度也将不再改变,正确。
12.A 解析:A项,压强越大,反应速率越快,正确;B项,升高温度,反应速率加快,错误;C项,平衡时,反应没有停止,v(正)=v(逆)≠0,错误;D项,可逆反应中,反应物不可能完全反应,则转化率达不到100%,错误。
13.D 解析:A项,增大反应物浓度,反应速率加快,正确;B项,使用催化剂可以加快反应速率,正确;C项,平衡时,v(正)=v(逆),正确;D项,可逆反应中,反应物不可能完全转化为生成物,错误。
14.C 解析:A项,合适的催化剂可以加快反应速率,正确;B项,升高温度可以加快反应速率,正确;C项,可逆反应中,反应物的转化率达不到100%,错误;D项,增大浓度,可以加快反应速率,正确。
15.A 解析:A项,升温可以加快反应速率,正确;B项,催化剂可以改变反应速率,错误;C项,减小反应物浓度,可以减慢反应速率,错误;D项,可逆反应中反应物不可能完全转化为生成物,错误。
16.A 解析:A项,可逆反应中,反应物不可能完全转化为生成物,错误;升温、使用催化剂、增大浓度均可以加快反应速率。
17.C 解析:A项,增大NH3浓度,反应速率加快,错误;B项,降低温度,反应速率减慢,错误;C项,催化剂可以加快反应速率,正确;D项,可逆反应中,反应物不可能完全转化为生成物,错误。
第6讲 离子共存(含解析)-2024年江苏省普通高中学业水平合格性考试复习: 这是一份第6讲 离子共存(含解析)-2024年江苏省普通高中学业水平合格性考试复习,共8页。试卷主要包含了复分解反应,发生氧化还原反应,生成配合物等内容,欢迎下载使用。
第2讲 分散系(含解析)-2024年江苏省普通高中学业水平合格性考试复习: 这是一份第2讲 分散系(含解析)-2024年江苏省普通高中学业水平合格性考试复习,共5页。试卷主要包含了胶体的应用等内容,欢迎下载使用。
第32讲 乙醇 乙酸(含解析)-2024年江苏省普通高中学业水平合格性考试复习: 这是一份第32讲 乙醇 乙酸(含解析)-2024年江苏省普通高中学业水平合格性考试复习,共11页。试卷主要包含了乙醇,乙酸等内容,欢迎下载使用。