




【期中真题】福建省厦门双十中学2022-2023学年高三上学期期中考试化学试题.zip
展开厦门双十中学2023届高三上学期期中考试
化学试题
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.请认真阅读答题卡上的注意事项,不得用规定以外的笔和纸答题,不得在答题卡上做任何标记。
3.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其他答案标号。
4.考试结束后,将答题卡交回。
可能用到的相对原子质量:H-1 B-11 C-12 N-14 O-16 F-19 Na-23 Mg-24 S-32 Cl-35.5 As-75
一、选择题:本题共10小题,每小题4分,共40分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1. 下列说法合理的是
A. NaOH能促进油脂水解,可用含NaOH的洗涤剂去除人体皮肤表面的油性物质
B. 新冠肺炎抗疫中使用的干雾过氧化氢空气消毒机,利用了过氧化氢的氧化性
C. 工业生产中常把原料粉碎成小颗粒,可以提高原料的平衡转化率
D. 增大氮肥、磷肥、钾肥使用量,不会改变生态平衡且能提高农作物产量
2. NA为阿伏伽德罗常数的值。下列说法正确的是
A. 12gNaHSO4晶体中阴离子所带电荷数为0.1NA
B. 标准状况下,2.24LCHCl3中含有共价键的数目为0.4NA
C. 1LpH=13的Ba(OH)2溶液中Ba2+数目为0.1NA
D. 0.1molFeI2与0.1molCl2反应时转移电子的数目为0.3NA
3. 下列离子方程式与所述事实相符且正确的是
A. 用H2O2从酸化的海带灰浸出液中提取碘:2I-+H2O2+2H+=I2+2H2O
B. 向碳酸氢铵溶液中加入过量的NaOH溶液:NH+OH-=NH3•H2O
C. 向明矾溶液中加入Ba(OH)2溶液至生成沉淀的物质的量最多:Al3++2SO+2Ba2++4OH-=Al(OH)+2BaSO4↓
D. 等体积、等物质的量浓度的NaHCO3溶液与Ba(OH)2溶液混合:2HCO+Ba2++2OH-=BaCO3↓+2H2O+CO
4. 新冠肺炎疫情牵动人心,化学在对抗疫情中起到重要作用。已知短周期主族元素W、X、Y、Z的原子序数依次增大,W的最外层电子数等于电子层数等于原子序数,W与X形成的一种原子数比为1:1的液体是强力的氧化剂可用于杀菌消毒,YZX的水溶液是84消毒液的主要成分,Z的单质是一种黄绿色气体。下列说法不正确的是( )
A. X没有最高正价,但是有正价
B. W与X形成的化合物中绝对不含非极性共价键
C. Y单质的还原性是短周期里最强的
D. Z最高价氧化物水化物是一种具有强氧化性的强酸
5. 玻璃仪器内壁残留的硫单质可用热NaOH溶液洗涤除去,发生如下反应:
①3S+ 6NaOH2Na2S+ Na2SO3+ 3H2O
②(x-1)S+Na2SNa2Sx (x=2~6)
③S+ Na2SO3Na2S2O3
下列说法正确是
A. 反应①②③中,硫单质的作用相同
B. 反应①中,每消耗1 mol硫单质转移4 mol电子
C. 0.96g硫单质与amL2mol·L-1热NaOH溶液恰好完全反应,只生成Na2S和Na2SO3,则a= 60
D. 1.28 g硫单质与10 mL 2 mol·L-1热NaOH溶液恰好完全反应,只生成Na2Sx和Na2S2O3,则x=5
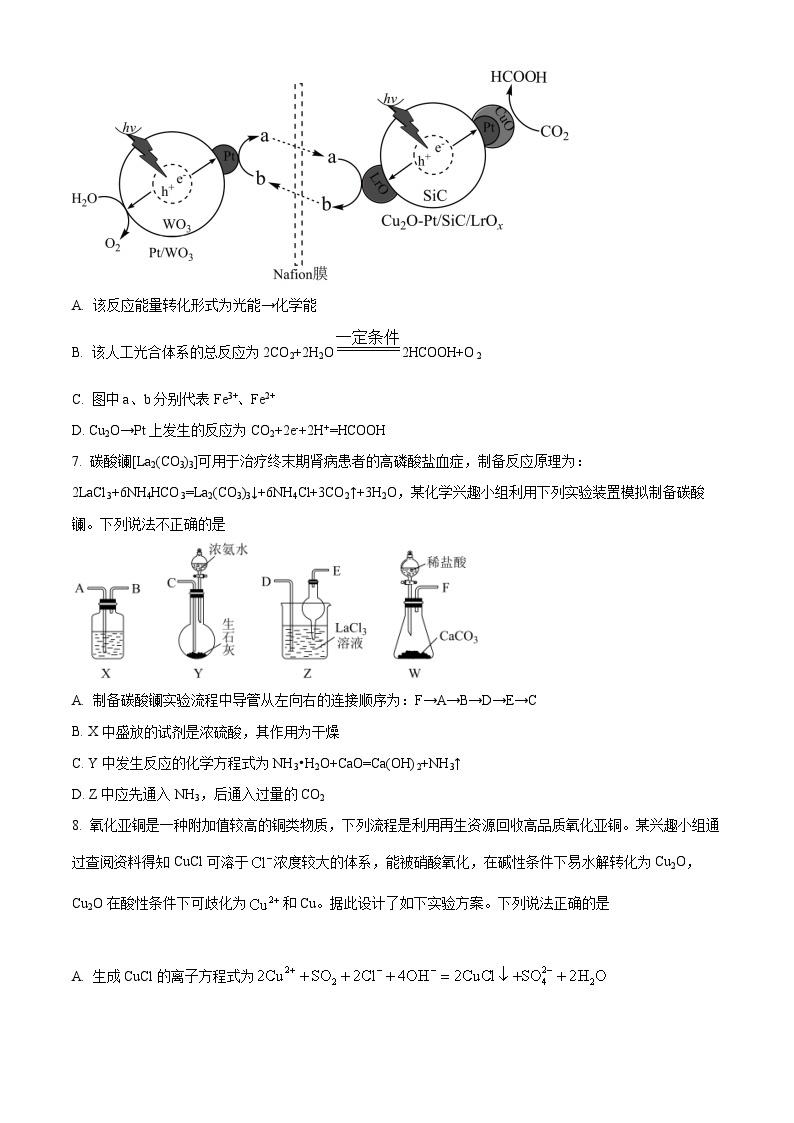
6. 科研人员通过控制光沉积的方法构建Cu2O-Pt/SiC/LrOx型复合材料光催化剂,然后以Fe2+和Fe3+离子渗透Nafion膜在酸性介质下构建了一个还原和氧化反应分离的人工光合体系,其反应机理如图。下列说法不正确的是
A. 该反应能量转化形式为光能→化学能
B. 该人工光合体系的总反应为2CO2+2H2O2HCOOH+O2
C. 图中a、b分别代表Fe3+、Fe2+
D. Cu2O→Pt上发生的反应为CO2+2e-+2H+=HCOOH
7. 碳酸镧[La2(CO3)3]可用于治疗终末期肾病患者的高磷酸盐血症,制备反应原理为:2LaCl3+6NH4HCO3=La2(CO3)3↓+6NH4Cl+3CO2↑+3H2O,某化学兴趣小组利用下列实验装置模拟制备碳酸镧。下列说法不正确的是
A. 制备碳酸镧实验流程中导管从左向右的连接顺序为:F→A→B→D→E→C
B. X中盛放的试剂是浓硫酸,其作用为干燥
C. Y中发生反应的化学方程式为NH3•H2O+CaO=Ca(OH)2+NH3↑
D. Z中应先通入NH3,后通入过量的CO2
8. 氧化亚铜是一种附加值较高的铜类物质,下列流程是利用再生资源回收高品质氧化亚铜。某兴趣小组通过查阅资料得知CuCl可溶于浓度较大的体系,能被硝酸氧化,在碱性条件下易水解转化为Cu2O,Cu2O在酸性条件下可歧化为和Cu。据此设计了如下实验方案。下列说法正确的是
A. 生成CuCl的离子方程式为
B. 为确保完全沉淀,应向含铜废液中加入过量的NaCl
C. 检验制得的Cu2O中是否含有CuCl,可用硝酸银和硝酸
D. 可直接向含铜废液中加入葡萄糖,在碱性条件下制得Cu2O
9. 已知:(HF)2(g)2HF(g) >0,平衡体系的总质量m(总)与总物质的量n(总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是
A. 温度:T1<T2
B. 反应速率:v(b)<v(a)
C. 平衡常数:K(a)=K(b)<K(c)
D. 当时,
10. 常温下对于任一电池反应aA+bB=cC+dD,其电动势E=Eθ-•lg,n为电池反应中转移的电子数。该小组同学设计装置(如图1),以Zn-Cu原电池探究离子浓度的改变对电极电势的影响。小组同学测得初始时Zn(s)+Cu2+(1mol•L-1)=Zn2+(1mol•L-1)+Cu(s) Eθ=1.1V(该反应n=2),随放电进行,观察电池电动势的变化趋势并绘制了电池电动势变化示意图(如图2)。下列说法正确的是
A. 电压表读数为零后,则说明该原电池中Cu2+已经消耗完全
B. 小组同学向ZnSO4和CuSO4溶液中同时快速加入少量相同体积和浓度的Na2S溶液,发现电池电动势突然减小,则可知:Ksp(ZnS)<Ksp(CuS)
C. 小组同学推测图2中直线与X轴的交点坐标大约为(37,0)
D. 小组同学推测若将初始时左侧1mol•L-1的Zn-ZnSO4半电池,换为2mol•L-1的CuSO4-Cu半电池,右侧半电池保持不变,则仍能观察到相同的电压表偏转情
二、填空题:本题包括5小题,共60分
11. 钯催化剂(主要成分为Pd、α-Al2O3,还含少量铁、铜等元素)在使用过程中,Pd易被氧化为难溶于酸的PdO而失活。一种从废钯催化剂中回收海绵钯的工艺流程如图。
(1)“还原i”加入甲酸的目的是还原______(填化学式)。
(2)“酸浸”过程:
①从绿色化学要求出发,酸浸液应选择_____(填标号)。
A.王水(浓硝酸和浓盐酸按体积比1:3混合)
B.盐酸和Cl2
C.盐酸和H2O2
②温度、固液比对浸取率的影响如图,则“酸浸”的最佳条件为_____。
(3)已知:
I.“离子交换”和“洗脱”可简单表示为:[PdCl4]2-+2RClR2PdCl4+2Cl-,(RCl为阴离子交换树脂)。
II.“沉钯”过程钯元素主要发生如下转化:H2PdCl4(稀溶液)→[Pd(NH3)4]Cl2(稀溶液)→[Pd(NH3)2]Cl2(沉淀)。
①“离子交换”流出液中阳离子有______(填离子符号)。
②淋洗液需保持pH小于2的原因是______。
(4)“还原ii”中产生无毒无害气体。由生成[Pd(NH3)2]Cl2海绵钯的化学方程式为_____。
(5)该工艺流程中可循环利用的物质有_____。
12. 镁条投入盐酸时,快速溶解并产生大量气泡;投入热水时,其表面会附着微量气泡。受此启发,某兴趣小组对Mg与NaHCO3溶液的反应进行了如表探究:
实验序号 | 实验操作 | 实验现象 |
1 | 向1.5mL1mol•L-1NaHCO3溶液中加入长3cm的镁条 | 持续快速产生大量气泡,溶液略显浑浊 |
I.探究反应产生的气体成分。
(1)经检验反应产生的气体有H2,实验室检验H2的方法为______。
(2)小组成员认为反应产生的气体中可能有CO2,并对此进行了如图实验(图1、图2中曲线②均为对应加入镁条的数据):
实验序号 | 实验操作 |
2 | 分别称取两份6.0mL1mol•L-1NaHCO3溶液于两个相同塑料瓶中(其中一个加入0.1g镁条),塞紧CO2,气体传感器,采集数据,各重复实验1次,得到图1所示曲线 |
3 | 分别称取两份30.0mL1mol•L-1NaHCO3溶液于两个相同烧杯中(其中一个加入1.1g镁条),插入pH传感器,搅拌并采集数据,得到图2所示曲线 |
图1中曲线②对应的CO2,含量逐渐增大的原因为______(用化学方程式表示);结合实验3解释,随着时间推移,图1中曲线②的数值低于曲线①的原因为______。
II.探究Mg与NaHCO3溶液反应比与热水反应快的原因。
小组成员推测可能是溶液中的Na+或HCO加快了该反应的发生,对比实验1设计实验如表:
实验序号 | 实验操作 | 实验现象 |
4 | 向______溶液中加入长3cm镁条 | 持续快速产生大量气泡,溶液略显浑浊 |
(3)结合实验1和4,可知溶液中的HCO加快了反应的发生。
①实验4中横线处内容为______。
②查阅文献可知,Mg(OH)2质地致密,MgCO3质地疏松,请结合必要的文字和化学用语解释HCO能加快该反应的原因为_____。
III.探究固体浑浊物的组成。
文献显示,固体浑浊物为Mg(OH)2和MgCO3的混合物。
(4)某同学设计了实验方案,测定混合物组成。实验测得固体浑浊物在热分解前后的质量分别为3.42g和2.00g,据此计算出固体浑浊物中n[Mg(OH)2]:n[MgCO3]=______。
13. 绿色能源的开发利用是未来能源发展的重要方向,也是实现“碳中和”目标的重要举措。氢能是重要的绿色能源,利用甲烷来制取氢气的总反应可表示为:CH4(g)+2H2O(g)CO2(g)+4H2(g),该反应可通过如下过程来实现:
反应I:CH4(g)+H2O(g)3H2(g)+CO(g) △H1=+206.3kJ•mol-1
反应II:CO(g)+H2O(g)CO2(g)+H2(g) △H2=-41.2kJ•mol-1
(1)总反应的△H=______kJ•mol-1
(2)在恒温的刚性容器中,发生上述反应,测得一段时间后,CH4转化率变化如图所示,请解释温度升高转化率变化的原因是______。
(3)在恒容条件下发生上述反应,不同进气比[n(CH4):n(H2O)]和不同温度时测得相应的CH4平衡转化率见表。
平衡点 | a | b | c | d |
n(CH4)/mol | 1 | 1 | 1 | 1 |
n(H2O)/mol | 2 | 2 | 1 | 1 |
CH4平衡转化率% | 50 | 69 | 50 | 20 |
①由表数据分析,温度:a点______b点(填“>”或“<”)。
②c点平衡混合物中的体积分数为______(保留3位有效数字)。
②若d点总压强为aMPa,则d点反应I分压平衡常数Kp为_______(MPa)2(列出计算式即可)。
(4)反应II在工业上称为一氧化碳的催化变换反应,研究表明该反应用Fe3O4作催化剂,反应历程如下:
第一步:Fe3O4+4CO→3Fe+4CO2
第二步:3Fe+4H2O→Fe3O4+4H2
已知第一步为慢反应,则第一步反应活化能比第二步反应______(填“大”或“小”)。
由于CO还原性较强,若将Fe3O4还原成Fe,并以Fe的形式大量存在于反应体系中,会使催化剂失去活性,但在实际生产中一般不会发生催化剂失去活性的情况,请结合一氧化碳的催化变换反应历程说明理由______。
(5)用二氧化碳与氢气催化加氢制乙醇,其反应原理为:2CO2(g)+6H2(g)CH3CH2OH(g)+3H2O(g) △H<0。经实验测定在不同投料比x1、x2、x3时CO2的平衡转化率与温度的关系如图曲线所示x=。
①x1、x2、x3从小到大的顺序为______。
②从平衡角度分析,随温度升高,不同投料比时CO2平衡转化率趋于相近的原因是______。
14. 我国科学家团队采用自激发缺陷诱导的方法获得白光,合成了首例缺陷诱导的晶态无机硼酸盐单一组分白光材料Ba2[Sn(OH)6][B(OH)4]2。
(1)基态50Sn原子的价电子排布式为______。Ba、Sn、O三种元素的电负性由大到小的顺序为______。
(2)Na2[B4O5(OH)4]·8H2O(硼砂)的阴离子的结构式如图所示。则硼原子的杂化方式为______;硼砂中存在的作用力有______(填标号)。
a.氢键 b.离子键 c.共价键 d.配位键
(3)环硼氮六烷(结构如图)在热水中比冷水中溶解度显著增大的主要原因是______。
(4)超高热导率半导体材料——砷化硼(BAs)的晶胞结构如图所示,则1号砷原子的坐标为______。已知阿伏加德罗常数的值为NA,若晶胞中As原子到B原子最近距离为a pm,则该晶体的密度为______g·cm-3。(列出含a、NA的计算式即可)。
15. 查尔酮类化合物J()是黄酮类药物合成中间体,一种合成路线如图:
已知:RCOCH3+R′CHORCOCH=CHR′
(1)H的名称为______。I中含氧官能团的名称为_____。
(2)C→D的反应类型为_____,H→I的反应类型为_____。
(3)E的结构简式为_____。
(4)F→G反应的化学方程式为_____。
(5)满足下列条件的E的同分异构体的结构简式为______。
①核磁共振氢谱有5组峰,峰面积之比为2∶2∶2∶1∶1
②能发生银镜反应
③遇FeCl3显色
【期中真题】福建省厦门第一中学2022-2023学年高二上学期期中考试化学试题.zip: 这是一份【期中真题】福建省厦门第一中学2022-2023学年高二上学期期中考试化学试题.zip,文件包含期中真题福建省厦门第一中学2022-2023学年高二上学期期中考试化学试题原卷版docx、期中真题福建省厦门第一中学2022-2023学年高二上学期期中考试化学试题解析版docx等2份试卷配套教学资源,其中试卷共35页, 欢迎下载使用。
【期中真题】重庆市育才中学校2022-2023学年高三上学期期中考试化学试题.zip: 这是一份【期中真题】重庆市育才中学校2022-2023学年高三上学期期中考试化学试题.zip,文件包含期中真题重庆市育才中学校2022-2023学年高三上学期期中考试化学试题原卷版docx、期中真题重庆市育才中学校2022-2023学年高三上学期期中考试化学试题解析版docx等2份试卷配套教学资源,其中试卷共26页, 欢迎下载使用。
【期中真题】辽宁省实验中学2022-2023学年高三上学期期中考试化学试题.zip: 这是一份【期中真题】辽宁省实验中学2022-2023学年高三上学期期中考试化学试题.zip,文件包含期中真题辽宁省实验中学2022-2023学年高三上学期期中考试化学试题原卷版docx、期中真题辽宁省实验中学2022-2023学年高三上学期期中考试化学试题解析版docx等2份试卷配套教学资源,其中试卷共24页, 欢迎下载使用。












