




【暑假初高衔接】人教版化学初三(升高一)暑假预习-(必修1)第11课 铁及其化合物 讲学案
展开
第11课时 铁及其化合物
学习目标:
1.了解铁单质的性质
2.铁的重要化合物的性质
3.Fe2+和Fe3+的性质及检验
重点:
1.铁盐和亚铁盐的转化
2.Fe3+的检验
难点:
1.制备Fe(OH)2的实验
2.Fe、Fe2+、Fe3+转化关系模型
温故知新
CO是一种无色、无味、有毒的可燃气体污染物,具有还原性,可用于冶金工业。某兴趣小组为探究其具有还原性,设计了如下实验装置。请回答以下有关问题:
①CO气体能使人中毒,其原因是 。
②实验开始时,先通入CO一段时间后,再加热,其原因是
③实验中图A处玻璃管中发生的现象是 ,其化学反应方程式为 。
④实验中图B处发生的现象是 ,其化学反应方程式为 。
⑤该装置中有一个明显的缺陷 ,请指出改正方法 。
开启新世界
人类早期使用的铁,是来自于太空的陨铁。在自然界中可以像陨铁中的铁那样以单质形式存在,但主要是以+2价,+3价的化合物形式存在于矿石中,铁元素在地壳中的含量仅次于氧、硅和铝居第四位。
我国目前发现最早的人工冶铁制品是甘肃灵台出土的春秋初年秦国的铜柄铁剑,这说明春秋初期我国已经掌握了冶铁技术。战国中期后,铁制工具在社会生产中发挥了巨大作用。工业炼铁的原理是用还原的方法把铁从铁石中提炼出来,你还记得炼铁高炉内发生了化学反应吗?
【思考】单质铁具有什么性质?
单质铁具有________性和___________。铁能导电,但其导电性不如铜和铝。铁能被________吸引。铁的化学性质比较活泼,它能与许多物质发生化学反应。
写出下列离子方程式:
1.铁和稀硫酸:______________________________________;
2.铁在氧气中燃烧:____________________________________;
3.铁在氯气中燃烧:____________________________________;
4.铁和硫酸铜反应:____________________________________。
根据上面4个离子方程式可以看出:在一定条件下,铁作为_________剂能与非金属单质、酸、盐溶液反应。铁与氧化性较弱的氧化剂反应,铁原子失去____个电子生成_____价铁的化合物;铁与氧化锌较强的氧化剂反应,铁原子失去_____原子,生成______价铁的化合物。
Fe — 2e— → Fe2+
Fe — 3e— → Fe3+
【练习1】下列物质中,不能由金属跟非金属单质直接化合得到的是
A. Na2O2 B. NaCl C. FeCl2 D. Fe3O4
【思考】金属活动性顺序中,K、Ca、Na常温下能与水发生反应,Mg在热水中也能和水反应,那么铁在什么情况下能和水蒸气发生反应?
在钢铁厂的生产中,炽热的铁水或钢水注入模具前,模具必须进行充分的干燥处理,不能留水。这是为什么呢?
[实验猜想]铁在高温下能与水蒸气发生反应。
[设计实验]利用酒精灯加热水,提供水蒸气,水蒸气与铁粉混合用酒精喷灯进行加热,如果产生气体,将产生的气体收集研究。
[实验装置]
A B C D
[实验步骤]
1.检查__________,放入药品;
2.点燃_____处的酒精灯/酒精喷灯,再点燃_____处的酒精灯/酒精喷灯。
3.一段时间后,取下试管中收集的气体,用拇指堵住试管口,靠近酒精灯火焰,移开拇指。
[实验现象]试管中的气体具有可燃性,点燃有爆鸣声;玻璃管内红热的铁变化黑色,黑色固体具有磁性。
[实验结论]铁在高温下与水蒸气反应有可燃性气体生成,铁变成了四氧化三铁。化学方程式:
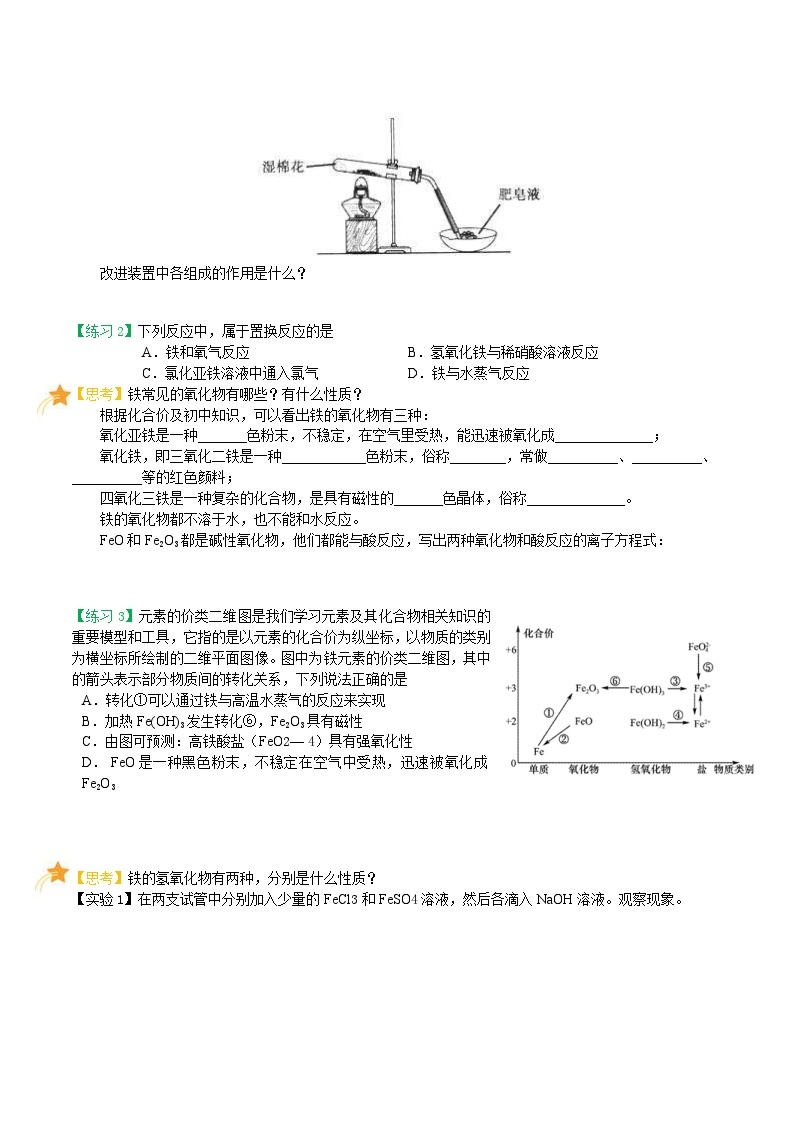
[反思与交流]有的同学认为这套装置过于复杂,简化为下图
改进装置中各组成的作用是什么?
【练习2】下列反应中,属于置换反应的是
A.铁和氧气反应 B.氢氧化铁与稀硝酸溶液反应
C.氯化亚铁溶液中通入氯气 D.铁与水蒸气反应
【思考】铁常见的氧化物有哪些?有什么性质?
根据化合价及初中知识,可以看出铁的氧化物有三种:
氧化亚铁是一种_______色粉末,不稳定,在空气里受热,能迅速被氧化成______________;
氧化铁,即三氧化二铁是一种____________色粉末,俗称________,常做__________、__________、__________等的红色颜料;
四氧化三铁是一种复杂的化合物,是具有磁性的_______色晶体,俗称______________。
铁的氧化物都不溶于水,也不能和水反应。
FeO和Fe2O3都是碱性氧化物,他们都能与酸反应,写出两种氧化物和酸反应的离子方程式:
【练习3】元素的价类二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图像。图中为铁元素的价类二维图,其中的箭头表示部分物质间的转化关系,下列说法正确的是
A.转化①可以通过铁与高温水蒸气的反应来实现
B.加热Fe(OH)3发生转化⑥,Fe2O3具有磁性
C.由图可预测:高铁酸盐(FeO2— 4)具有强氧化性
D. FeO是一种黑色粉末,不稳定在空气中受热,迅速被氧化成Fe2O3
【思考】铁的氢氧化物有两种,分别是什么性质?
【实验1】在两支试管中分别加入少量的FeCl3和FeSO4溶液,然后各滴入NaOH溶液。观察现象。
Fe(OH)3 Fe(OH)2
【实验现象】FeCl3和NaOH反应,迅速生成红褐色沉淀,一段时间后不变化;FeCl2和NaOH反应,迅速生成白色絮状沉淀,白色沉淀迅速变为灰绿色,一段时间后有红褐色沉淀生成。
上述反应的化学方程式:
【思考】为什么白色的氢氧化亚铁会有这些变化?
亚铁化合物不稳定,容易空气中的氧气被氧化成三价铁,化学方程式:_________________________。
【思考】氢氧化亚铁易被氧化,实验室如何制备氢氧化亚铁?
方法:将硫酸亚铁置于试管中,在硫酸亚铁溶液上滴一层石蜡油或煤油。用长胶头滴管吸适量煮沸后的氢氧化钠溶液,将滴管下端伸入液面以下,挤入氢氧化钠溶液。
石蜡油或煤油的作用是___________________,氢氧化钠溶液需要煮沸的原因是____________________。
Fe(OH)3
【实验2】加热Fe(OH)3
【实验现象】氢氧化铁变为红褐色粉末,试管口有水滴出现。
化学方程式为:____________________________。
Fe(OH)2和Fe(OH)3从物质的分类来看,都属于____________,所以都能和______反应生成盐和水,写出两者与稀盐酸的化学方程式________________________,________________________。
【练习4】下列离子方程式书写错误的是
A.铁与稀硫酸反应:Fe+6H+ === Fe3+ +3H2↑
B.氧化钠溶于水:Na2O+H2O = 2Na++2OH—
C.FeSO4溶液在空气中变质:12Fe2++3O2+6H2O = 8Fe3++4Fe(OH)3
D.在强碱性溶液中NaClO与Fe(OH)3 反应生成Na2FeO4 :
3ClO— + 2Fe(OH)3 +4OH—= 2FeO2— 4+3Cl— +5H2O
【思考】Fe2(SO4)3、FeCl3是常见的铁盐,FeCl2、FeSO4是常见的亚铁盐,通过刚才的学习我们知道,亚铁不稳定,容易被氧化生成Fe3+,被氧化后的亚铁盐开始变质,我们要怎样才能知道亚铁盐变质呢?
【实验3】在两支试管中分别加入少量的FeCl3溶液和FeCl2溶液,各滴入几滴KSCN溶液,观察现象。将氯气通入FeCl2(或滴加新制氯水),观察现象。向FeCl3溶液中加入过量铁粉,观察现象。
Fe3+与KSCN溶液反应生成的红色物质不是沉淀,是一种络合物;Fe2+可以使用K3[Fe(CN)6]检验,现象为出现蓝色沉淀。
【实验现象】向FeCl3中滴加KSCN溶液,溶液变为(血)红色,FeCl2无明显变化。FeCl2中通入氯气(或滴加新制氯水)后,出现溶液变为(血)红色。向FeCl3溶液中加入过量铁粉后,红色消失。
【分析】Fe3+能使和KSCN反应出现(血)红色,Fe2+无明显变化。当FeCl2中通入氯气(或滴加新制氯水)后,Fe2+被氧化成了Fe3+,出现溶液变为(血)红色。向FeCl3溶液中加入过量铁粉后,Fe3+被还原成了Fe2+。
所以鉴别FeCl2溶液是否开始变质可以使用KSCN溶液检验。
【思考】上述实验说明FeCl3溶液中的Fe3+被铁粉_______成Fe2+,Fe2+由被Cl2_________成Fe3+,写出两个反应的离子方程式________________________,_____________________。
Fe、FeSO4、Fe2(SO4)3三种物质中,可以做还原剂的是___________,可以做氧化剂的是_____________,既能做氧化剂也能做还原剂的是_______________。完成下图的“铁三角”,并写出相关离子方程式。
Fe
②
③
④
①
铁三角
⑤
⑥
Fe2+ Fe3+
① ________________________________
② ________________________________
③ ________________________________
④ ________________________________
⑤ ________________________________
⑥ ________________________________
【思考】Fe3+具有氧化性,在生产中哪些地方可以用到呢?
FeCl3溶液常用于蚀刻铜板,化学方程式为____________________________。
【练习5】向一定量的Fe、Fe2O3、FeO的混合物中加入100 mL 1 mol·L—1的盐酸,恰好使混合物完全反应溶解,放出4.48 mL(标准状况)气体。所得溶液中,加入KSCN溶液无红色出现,那么用足量的CO在高温下还原相同质量的此混合物,得到铁的质量为
A.11.2 g B.5.6 g C.2.8 g D.无法计算
【练习6】苹果汁是人们喜爱的饮料,由于此饮料中含有Fe2+,在空气中易转变为Fe3+。若榨汁时加入维生素C,可有效防止这种现象的发生。这说明维生素C具有
A.还原性 B.氧化性 C.碱性 D.酸性
课堂练习
1.下列有关物质及成分、性质和用途都正确的是( )
选项
物质及成分
性质
用途
A
小苏打(Na2CO3)
与酸反应产生二氧化碳
作发酵粉
B
胃舒平[Al(OH)3 ]
与酸发生中和反应
做胃酸中和剂
C
磁性氧化铁(Fe2O3)
难溶于水,颜色为红色
制造红色涂料
D
蓝矾(CuSO4·5H2O)
蓝色
检验水蒸气
2.向盛有Fe2(SO4)3溶液的试管中滴入几滴KSCN溶液后,溶液呈
A. 无色 B. 黄色 C. 红色 D. 浅绿色
3.除去FeCl3溶液中的少量FeCl2杂质,可向其中加入适量的
A. Fe B. 氯水 C. KSCN溶液 D. 硝酸
4.把铁片放入下列溶液中,铁片溶解,溶液质量增加,但没有气体放出的是
A. 硝酸银溶液 B. 硫酸铜溶液 C. 稀硫酸 D. 硫酸铁溶液
5.下列说法中正确的是
A.铝粉与氧化镁混合共热能冶炼出镁
B.FeCl2只能通过置换反应生成,FeCl3只能通过化合反应生成
C.Fe3O4中铁元素的化合价为+2,+3价,故Fe3O4为混合物D
.等质量的NaHCO3和Na2CO3与足量盐酸反应,在相同条件下Na2CO3产生的CO2体积小
6.下列物质长期露置在空气中其成分不发生变化的是( )
A. Na2O2 B. 氯水 C. Na2CO3 D. Fe(OH)2
7.下列各组物质反应后,滴入溶液,显红色的是
①Fe、稀盐酸;②FeCl2溶液和Cl2;③Fe、CuSO4溶液;④Fe2O3、稀硫酸
A.②④ B.①② C.③④ D.①④
8.检验某加碘食盐中是否含有,取相同食盐样品进行如表所示实验。
实验①
实验②
实验③
振荡,溶液迅速变为蓝色
振荡,一段时间后溶液变为浅蓝色
振荡,溶液变为浅黄色
(已知:KIO3+5KI+3H2SO4 = 3I2+3K2SO4+3H2O)
下列说法正确的是
A.仅由实验①就能证明食盐样品中存在KIO3
B.实验③能证明食盐样品中不存在KIO3
C.实验②中发生反应的离子方程式4I—+O2+4H+ = 2I2+2H2O
D.以上实验说明离子的还原性:I—>Fe2+
9.阅读下面科普信息,回答问题:
一个体重50 kg的健康人含铁2 g,这2 g铁在人体中以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是____
A.Fe B.Fe2+ C.Fe3+
(2)工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有________性。下列不能实现上述转化的物质是_________
A.Cl2 B.O2 C.FeCl3 D.KMnO4(H+)
(3)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有__________性。
(4)在Fe+4HNO3(稀)= Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了_________和________性。
10.某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol/L的溶液。在FeCl2溶液中需加入少量铁屑,其目的是________。
(2)甲组同学取2 mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为________。
(3)乙组同学认为甲组的实验不够严谨,该组同学在2 mL FeCl2溶液中先加入0.5 mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是_____________________。
能力提升
1.下列关于铁的叙述中错误的是
A.纯净的铁是光亮的银白色金属
B.铁能被磁体吸引
C.铁是地壳中含量最多的金属元素
D.铁具有延展性和导热性,可制作炊具
2.欲除去FeSO4溶液中含有的CuSO4和Fe2(SO4)3等少量杂质,应选用的试剂是
A.氨水 B.铝粉
C.铁粉 D.NaOH溶液
3.下列各组物质相互反应后,再向得到的溶液中滴入KSCN溶液,溶液变成红色的是
A.新制氯水和氯化亚铁溶液
B.铁屑和氯化铜溶液
C.铁屑和过量稀硫酸
D.过量铁屑和氯化铁溶液
4.向下列物质中滴加NaOH溶液产生白色絮状沉淀,并迅速变成灰绿色,最后变成红褐色的是
A.FeSO4 B.Na2SO4
C.FeCl3 D.KCl
5.已知由FeO、Fe2O3、Fe3O4组成的混合物中,铁与氧的质量比为21:8,则混合物中FeO、Fe2O3、Fe3O4三种物质的物质的量之比为
A.2:3:5 B.1:1:3
C.2:5:3 D.1:2:3
6.某兴趣小组进行某补血剂中铁元素含量的测定实验流程如下:
下列说法不正确的是
A.步骤①研磨时研杵应保持垂直,小心压碎
B.步骤②加入氨水的作用是将Fe2+完全沉淀
C.步骤③多步操作为过滤、洗涤、灼烧至恒重、冷却、称重
D.每片补血剂中铁元素的质量为0.7w g
7.某工厂的工业硫酸盐废水中含有大量的Fe2+、Fe3+、较多的Cu2+和少量的Na+。工厂计划从该废水中回收硫酸亚铁和金属铜,设计如下流程图。
回答下列问题:
(1)A的化学式为________,D的化学式为________。
(2)在工业废水中加入过量A时,反应的离子方程式有__________________、____________________。
(3)得到FeSO4·7H2O晶体的操作Ⅲ为加热浓缩、冷却结晶、________、________、干燥。
8.用下面两种方法可以制得白色的Fe(OH)2沉淀。
方法一:用不含Fe3+的FeSO4溶液与用不含O2的蒸馏水配制的NaOH溶液反应制备。
(1)用硫酸亚铁晶体配制上述FeSO4溶液时还需加入____________。
(2)除去蒸馏水中溶解的O2,常采用________的方法。
(3)生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面以下,再挤出NaOH溶液。这样操作的理由是________________________________。
方法二:在如图所示装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备。
(1)在试管Ⅰ里加入的试剂是____________________。
(2)在试管Ⅱ里加入的试剂是________________________________。
(3)为了制得白色Fe(OH)2沉淀,在试管Ⅰ和试管Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤是________________________________________________。
(4)这样生成的Fe(OH)2沉淀能较长时间保持白色,其理由是__________________。
【暑假初高衔接】人教版化学初三(升高一)暑假预习-(必修1)第16课 化学键 讲学案: 这是一份【暑假初高衔接】人教版化学初三(升高一)暑假预习-(必修1)第16课 化学键 讲学案,文件包含暑假初高衔接人教版化学初三升高一暑假预习-必修1第16课化学键解析版docx、暑假初高衔接人教版化学初三升高一暑假预习-必修1第16课化学键原卷版docx等2份学案配套教学资源,其中学案共15页, 欢迎下载使用。
【暑假初高衔接】人教版化学初三(升高一)暑假预习-(必修1)第12课 金属材料 讲学案: 这是一份【暑假初高衔接】人教版化学初三(升高一)暑假预习-(必修1)第12课 金属材料 讲学案,文件包含暑假初高衔接人教版化学初三升高一暑假预习-必修1第12课金属材料解析版docx、暑假初高衔接人教版化学初三升高一暑假预习-必修1第12课金属材料原卷版docx等2份学案配套教学资源,其中学案共17页, 欢迎下载使用。
【暑假初高衔接】人教版化学初三(升高一)暑假预习-(必修1)第10课 物质的量(二) 讲学案: 这是一份【暑假初高衔接】人教版化学初三(升高一)暑假预习-(必修1)第10课 物质的量(二) 讲学案,文件包含暑假初高衔接人教版化学初三升高一暑假预习-必修1第10课物质的量二解析版docx、暑假初高衔接人教版化学初三升高一暑假预习-必修1第10课物质的量二原卷版docx等2份学案配套教学资源,其中学案共18页, 欢迎下载使用。












