




2023年高考化学一轮复习整合有效信息书写氧化还原方程式课件
展开OH- + H2O
练习①新制氯水滴入Na2S2O3溶液,写出该反应的离子方程式: _____________________________________________________。②硝化细菌可利用氧气和自身的酶,将酸性土壤中的NH4+氧化为NO3-,该反应的离子方程式:___________________________。
例1 [2020·全国卷Ⅲ,27(5)]硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式: _____________________________________________________。
Ni2++ ClO-+ == NiOOH+
2 1 2 1
4 1
4Cl2+S2O32-+5H2O==8Cl-+2SO42-+10H+
NH4++2O2==NO3-+2H++H2O
练习 ③不酸化的KMnO4和H2O2反应生成黑色沉淀的离子方程式: _____________________________________________________。④SO2通入双氧水中的化学方程式:_______________________。⑤单质金置于浓盐酸中,通入氯气可以溶解,生成[AuCl4]-的离子方程式:______________________________。⑥CuSO4与NaCl的混合溶液中通入SO2可制备氯化亚铜沉淀的离子反应:_______________________________________________。
2MnO4-+3H2O2==2MnO2↓+3O2↑+2OH-+2H2O
SO2+H2O2==H2SO4
2Au+2Cl-+3Cl2 =2[AuCl4]-
2Cu2++SO2+2Cl-+2H2O==2CuCl↓+SO42-+4H+
“六步法”突破新情境下氧化还原方程式的书写
①常识+信息判断;②H+/OH-/H2O先不写;③-2价氧不写产物;
最小公倍数,注意凑整;
四大金刚的变价原子及其搭配离子守恒
1.按要求完成下列方程式。(3)Na2S溶液长期放置有硫析出,原因为______________________________(用离子方程式表示)。(5)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其反应的离子方程式为 __________________________________。
2S2-+O2+2H2O==4OH-+2S↓
SO32-+I2+H2O==2I-+SO42-+2H+
除了补缺项H+/OH-等,还有四大金刚的判断!
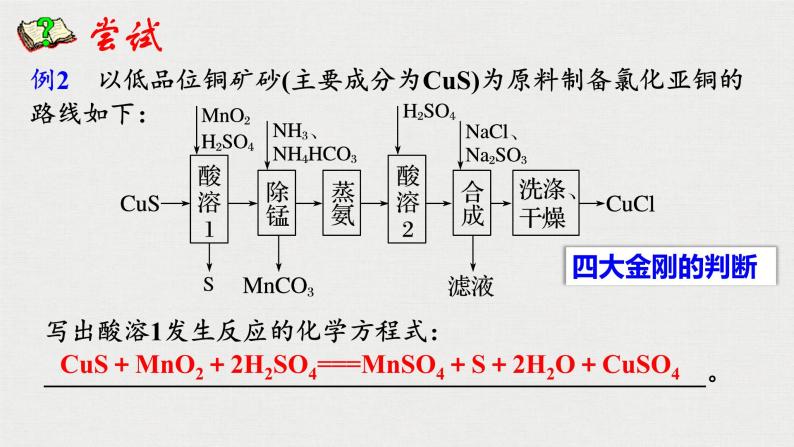
例2 以低品位铜矿砂(主要成分为CuS)为原料制备氯化亚铜的路线如下:
写出酸溶1发生反应的化学方程式:__________________________________________________。
CuS+MnO2+2H2SO4===MnSO4+S+2H2O+CuSO4
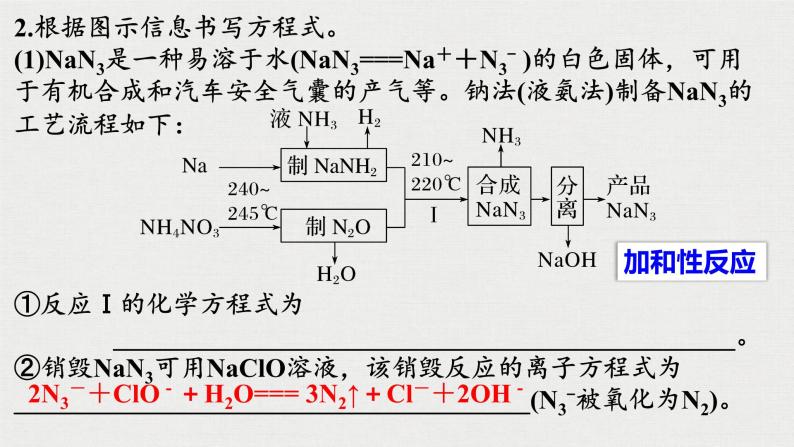
2.根据图示信息书写方程式。(1)NaN3是一种易溶于水(NaN3===Na++N3- )的白色固体,可用于有机合成和汽车安全气囊的产气等。钠法(液氨法)制备NaN3的工艺流程如下:
①反应Ⅰ的化学方程式为 _______________________________________________。②销毁NaN3可用NaClO溶液,该销毁反应的离子方程式为_______________________________________(N3-被氧化为N2)。
2N3-+ClO-+H2O=== 3N2↑+Cl-+2OH-
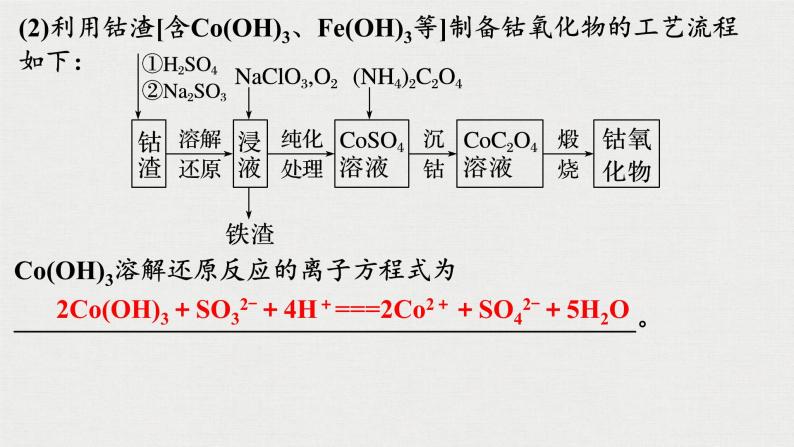
(2)利用钴渣[含C(OH)3、Fe(OH)3等]制备钴氧化物的工艺流程如下:
C(OH)3溶解还原反应的离子方程式为_______________________________________________。
2C(OH)3+SO32-+4H+===2C2++SO42-+5H2O
“价态变化规律”突破产物的判断
难点:记忆常见元素化合物的 、 、还有 。
(1)常见的氧化剂某些非金属单质、含有高价态元素的化合物、过氧化物等。
0 +1 +4 +5 +7
Cl- Cl- /Cl2 Cl-/Cl2 Cl- /Cl2 ——
注意:上述为无信息情况下的产物,有Cl-时酸性环境会生成Cl2。
②金属含氧酸根/金属氧化物:
+7 Mn2+/MnO2/MnO42- +2/+4/+6
+6 Fe3+/Fe(OH)3 +3
+6 Cr3+/Cr(OH)3 +3
+4 Pb2+/PbSO4 +2
+4 Sn2+(Ⅱ) +2
+3 C2+(Ⅱ) +2
+4 Ce3+(Ⅲ) +3
+6 SO2 +4
+6/-1 SO2 +4
+5 NO2/ NO/N2/NH4+ +4/+2/0/-3
0H2O/OH-/MOx/含氧酸根 -2
0 O2+(同上) -2
-1 O2+(同上) -2
(2)常见的还原剂活泼的金属单质、非金属阴离子及含低价态元素的化合物、低价金属阳离子、某些非金属单质及其氢化物等。
①还原剂硫系列:S2-/HS-/H2S,S,S2O32-,S2O42-,S2O52-,SO32-/HSO3-/SO2→ ;
-2 0 +2 +3 +4 +4
-3 N2 /NOx/HNO3
-2 N2
-3 N2
-3 N2+ 其它(CO2/SO42-)
-3 N2+ CO2
注意:上述为无信息情况下的产物; NH3 + HNO3== NH4NO3; (NH4)2Fe(SO4)2 + KMnO4 → Fe3+
练习 用如下方法回收废旧CPU中的单质Au(金),Ag和Cu:
Au+4NaCl+5HNO3===HAuCl4 +NO↑+2H2O+4NaNO3
4.[2019·全国卷Ⅱ,26(2)①]立德粉ZnS·BaSO4(也称锌钡白),是一种常用白色颜料。以重晶石(BaSO4)为原料,可按如下工艺生产立德粉:
在回转炉中重晶石被过量焦炭还原为可溶性硫化钡,该过程的化学方程式为_____________________________________。回转炉尾气中含有有毒气体,生产上可通过水蒸气变换反应将其转化为CO2和一种清洁能源气体,该反应的化学方程式为: ______________________________。
2024届高三化学 一轮复习 陌生方程式书写 《非氧化还原方程式》书写课件: 这是一份2024届高三化学 一轮复习 陌生方程式书写 《非氧化还原方程式》书写课件,共3页。PPT课件主要包含了盐的水解,环节一等内容,欢迎下载使用。
高考化学二轮复习课件专题突破(二) 整合有效信息书写化学(离子)方程式(含解析): 这是一份高考化学二轮复习课件专题突破(二) 整合有效信息书写化学(离子)方程式(含解析),共20页。PPT课件主要包含了章末综合检测二等内容,欢迎下载使用。
【备战2023高考】化学总复习——专题讲座(二)《整合有效信息书写陌生化学方程式》讲义: 这是一份【备战2023高考】化学总复习——专题讲座(二)《整合有效信息书写陌生化学方程式》讲义,文件包含备战2023高考化学总复习专题讲座二《整合有效信息书写陌生化学方程式》讲义解析版docx、备战2023高考化学总复习专题讲座二《整合有效信息书写陌生化学方程式》讲义原卷版docx等2份课件配套教学资源,其中PPT共0页, 欢迎下载使用。












