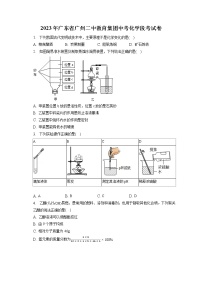

2021年广东省广州实验中学教育集团中考二模化学试题(含答案)
展开2021年广东省广州实验中学教育集团中考二模化学试题
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列方法没有蕴含化学变化的是
A.把秸秆、杂草、人畜粪便放在密闭的沼气池中发酵,产生甲烷
B.用氯化钠消除公路上的积雪
C.用氢氧化钠溶液的强腐蚀性,制作叶脉书签
D.生石灰做食品干燥剂
2.医疗急救中给病人输氧,其中“氧”指的是
A.氧元素 B.氧原子 C.氧分子 D.氧离子
3.“世界棉花看中国,中国棉花看新疆”。新疆长绒棉属于材料中的
A.合成材料 B.天然纤维 C.无机材料 D.复合材料
4.2021年世界水日的主题是“珍惜水、爱护水”。下列水处理方法错误的是
A.用明矾除去水中的悬浮物
B.用Na2SO4除去硬水中的Mg2+和Ca2+
C.用臭氧进行自来水消毒
D.污水经物理、化学成生化方法进行分级处理后,可以达到农灌或景观用水标准
5.已知硫和硒在元素周期中处于同一族,其原子结构示意图如图所示,下列说法不正确的是
A.图中X=18
B.硫原子和硒原子的化学性质相似
C.硫在氧气中燃烧时,硫原子得到两个电子形成S2-
D.硒是人体必需的微量元素
6.下列诗句或谚语隐含的化学知识,说法错误的是
A.“甘之如怡”,糖类都有甜味
B.“木棉花落絮飞初”,“絮”的主要成分是纤维素
C.“酒香不怕巷子深”,说明分子在不断运动
D.“真金不怕火炼”说明金的化学性质很稳定
7.从海水中提取粗盐的流程如下,下列说法正确的是
A.蒸发池中,氯化钠溶液溶质质量分数逐渐变大
B.经过第③步的操作,进入结晶池后,继续蒸发水分,只有氯化钠晶体析出
C.海水晒盐的过程说明NaCl的溶解度随温度升高而降低
D.往母液中加入NaCl固体,溶液质量增加
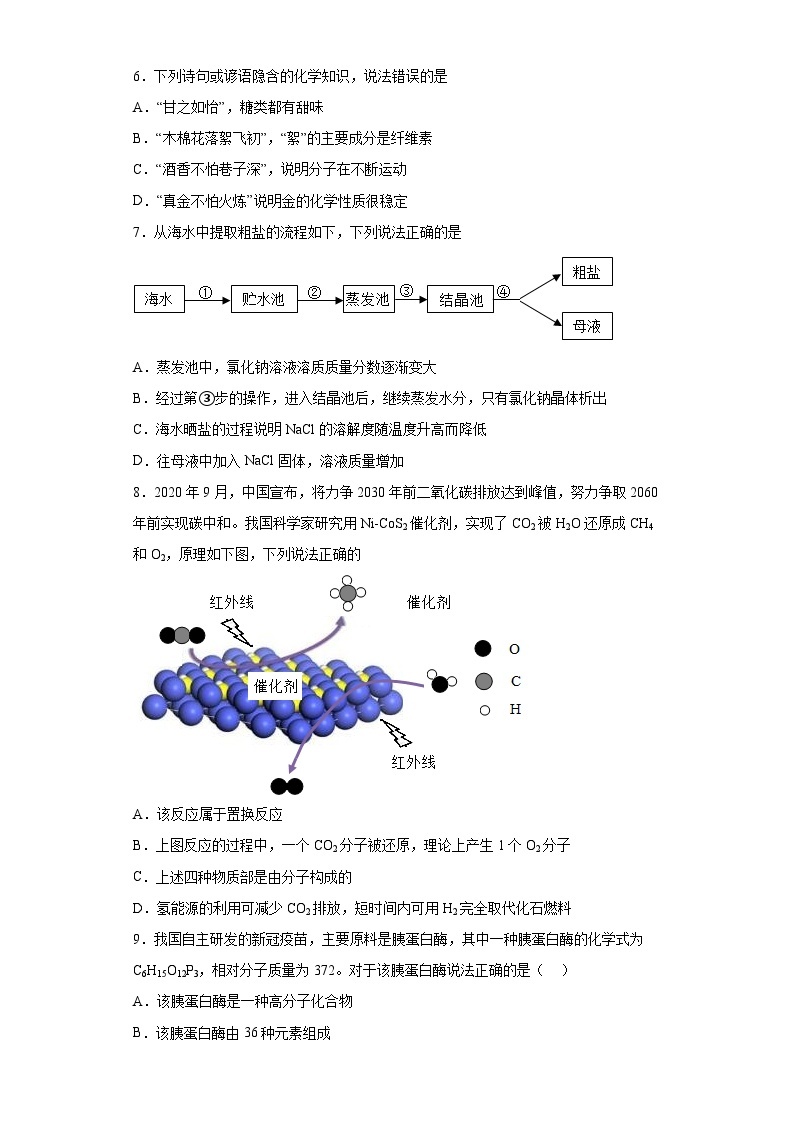
8.2020年9月,中国宣布,将力争2030年前二氧化碳排放达到峰值,努力争取2060年前实现碳中和。我国科学家研究用Ni-CoS2催化剂,实现了CO2被H2O还原成CH4和O2,原理如下图,下列说法正确的
A.该反应属于置换反应
B.上图反应的过程中,一个CO2分子被还原,理论上产生1个O2分子
C.上述四种物质部是由分子构成的
D.氢能源的利用可减少CO2排放,短时间内可用H2完全取代化石燃料
9.我国自主研发的新冠疫苗,主要原料是胰蛋白酶,其中一种胰蛋白酶的化学式为C6H15O12P3,相对分子质量为372。对于该胰蛋白酶说法正确的是( )
A.该胰蛋白酶是一种高分子化合物
B.该胰蛋白酶由36种元素组成
C.该胰蛋白酶中碳、氧元素质量比为3:8
D.该胰蛋白酶一个分子的质量为372
10.HCl的水溶液俗称盐酸,下列关于HCl的说法正确的
A.组成:HCl气体由H+、Cl-构成
B.性质:将HCl气体通入紫色石蕊试液,石蕊试液变蓝
C.用途:浓盐酸常用来做干燥剂
D.生产:工业上可用氯化钠来生产盐酸
11.过碳酸钠,化学式:2Na2CO3·3H2O2(或Na2CO4),又称过氧碳酸钠,俗称固体双氧水,是一种很好的供氧剂,与水反应:,进而缓慢放出氧气。下列说法正确的是
A.过碳酸钠与水反应的方程式中有元素化合价发生改变
B.过碳酸钠的水溶液呈碱性
C.缓慢放出氧气的化学方程式为
D.过碳酸钠与稀盐酸反应,只能产生一种气体
12.下列操作,能发生化学反应,且有明显现象的是
A.向CuO粉末中滴加氢氧化钠溶液
B.将打磨过的铝丝放入硝酸银溶液
C.研磨尿素【CO(NH2)2】与熟石灰的混合粉末
D.向CaCO3中滴加BaCl2溶液
13.下列下列少量杂质的方法正确的是
选项 | 物质 | 杂质 | 方法 |
A | C | CuO | 在空气中充分灼烧 |
B | 氯化钙溶液 | 盐酸 | 加入过量的熟石灰,过滤 |
c | NaOH溶液 | Na2CO3 | 逐滴滴加Ba(OH)2溶液,直到不再产生沉淀,过滤 |
D | NH3 | H2O | 将混合气体通过盛有浓硫酸的洗气瓶 |
A.A B.B C.C D.D
14.下列实验、操作、现象及结论均正确的是
| 实验操作 | 现象 | 结论 |
A | 将CO通入足量的澄清石灰水 | 产生白色沉淀 | 非金属氧化物可与碱反应生成盐和水 |
B | 用棉花分别蘸取酒精和水,放到酒精灯火焰上加热 | 酒精燃烧,产生蓝色火焰;水不燃烧 | 燃烧需要温度达到可燃物的着火点 |
C | 用小木条蘸浓硫酸 | 小木条表面碳化变黑 | 木条应含有C、H、O三种元素 |
D | 将等体积的稀硫酸和氢氧化钠溶液混合,充分反应后,滴加硝酸钡溶液 | 产生白色沉淀 | 硫酸过量 |
A.A B.B C.C D.D
二、填空题
15.下图是氮元素的化合价与物质类别的部分关系图:
(1)X代表的物质类别是______。
(2)B点表示的物质会导致酸雨,说明其溶于水会产生______(填离子符号)。
(3)一种新型火箭燃料亚硝酸氮的化学式为N(NO2)3,其中氮元素的化合价只有一种,均为______,则亚硝酸根离子的符号是______,F的化学式可能是______。(写一个)
(4)价类二维图中的物质在一定条件下可相互转化,若E为KNO3,则C转化为E的化学方程式为:______。
16.2021年3月全国两会期间,有人大代表建议将有色金重高端装备列入国家重点支持的高新技术领域。广义的有色金属是指铁、锰、铬以外的所有金属以及它们形成的合金,它们在多个行业中有着广泛的应用。请回答下列问题:
(1)黄铜、18K黄金都是有色合金。根据合金的一般特性可推知,黄铜的熔点比纯铜______(选填“高”或“低”),18K黄金的硬度比纯金______(选填“大”或“小”)。
(2)锂(Li)、钠、钾是有色金属大家族中的同一“小家族”成员。钠是一种极活泼金属,下图为钠与硫酸铜溶液反应的微观过程示意图。
①写出反应Ⅰ的化学方程式:______。
②用金属钾与硫酸铜溶液反应,预测其现象______。
17.有一包白色固体样品,可能由NaOH、CaCO3、BaCl2、MgCl2中的一种或几种物质组成,为探究该榉品的组成,某小组取量样品进行如下试验:
步骤Ⅰ:取少量样品于烧杯中,加足量水,充分搅拌,有白色不溶物产生。
步骤Ⅱ:取步骤Ⅰ的白色不溶物,加入足最稀盐酸,固体完全溶解,且有气泡产生。
步骤Ⅲ:取少量步骤Ⅰ所得的无色滤液,通入二氧化碳气体,有白色沉淀生成。
【查阅资料】CO2不能直接与BaCl2成MgCl2发生反应。
请回答下列问题:
(1)步骤Ⅱ产生气体的化学方程式为______。步骤Ⅲ可以确定该白色固体样品一定含有______。(填化学式)
(2)若要进一步确定样品的成分,还需进行的实验操作是______。
三、流程题
18.铁及其化合物在生产生活中用途广泛,如碳酸亚铁(FeCO3)可用作补血剂。工业上可用硫酸厂的炉渣(含Fe2O3、FeO、SiO2)制备FeCO3。其流程如图:
(1)溶液A的溶质有______种;往A中加入过量Fe,发生化合反应得到FeSO4溶液的方程式为______。
(2)已知溶液pH大于8.8时,Fe2+完全生成Fe(OH)2沉淀,现用1%的Na2CO3溶液(溶液pH≈11.62,浓度越大,碱性越强)在烧杯中制备FeCO3,应选用的加料方式是______。(填字母)
A.将FeSO4溶液与Na2CO3溶液同时加入烧杯中
B.将Na2CO3溶液缓慢加入盛有FeSO4溶液的烧杯中
C.将FeSO4溶液缓慢加入盛有Na2CO3溶液的烧杯中
(3)操作④要用蒸馏水洗涤FeCO3,目的是除去表面附着的杂质,洗涤干净的标志是:取最后一次洗涤液,向其中加入适量的______溶液,无______产生(填现象),即为洗涤干净。
(4)若整个流程共消耗10%的硫酸0.49t。
①需要98%的浓硫酸______t。
②理论上最后得到的FeCO3质量最多为______t。
四、实验题
19.掌握实验室制取气体的方法是初中生必备的化学素养,实验室里现有氯酸钾、二氧化锰、石灰石和稀盐酸,以及下列仪器:
(1)仪器③的名称为______。
(2)利用上述仪器和药品可以制取二氧化碳,需要的仪器除②以外,还需要______。(填序号)
(3)利用上述仪器和药品还可以制取氧气,反应的化学方程式为______。但加热过程中,有同学发现试管内有熔融状的紫红色物质出现,持续加热,试管内的紫红色物质又逐渐变成黑色。根据上述实验结果,小组同学查阅资料,得到氯酸钾制氧气的反应机理如下:
Ⅰ、______
Ⅱ、紫红色物质受热分解
Ⅲ、
①将反应Ⅰ补充完整
②反应Ⅱ的化学方程式为______。
③根据上述反应机理,理论上,充分反应前后,二氧化锰的______和______不变;但称量回收得到的MnO2的质量,发现总是小于加热前的质量,原因可能是______。
五、填空题
20.10%的CaCl2溶液常用作路面的保湿剂。
(1)要配制200kg10%的CaCl2溶液,需要水的质量为______。
(2)工业上常用氯化钙溶液与碳酸铵反应制备高纯碳酸钙,反应的化学方程式为______。
(3)根据各类物质之间的反应规律,请设计两种制备CaCl2的方案,完成下表:
方案 | 原料1 | 原料2 | 预期反应的化学方程式 | 依据的反应规律 |
① | ______ | ______ | ______ | 金属氧化物与酸反应,生成盐和水 |
② | ______ | ______ | ______ | ______ |
参考答案:
1.B
2.C
3.B
4.B
5.C
6.A
7.A
8.C
9.C
10.D
11.B
12.B
13.C
14.C
15.(1)单质
(2)H+
(3) +3
NaNO2
(4)2KOH+N2O5=2KNO3+H2O
16.(1) 低 大
(2) 产生气泡和蓝色沉淀
17.(1) CaCO3+2HCl=CaCl2+H2O+CO2↑ NaOH、BaCl2
(2)取少量步骤II后所得的溶液,滴入足量氢氧化钠溶液,如若产生白色沉淀,则含有氯化镁,若不产生白色沉淀,则不含氯化镁
18.(1) 3
(2)B
(3) 氯化钡 白色沉淀
(4) 0.05 0.058
19.(1)集气瓶
(2)③④⑦
(3) MnO2 质量 化学性质 氯气有剩余,第Ⅲ步反应未完全反应,使得生成二氧化锰的量减少
20.(1)180kg
(2)CaCl2+ (NH4) 2CO3=CaCO3↓+2NH4Cl;
(3) 氧化钙 稀盐酸 CaO+2HCl=CaCl2+H2O 氢氧化钙 稀盐酸 碱与酸反应,生成盐和水 Ca(OH)2+2HCl=CaCl2+2H2O
2021年广东省广州实验中学教育集团中考二模化学试题(含解析): 这是一份2021年广东省广州实验中学教育集团中考二模化学试题(含解析),共15页。试卷主要包含了单选题,填空题,流程题,实验题等内容,欢迎下载使用。
2023年广东省广州市广州大学附属中学中考二模化学试题: 这是一份2023年广东省广州市广州大学附属中学中考二模化学试题,共8页。
2023年广东省深圳市南山区南山实验教育集团中考二模化学试题: 这是一份2023年广东省深圳市南山区南山实验教育集团中考二模化学试题,共11页。试卷主要包含了全卷共4页,共16题,考试结束后,请将答题卡交回,可能用到的相对原子质量等内容,欢迎下载使用。