




卷03——高二化学下学期期末模拟测试卷(鲁科版2019)
展开下学期期末高分必刷卷03
高二化学
(满分:100分,时间:90分钟)
注意事项:
1.本试卷分第Ⅰ卷和第Ⅱ卷两部分。答卷前,考生务必将自己的姓名、准考证号填写在答题纸上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题纸上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题纸上。写在本试卷上无效。
4.测试范围:选择性必修2+选择性必修3
第Ⅰ卷
一、选择题(本题共10小题,每小题2分,共20分。每小题只有一个正确选项。)
1.(2021·大连市103中学高二月考)所下列化学用语的理解正确的是( )
A.比例模型既可以表示甲烷分子,也可以表示四氯化碳分子
B.电子式H既可以表示羟基,也可以表示氢氧根离子
C.丙烯的最简式可表示为CH2
D.结构简式(CH3)2CHCH3既可以表示正丁烷,也可以表示异丁烷
【答案】C
【详解】
A、比例模型的需要符合原子大小的比例,甲烷分子中的氢原子的半径比碳原子小,而四氯化碳分子中氯原子的半径比碳原子大,所以这两种分子不能用同一个比例模型来表示,A错误;
B、H可以表示羟基,而氢氧根的电子式为:,B错误;
C、将有机物的分子式化为最简式,是用元素符号表示化合物分子中各元素的原子个数比的最简关系式,就是最简式;丙烯的分子式为C3H6,则其最简式为CH2,C正确;
D、结构简式(CH3)2CHCH3仅表示异丁烷,D错误;
故合理选项为C。
2.(2019·剑河县第二高级中学高二期末)下列说法中正确的是( )
A.光导纤维、棉花、油脂、ABS树脂都是由高分子化合物组成的物质
B.开发核能、太阳能等新能源,推广基础甲醇汽油、使用无磷洗涤剂都可直接降低碳排放
C.红外光谱仪、核磁共振仪、质谱仪都可用于有机化合物结构的分析
D.通电时,溶液中的溶质离子分别向两极移动,胶体中的分散质粒子向某一极移动
【答案】C
【详解】
A.光导纤维是SiO2,属于无机物,油脂是高级脂肪酸与甘油形成的酯,属于酯类化合物,则二者不属于高分子化合物,故A错误;
B.无磷洗涤剂是在洗涤剂的成分中去掉了导致水污染的磷元素,它不会降低碳排放,故B错误;
C.有机化合物结构的分析过程中,经常用到红外光谱仪、核磁共振仪、质谱仪物理仪器,故C正确;
D.如果溶液中的溶质是非电解质,不能电离,则不会向两极移动,故D错误。
3.(2021·河北石家庄市·石家庄二中高二月考)向CuSO4溶液中逐滴滴加氨水,先生成蓝色沉淀,后蓝色沉淀逐渐溶解为深蓝色溶液,向深蓝色溶液中加入95%乙醇,深蓝色溶液变浑浊,静置后有深蓝色硫酸四氨合铜晶体析出,上层溶液颜色变浅.下列有关说法正确的是
A.生成蓝色沉淀反应的离子方程式为Cu2++2OH-=Cu(OH)2↓
B.NH3极易溶于水是因为氨分子与水分子形成配位键
C.蓝色沉淀溶解为深蓝色溶液是因为NH4+提供孤对电子
D.硫酸四氨合铜在乙醇中的溶解度小于在水中的溶解度
【答案】D
【详解】
A.一水合氨为弱电解质,离子方程式中不能拆,正确离子方程式为Cu2++2NH3·H2O=Cu(OH)2↓+2NH4+,A错误;
B.N、O元素的电负性均较大,氨分子和水分子间易形成氢键,所以NH3极易溶于水,与配位键无关,B错误;
C.蓝色沉淀溶解为深蓝色溶液的过程Cu(OH)2转化为[Cu(NH3)4]2+,提供孤电子对的是NH3,NH4+中并不含孤电子对,C错误;
D.向深蓝色溶液中加入95%乙醇,深蓝色溶液变浑浊,说明硫酸四氨合铜在乙醇中的溶解度小于在水中的溶解度,加入乙醇后硫酸四氨合铜变成沉淀析出,D正确。
4.(2021·山东聊城市·高二期中)下列有关晶体的叙述正确且前后叙述有因果关系的是
A.SiO2晶体熔点高、硬度大;SiO2晶体可用于制造光导纤维
B.碘晶体中的I—I键能较小;晶体碘沸点低、易升华
C.在金刚石和硅晶体中,原子间通过共价键形成空间网状结构;金刚石和硅晶体类型相同
D.NaCl晶体中Na+与Cl—个数比为1:1,CsCl晶体中Cs+与Cl—个数比也为1∶l,NaCl和CsCl的晶胞结构相同
【答案】C
【详解】
A.SiO2是原子晶体,熔点高、硬度大,SiO2晶体可用于制造光导纤维,但与其熔点高和硬度大无关,故A错误;
B.碘晶体中的 I—I 键能较小,导致碘的稳定性较弱,晶体碘之间的范德华力较小,导致沸点低、易升华,故B错误;
C.碳和硅同主族,在金刚石和硅晶体中,原子间通过共价键形成空间网状结构,金刚石和硅晶体类型相同,都是原子晶体,故C正确;
D.NaCl晶体和CsCl晶体中Na+与Cl—个数比为1:1,NaCl晶体中每个钠离子周围含有6个氯离子,每个氯离子周围有6个钠离子,每个氯化钠晶胞中含有4个钠离子和氯离子;CsCl晶体中每个铯离子周围含有8个氯离子,每个氯离子周围也有8个氯离子,每个氯化铯晶体中含有1个铯离子和1个氯离子,二者的结构不同,故D错误。
5.(2020·枣庄市第三中学高二月考)下列说法中错误的是
A.从CH4、NH4+、SO42-为正四面体结构,可推测PH4+、PO43-也为正四面体结构
B.1 mol金刚石晶体中,平均含有2 mol C—C键
C.水的沸点比硫化氢的高,是因为H2O分子间存在氢键,H2S分子间不能形成氢键
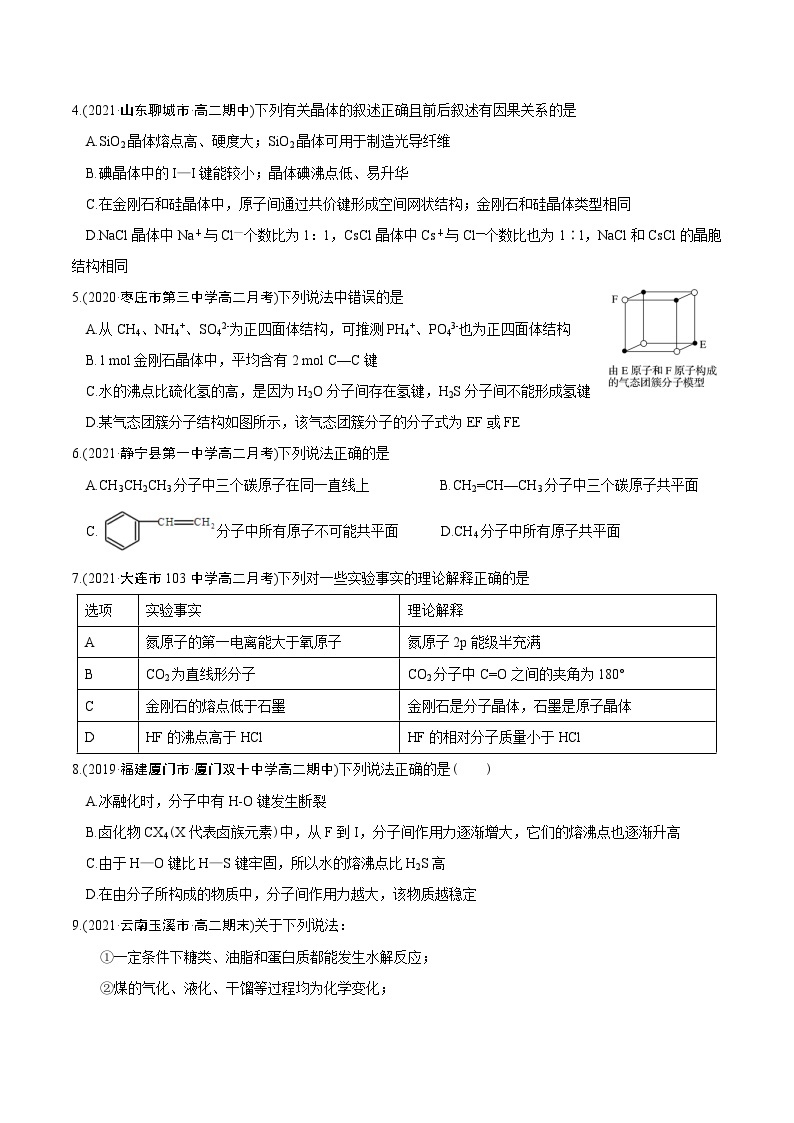
D.某气态团簇分子结构如图所示,该气态团簇分子的分子式为EF或FE
【答案】D
【解析】
【详解】
A.PH4+、PO43-中都形成4个σ键,且孤电子对数分别为0,则应为正四面体结构,选项A正确;
B.金刚石晶体中,每个C原子与其它4个C原子形成共价键,且每2个C原子形成1个共价键,则1 mol金刚石晶体中,平均含有4mol×=2 molC-C键,选项B正确;
C.氢键的作用力大于分子间作用力,H2O分子间存在氢键,H2S分子间不能形成氢键,导致水的沸点比硫化氢的高,选项C正确;
D.团簇分子中含有4个E、4个F原子,分子式应为E4F4或F4E4,选项D错误。
答案选D。
6.(2021·静宁县第一中学高二月考)下列说法正确的是
A.CH3CH2CH3分子中三个碳原子在同一直线上
B.CH2=CH—CH3分子中三个碳原子共平面
C.分子中所有原子不可能共平面
D.CH4分子中所有原子共平面
【答案】B
【详解】
A.烷烃中碳原子呈“锯齿形”,不可能共直线,A错误;
B.碳碳双键以及与双键直接相连的原子位于同一平面,可知该分子中三个碳原子共平面,B正确;
C.苯分子中所有原子共平面,故分子中所有原子有可能共平面,C错误;
D.CH4分子中4个氢原子构成正四面体形,所有原子不可能共平面,D错误;
故选B。
7.(2021·大连市103中学高二月考)下列对一些实验事实的理论解释正确的是
选项
实验事实
理论解释
A
氮原子的第一电离能大于氧原子
氮原子2p能级半充满
B
CO2为直线形分子
CO2分子中C=O之间的夹角为180°
C
金刚石的熔点低于石墨
金刚石是分子晶体,石墨是原子晶体
D
HF的沸点高于HCl
HF的相对分子质量小于HCl
【答案】A
【详解】
A.氮原子2p能级半充满,所以比较稳定,氮原子的第一电离能大于氧原子,故A正确;
B.理论解释不对,CO2分子的价层电子对是2,根据价层电子对互斥理论,CO2分子是直线型,故B错误;
C.金刚石是原子晶体,故C错误;
D.理论解释不对,HF分子中含有氢键,故HF的沸点高于HCl,故D错误;
答案选A。
8.(2019·福建厦门市·厦门双十中学高二期中)下列说法正确的是( )
A.冰融化时,分子中有H-O键发生断裂
B.卤化物CX4(X代表卤族元素)中,从F到I,分子间作用力逐渐增大,它们的熔沸点也逐渐升高
C.由于H—O键比H—S键牢固,所以水的熔沸点比H2S高
D.在由分子所构成的物质中,分子间作用力越大,该物质越稳定
【答案】B
【详解】
A.冰融化时发生物理变化,只破坏范德华力而不破坏化学键,故A错误;
B.CX4均为分子晶体,物质的熔沸点与其相对分子质量成正比,卤化物CX4(X代表卤族元素)中,从F到I,CX4分子的相对分子质量增大,分子间作用力逐渐增大,它们的熔沸点也逐渐升高,故B正确;
C.物质的熔沸点与化学键无关,水的熔沸点比H2S高,因为水分子间存在氢键,故C错误;
D.物质的稳定性与化学键有关,与范德华力无关,故D错误;
故选B。
9.(2021·云南玉溪市·高二期末)关于下列说法:
①一定条件下糖类、油脂和蛋白质都能发生水解反应;
②煤的气化、液化、干馏等过程均为化学变化;
③在炽热碎瓷片的作用下,石蜡油能分解产生乙烯;
④棉花、蚕丝、花生油都是天然高分子化合物;
⑤淀粉和纤维素互为同分异构体;
⑥乙烯与苯都是平面型分子;
⑦可以利用灼烧的方法鉴别棉线和羊毛。正确的有
A.4个 B.5个 C.6个 D.7个
【答案】A
【详解】
①单糖不会发生水解反应,故①错误;
②煤的气化、液化、干馏都是化学变化,故②正确;
③在炽热碎瓷片的作用下,石蜡油分解产生乙烯,故③正确;
④花生油不是天然高分子化合物,故④错误;
⑤淀粉和纤维素不是同分异构体,故⑤错误;
⑥乙烯与苯都是平面型分子,故⑥正确;
⑦可以利用灼烧的方法鉴别棉线和羊毛线,故⑦正确。
正确的说法有4个,选A。
10.(2020·长沙市·湖南师大附中高二期末)下列操作不能达到相应实验目的的是
选项
实验目的
操作
A
鉴别蔗糖和葡萄糖
分别加入新制氢氧化铜碱性悬浊液,加热煮沸
B
测定0.5 mol·L-1纯碱溶液的pH
用洁净的玻璃棒蘸取0.5 mol·L-1纯碱溶液滴在pH试纸上
C
用95.5%的酒精制备无水酒精
向95.5%的酒精中加入新制生石灰,然后蒸馏
D
实验室制备溴苯
向烧瓶中依次加入苯、溴水、铁粉,无需加热
【答案】D
【详解】
A. 蔗糖是非还原性双糖,葡萄糖是还原性单糖,分别加入新制氢氧化铜碱性悬浊液,加热煮沸,观察到有砖红色沉淀产生的是葡萄糖,A正确;
B. 用洁净的玻璃棒蘸取0.5 mol·L-1纯碱溶液滴在pH试纸上来测定0.5 mol·L-1纯碱溶液的pH,B正确;
C. 向95.5%的酒精中加入新制生石灰除去其中的少量水,乙醇的沸点较低,然后蒸馏分离制备无水酒精,C正确;
D. 实验室制备溴苯的药品是苯、液溴、铁粉或三溴化铁,苯与溴水会发生萃取分层现象,铁粉在水底与溴的苯溶液无法接触,D错误。
答案为D。
二、选择题(本题共5个小题,每小题4分,共20分。每小题有一个或两个正确选项,选全对得4分,选对但不全得2分,选错得0分。)
11.(2021·湖北黄冈市·高二期末) 下列叙述不正确的是
A.H2S和CS2分子都是含极性键的极性分子
B.PH3分子稳定性低于NH3分子,因为N—H键键能高
C.NH4+为正四面体结构,可推测出PH4+也为正四面体结构
D.H2O分解为H2和O2需要破坏共价键
【答案】A
【详解】
A.极性键是指不同种元素之间形成的共价键,CS2的结构式为S=C=S,只存在非极性键,故A错误;
B.根据元素周期律,简单气态氢化物的稳定性与电负性成相关,电负性大的形成的键能高,更稳定,N与P同主族,电负性N>P,N—H键键能高于P—H,故B正确;
C. NH4+中N为sp3杂化,4个H原子分别位于正四面体四个顶点,N原子位于中心,因为N和P同主族,价电子层结构相同, NH4+与PH4+结构相似,所以可推测出PH4+也为正四面体结构,故C正确;
D.水分解是化学反应,存在共价键断裂,故D正确;
12.(2021·山东枣庄市·滕州市第一中学新校高二月考)三草酸合铁酸钾(K3[Fe(C2O4)3]·3H2O)是制备铁触媒的主要原料。该配合物在光照下发生分解:2K3[Fe(C2O4)3]·3H2O3K2C2O4+2FeC2O4+2CO2↑+6H2O。下列说法错误的是
A.Fe3+的最高能层电子排布式为3d5
B.铁元素位于第4周期VIIIB族
C.C2O42-中C原子的杂化方式为sp2
D.CO2分子中s键和p键数目比为1:1
【答案】AB
【详解】
A.Fe3+的电子排布式为1s22s22p63s23p63d6,最高能层电子排布式为3s23p63d6,A错误;
B.铁原子的电子排布式为1s22s22p63s23p63d64s2,其价电子数为8,则铁元素位于第4周期VIII族,B错误;
C.C2O42-中C原子的价层电子对数为=3,所以杂化方式为sp2,C正确;
D.CO2分子的结构式为O=C=O,s键和p键各为2个,二者的数目比为1:1,D正确。
13.(2020·吴江汾湖高级中学月考)室温下进行下列实验,根据实验操作和现象所得出的结论正确的是( )
选项
实验操作和现象
结论
A
某溶液中加入的Ba(NO3)2溶液,再滴加AgNO3溶液,有白色沉淀生成
溶液中一定含有Cl—
B
用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,铝箔熔化但不滴落
氧化铝的熔点高于铝单质
C
向Na2CO3溶液中加入盐酸,将产生的气体直接通入硅酸钠溶液中,产生白色胶状沉淀
酸性:盐酸>碳酸>硅酸
D
向2 mL 2%的硫酸铜溶液中滴入几滴NaOH溶液,振荡后再加入1 mL有机物X,加热后未出现砖红色沉淀
有机物X中不含醛基
【答案】B
【详解】
A.某溶液中加入的Ba(NO3)2溶液,再滴加AgNO3溶液,有白色沉淀生成,该白色沉淀不一定为AgCl,也可能为BaSO4,则溶液中不一定含有Cl−,故A错误;
B.仔细打磨过的铝箔在酒精灯上加热,表面的铝单质被氧化生成氧化铝,包裹在铝单质的表面,由于氧化铝的熔点高于铝单质,则铝箔熔化但不滴落,故B正确;
C.向Na2CO3溶液中加入盐酸反应生成二氧化碳气体,说明盐酸的酸性强于碳酸,但盐酸易挥发,生成的气体中混有氯化氢气体,将生成的混合气体通入硅酸钠溶液中,氯化氢溶于水形成的盐酸会与硅酸钠反应白色的胶状沉淀硅酸,无法比较碳酸与硅酸的酸性,应将生成的气体通入饱和碳酸氢钠溶液后在通入到硅酸钠溶液中,若产生白色胶状沉淀,说明碳酸的酸性强于硅酸,故C错误;
D.向2mL2%的硫酸铜溶液中滴入几滴NaOH溶液,硫酸铜溶液过量,生成氢氧化铜较少,且检验醛基,应在碱性条件下进行,则振荡后再加入1mL有机物X,加热后未出现砖红色沉淀的原因可能是加入的NaOH溶液的量不足导致,故D错误;
答案选B。
14.(2021·湖南长沙市·雅礼中学高二月考)下列化学实验事实及其解释或结论都正确的是
A.用玻璃棒蘸取新制氯水,滴在pH试纸上,然后与比色卡对照,可测定新制氯水的pH
B.取少量卤代烃Y在碱性溶液中水解,后滴加AgNO3溶液,未看到淡黄色沉淀,说明卤代烃中不含有溴元素
C.向苯酚浊液中滴加Na2CO3溶液,浊液变澄清,说明苯酚的酸性强于H2CO3
D.向少量2%CuSO4溶液中加入过量的10%NaOH溶液,振荡,再加入0.5mL有机物Y,加热,未出现砖红色沉淀,说明Y中不含醛基
【答案】D
【详解】
A.新制氯水具有强氧化性,具有漂白性,用pH试纸无法测出新制氯水的pH,故A错误;
B.卤代烃在碱性溶液中水解,卤素原子转化成卤素离子,需要先加入硝酸酸化,再滴加AgNO3溶液,生成淡黄色沉淀,说明该卤代烃中含有溴元素,故B错误;
C.向苯酚浊液中滴加碳酸钠溶液,浊液变澄清,发生+→+,推出苯酚的酸性强于,故C错误;
D.向少量2%CuSO4溶液中加入过量的10%NaOH溶液,氢氧化钠过量,振荡,再加入0.5mL有机物Y,加热,未出现砖红色沉淀,说明Y中不含有醛基,故D正确;
答案为D。
15.(2021·大名县第一中学高二月考)某石油化工产品X的转化关系如图,下列判断不正确的是
A.X可以发生加聚反应 B.Y能与NaHCO3溶液反应产生CO2
C.Z与CH3OCH3互为同分异构体 D.W的结构简式为CH3COOC2H5
【答案】BC
【详解】
A. X为CH2==CH2,含有碳碳双键,可以发生加聚反应,A正确;
B. Y为CH3CH2OH,含有羟基,而不含羧基,不能与NaHCO3溶液反应生成CO2,B错误;
C.Z为CH3CHO,与CH3OCH3的分子式不同,因此二者不互为同分异构体,C错误;
D. W为乙酸乙酯,结构简式为CH3COOC2H5,D正确;
故选BC;
第II卷
三、非选择题(本大题共5题,共60分。)
16.(2020·陕西咸阳市实验中学高二月考)已知A、B、C、D、M、W六种元素的原子序数依次递增,都位于前四周期。其中A、D原子的最外层电子数均等于其周期序数,且D原子的电子层数是A的3倍;B原子s轨道电子数是p轨道电子数的两倍;C原子L层上有2对成对电子。M和W均有“生物金属”之称,M4+和氩原子的核外电子排布相同;W处于元素周期表中第8列。请回答下列问题:
⑴1 mol B2A2分子中含σ键的数目是________。
⑵BC2在高温高压下所形成的晶体其晶胞如图1所示。则该晶体的类型属于________晶体(填“分子”、“原子”);该晶体中B原子轨道的杂化类型为________。
⑶“生物金属”M的晶胞如图2所示。则晶胞中一个M原子与_____个M原子紧邻;若该晶体的密度为ρ g·cm-3,阿伏加德罗常数为NAmol-1,M原子的摩尔质量为Mrg·mol-1,则该晶胞的“边长”为________cm。
⑷“生物金属”W元素应用广泛,如人体内W元素的含量偏低,则会影响O2在体内的正常运输。已知W2+与KCN溶液反应得W(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成配合物,其配离子结构如图3所示。
①W元素基态原子价电子排布式为________。
②1个CN-中π键数目为________。
⑸光谱证实单质D与强碱溶液反应有[D(OH)4]-生成,则[D(OH)4]-中存在________(填字母)。
a.共价键 b.配位键 c.σ键 d.π键
【答案】3NA(或1.806×1024) 原子 sp3 12 3d64s2 2 abc
【详解】
⑴B2A2分子为C2H2,1 mol C2H2含σ键的数目是3NA(或1.806×1024);故答案为:3NA(或1.806×1024)。
⑵BC2在高温高压下所形成的晶体其晶胞如图,则一个C与周围四个O相连。则该晶体的类型属于原子晶体,该晶体中C原子有四个σ键,其原子轨道的杂化类型为sp3;故答案为:原子;sp3。
⑶“生物金属”M的晶胞如图2所示。Ti是面心立方最密堆积,配位数为12,所以晶胞中一个Ti原子与周围12个Ti原子紧邻,该晶胞中Ti原子个数为;若该晶体的密度为ρ g·cm−3,阿伏加德罗常数为NA mol−1,M原子的摩尔质量为Mr g·mol−1,设晶胞的“边长”为l,根据,则该晶胞的“边长”为;故答案为:。
⑷①Fe是26号元素,元素基态原子价电子排布式为[Ar]3d64s2,价电子排布式为3d64s2;故答案为:3d64s2。
②CN-中是碳氮三键,因此1个CN-中π键数目为2;故答案为:2。
⑸[Al(OH)4]-是Al(OH)3和OH-形成的,含有共价键、配位键和σ键;故答案为:abc。
17.(2021·大连市103中学高二月考)按要求回答问题
(1)某有机化合物的结构简式如下,,写出官能团的名称_______________________;
(2)相对分子质量为84的烃,能使溴水褪色。若该烃分子中所有的碳原子都在同一个平面内,则该烃的结构简式为__________________;名称是___________________ ,该烃和溴化氢加成只能生成一种产物,则满足该要求的烃有____________种。
(3)如图所示的是用燃烧法确定有机物分子式的常用装置。
现准确称取1.8 g样品(只含C、H、O三种元素中的两种或三种),经燃烧后A管增重1.76 g,B管增重0.36 g。请回答:
①根据气流方向将装置进行连接,连接的顺序是__________________________________。
②该有机物的最简式为_________________。
③该有机物蒸汽密度相对于氢气为45,核磁共振氢谱显示只有一组峰,写出结构简式______________。
【答案】羟基、羧基 (CH3)2C=C(CH3)2 2,3-二甲基-2-丁烯 2 g接f,e接h,I接 c或(d),d或(c)接a或(b) CHO2 HOOC-COOH
【详解】
(1)某结构简式如下,,官能团的名称为羟基、羧基。
(2)相对分子质量为84的烃,C原子数目最大值为84÷12=7,能使溴水褪色说明含有不饱和键,若该烃分子中所有的碳原子都在同一个平面内,则该烃的结构简式为:(CH3)2C=C(CH3)2,2,3-二甲基-2-丁烯;如该烃和溴化氢加成只能生成一种产物,含有碳碳双键,且关于碳碳双键对称,符合条件的结构简式有:CH3CH2C = CCH2CH3、(CH3)2C= C(CH3)2。
(3) 1.8 g样品(只含C、H、O三种元素中的两种或三种),经燃烧后A管增重1.76 g,吸收二氧化碳,二氧化碳的物质的量为0.04mol,B管增重0.36 g吸收水,水的物质的量为0.02mol。
①D中生成的氧气中含有水蒸气,应先通过C中的浓硫酸干燥,在F中电炉加热时用纯氧氧化管内样品,生成二氧化碳和水,如有一氧化碳生成,则F中CuO可与CO进一步反应生成二氧化碳,然后分别通入B(吸收水)、A( 吸收二氧化碳)中,根据产物的质量推断有机物的组成,则产生的氧气按从左到右流向,所选置的连接顺序应是:D→C→F→B→A,所选用的各导管口连接的顺序是g接f,e接h,I接c或(d),d或(c)接a或(b),故答案为;g接f,e接h,I接 c或(d),d或(c)接a或(b)。
②A管质量增加1.76g为二氧化碳的质量,可得碳元素的质量:0.48g,B管质量增加0.36g是水的质量,可得氢元素的质量:0.04g,从而可推出含氧元素的质量为:1.8g- 0.48- 0.04= 1.28g,设最简式为CxHyOz,则X:Y:Z=1:1:2即最简式为CHO2,故答案为:CHO2。
③该有机物相对分子质量为90,分子式为C2H2O4核磁共振氢谱显示只有一组峰,结构简式:HOOC-COOH。
18.(2020·长春市·吉林省实验高二期中)某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯
已知: +H2O
密度(g/cm3)
熔点(℃)
沸点(℃)
溶解性
环己醇
0.96
25
161
能溶于水
环己烯
0.81
-103
83
难溶于水
(1)制备粗品:将12.5 mL环己醇加入试管A中,再加入l mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是_________________________。
②导管B除了导气外还具有的作用是_____________。
(2)制备精品:
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在_________层(填上或下),分液后用_________ (填入编号)洗涤。
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按如图装置蒸馏,冷却水应从_________口进入,目的是使冷却水与气体形成逆流方向。
③收集产品时,控制的温度应在_________左右,实验制得的环己烯精品质量低于理论产量,可能的原因是__________。
a.蒸馏时从70 ℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
【答案】防暴沸 冷凝 上 c g 83℃ c
【详解】
(1)①根据制乙烯实验的知识,发生装置A中碎瓷片的作用是防止暴沸;
②导管B比较长,能增加与空气的接触面积,其作用是导气和将生成的气体物质冷凝回流;
(2)①环己烯是烃类,不溶于氯化钠溶液,且密度比水小,振荡、静置、分层后环己烯在上层;环己烯中含有碳碳双键,可以被KMnO4溶液氧化,稀H2SO4不能除去,反而能引入新的酸性杂质,只有Na2CO3溶液,不能与环己烯反应,可以与酸性杂质反应,答案选c;
②冷却水与气体形成逆流,使气体得到充分冷却,则冷却水从冷凝管的下口即g口进入;
③根据表中数据可知,馏分环己烯的沸点为83℃,故收集产品应控制温度在83℃左右;
a.蒸馏时从70℃开始收集产品,提前收集,产品中混有杂质,实际产量高于理论产量,故a错误;
b.环己醇实际用量多了,制取的环己烯的物质的量增大,实验制得的环己烯精品质量高于理论产量,故b错误;
c.若粗产品中混有环己醇,导致测定消耗的环己醇量增大,制得的环己烯精品质量低于理论产量,故c正确;
故答案选c。
19.(2021·河北石家庄市·石家庄二中高二月考)过渡金属单质及化合物具有广泛用途.回答下列问题:
(1)Co基态原子的核外电子排布式为_______。
(2)基态铜原子核外电子占据能级数为_______;核外电子共有_______种不同的运动状态。
(3)向含Fe3+的溶液中滴加少量的KSCN溶液,溶液中生成红色的[Fe(SCN)(H2O)5]2+。
①与N同周期的主族元素中,第一电离能比N大的元素是_______。
②与SCN-互为等电子体的非极性分子的化学式为_______(任写一种)。
(4)化学上可用EDTA测定Fe2+和Co2+的含量EDTA的结构简式如图所示:
EDTA分子中,碳原子的杂化方式为_______,其分子中含有的四种非金属元素的电负性由大到小顺序为_______。
(5)铁、镍易与CO作用形成羰基配合物Fe(CO)5、Ni(CO)4,1mol Ni(CO)4分子中含有σ键数目为_______. Ni(CO)4的中心原子价电子数与配位体提供电子总数之和为_______。
(6)Cr(CO)6是一种典型的羰基配合物.其配体为CO,则Cr(CO)6分子中π键的数目为_______.已知形成Cr(CO)6时,Cr原子的杂化方式为d2sp3,根据原子轨道杂化规律,其杂化后形成的杂化轨道数为_______个,Cr(CO)6的分子立体构型为_______。
(7)硫酸锌溶于氨水可形成[Zn(NH3)4]2+离子,[Zn(NH3)4]2+离子具有对称的空间构型,其中两个NH3被两个Cl取代,只有一种产物,则[Zn(NH3)4]2+的空间构型为_______。
(8)元素铜的第一电离能ICu,元素锌的第一电离能IZn,已知ICu<IZn,其原因是______________________
________________________________________________________________________________________。
【答案】1s22s22p63s23p63d74s2或[Ar]3d74s2 7 29 F CO2、CS2等 sp3、sp2 O>N>C>H 8NA 18 12 6 正八面体 正四面体 Zn外围电子排布式为3d104s2,为全满的稳定结构,较难失去电子
【详解】
(1)Co是27号元素,原子核外有27个电子,核外电子排布式为1s22s22p63s23p63d74s2或[Ar]3d74s2;
(2)Cu是29号元素,基态铜的核外电子排布为1s22s22p63s23p63d104s1,占据7个能级;每个电子的运动状态各不相同,所以核外电子共有29种不同的运动状态;
(3)①同周期元素自左至右第一电离能呈增大趋势,但N的2p轨道半满较稳定,第一电离能大于O,所以与N同周期的主族元素中,第一电离能比N大的元素是F;
②SCN-含有3个原子、16个价电子,正负电子中心重合的分子为非极性分子,所以符合条件的等电子体为CO2、CS2等;
(4)EDTA中亚甲基中的C原子形成4个σ键,为sp3杂化,羧基中C形成C=O双键,为sp2杂化;非金属性越强电负性越大,非金属性O>N>C>H,则电负性O>N>C>H;
(5)Ni与CO形成的配位键为σ键,CO分子中的三键中有一个σ键,所以1mol Ni(CO)4分子中含有σ键数目为8NA;Ni(CO)4分子中心原子为Ni,其价电子排布为3d84s2,价电子数为10,每个CO配体提供一对电子,即2个,所以总和为10+2×4=18;
(6)CO分子中的三键中有2个π键,所以Cr(CO)6分子中π键的数目为6;Cr原子的杂化方式为d2sp3,即2个d轨道、1个s轨道、3个p轨道进行杂化,杂化前后轨道数目不变,所以杂化后形成的杂化轨道数为6,Cr(CO)6分子立体构型为正八面体;
(7)[Zn(NH3)4]2+离子具有对称的空间构型,其中两个NH3被两个Cl取代,只有一种产物,类别甲烷的结构和二氯代物的个数可知[Zn(NH3)4]2+为正四面体;
(8)Cu的外围电子排布式为3d104s1,失去一个电子变为3d10、为能量较低的稳定结构;Zn外围电子排布式为3d104s2,为全满的稳定结构,失去一个电子变为3d104s1、为不稳定结构,所以Cu失去一个电子较容易,Zn失去一个电子较难,即锌的第一电离能大于铜。
20.(2020·江苏扬州市·扬州中学高二期中)化合物G是一种治疗帕金森症的药品,其合成路线流程图如图:
(1)D中的官能团名称为溴原子、____________和____________。
(2)一定条件下,有机物C最多能和_______mol H2反应。
(3)写出同时满足下列条件的D的一种同分异构体的结构简式:_____________________________________。
①分子中只有3种不同化学环境的氢
②能发生银镜反应,苯环上的一取代物只有一种
(4)F通过取代反应得到G,写出G的结构简式:__________________________________。
(5)已知:RCH=CH—NO2RCH2CH2NH2(R代表烃基或H)。
请写出以和CH3NO2为原料制备的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
【答案】碳碳双键 硝基 4 或
【详解】
(1)D()中的官能团有溴原子、碳碳双键、硝基;
(2) C中苯环、醛基都能与氢气发生加成反应,1mol有机物C最多能和4mol H2反应;
(3)D为,其同分异构体满足:
①分子中只有3种不同化学环境的氢,则结构对称;
②能发生银镜反应,说明结构中含有醛基,苯环上的一取代物只有一种,说明结构具有较高的对称性,满足条件的有: 或;
(4)F为,通过取代反应得到G,G的分子式为C16H24N2O,所以应是F中氯原子被H原子替代生成G,碳骨架不变,则G为;
(5) 由D→E的转化,可知由2分子成环生成,结合C→D的转化,给予的信息“RCH=CH-NO2RCH2CH2NH2”,可先用用苯甲醛与CH3NO2/CH3OH反应生成,然后与HBr发生加成反应生成,再与氢气反应生成,而苯甲醇发生催化氧化生成苯甲醛,因此合成路线为。
卷05——高二化学下学期期末模拟测试卷(鲁科版2019): 这是一份卷05——高二化学下学期期末模拟测试卷(鲁科版2019),文件包含卷05高二化学下学期期末模拟测试卷鲁科版2019解析版docx、卷05高二化学下学期期末模拟测试卷鲁科版2019原卷版docx等2份试卷配套教学资源,其中试卷共25页, 欢迎下载使用。
卷04——高二化学下学期期末模拟测试卷(鲁科版2019): 这是一份卷04——高二化学下学期期末模拟测试卷(鲁科版2019),文件包含卷04高二化学下学期期末模拟测试卷鲁科版2019解析版docx、卷04高二化学下学期期末模拟测试卷鲁科版2019原卷版docx等2份试卷配套教学资源,其中试卷共27页, 欢迎下载使用。
卷02——高二化学下学期期末模拟测试卷(鲁科版2019): 这是一份卷02——高二化学下学期期末模拟测试卷(鲁科版2019),文件包含卷02高二化学下学期期末模拟测试卷鲁科版2019解析版docx、卷02高二化学下学期期末模拟测试卷鲁科版2019原卷版docx等2份试卷配套教学资源,其中试卷共25页, 欢迎下载使用。












