




- 专题04 化学能与热能——2022-2023学年高一化学下学期期末专项突破学案(人教版2019必修第二册) 学案 2 次下载
- 专题05 化学能与电能——2022-2023学年高一化学下学期期末专项突破学案(人教版2019必修第二册) 学案 3 次下载
- 专题07 几组有机化学概念的判断——2022-2023学年高一化学下学期期末专项突破学案(人教版2019必修第二册) 学案 4 次下载
- 专题08 官能团的性质与有机物的转化——2022-2023学年高一化学下学期期末专项突破学案(人教版2019必修第二册) 学案 3 次下载
- 专题09 金属与海水资源的开发利用——2022-2023学年高一化学下学期期末专项突破学案(人教版2019必修第二册) 学案 3 次下载
专题06 化学反应速率与平衡思想——2022-2023学年高一化学下学期期末专项突破学案(人教版2019必修第二册)
展开必刷06 化学反应速率与平衡思想(23题)
1.下列措施中,不能加快化学反应速率的是
A.锌与稀硫酸反应制H2时,适当增大压强
B.氮气与氢气合成NH3时,适当升高温度
C.双氧水分解制O2时,加入几滴FeCl3溶液
D.碳酸钙与稀盐酸反应制CO2时,粉碎固体
2.在恒温、体积为2 L的密闭容器中进行反应:2A(g)3B(g)+C(g),若反应物在前20 s由3 mol降为1.8 mol,则前20 s的平均反应速率为
A.v(B)=0.03 mol·L-1·s-1 B.v(B)=0.045 mol·L-1·s-1
C.v(C)=0.03 mol·L-1·s-1 D.v(C)=0.06 mol·L-1·s-1
3.某温度下,浓度都是1mol/L的两种气体X2和Y2,在密闭容器中反应生成气体Z,反应2min后,测得参加反应的X2为0.6mol/L,用Y2表示的反应速率v(Y2)=0.1mol/(L·min),生成的c(Z)为0.4mol/L,则该反应的化学方程式是( )
A.X2+2Y2=2XY2 B.2X2+Y2=2X2Y
C.3X2+Y2=2X3Y D.X2+3Y2=2XY3
4.已知反应,在不同条件下,用不同物质表示其反应速率,分别为
①
②
③
④
则此反应在不同条件下进行最快的是
A.②③ B.①③ C.②④ D.②
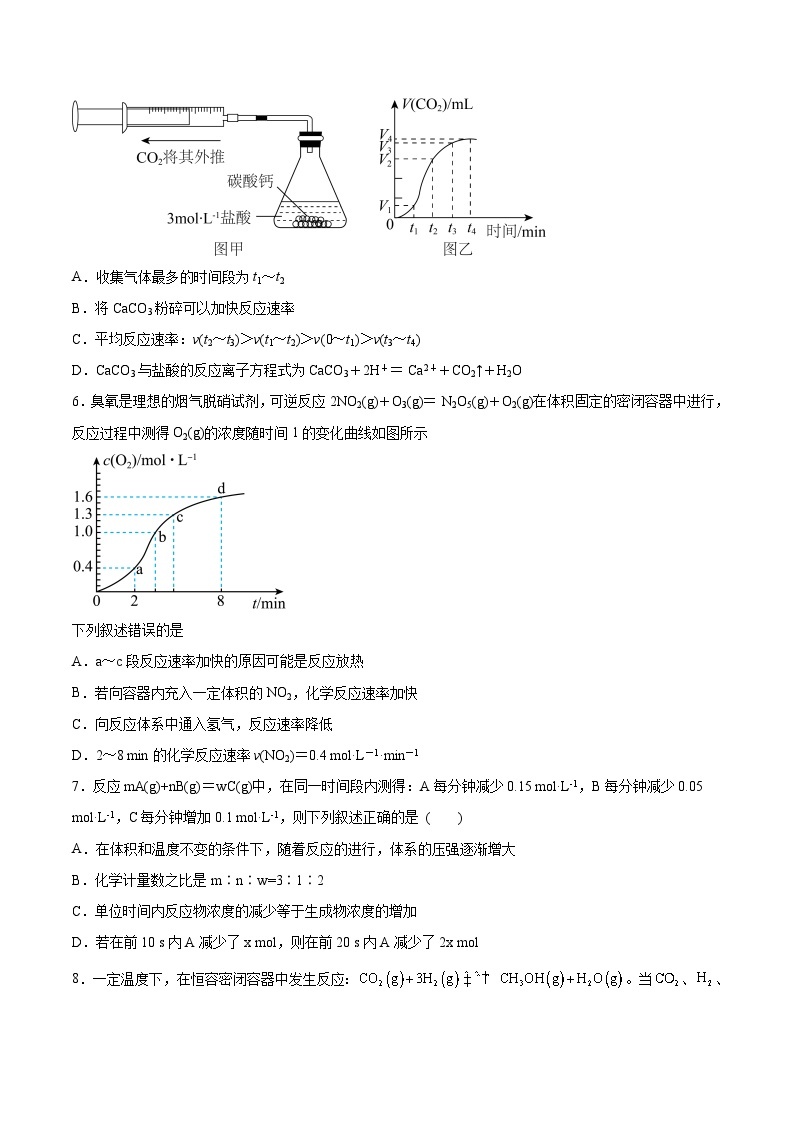
5.某同学用图甲所示装置及器材,测定碳酸盐与一定体积盐酸反应生成V(CO2)随反应时间变化情况,并绘制出图乙所示曲线。有关分析不正确的是
A.收集气体最多的时间段为t1~t2
B.将CaCO3粉碎可以加快反应速率
C.平均反应速率:v(t2~t3)>v(t1~t2)>v(0~t1)>v(t3~t4)
D.CaCO3与盐酸的反应离子方程式为CaCO3+2H+=Ca2++CO2↑+H2O
6.臭氧是理想的烟气脱硝试剂,可逆反应2NO2(g)+O3(g)=N2O5(g)+O2(g)在体积固定的密闭容器中进行,反应过程中测得O2(g)的浓度随时间1的变化曲线如图所示
下列叙述错误的是
A.a~c段反应速率加快的原因可能是反应放热
B.若向容器内充入一定体积的NO2,化学反应速率加快
C.向反应体系中通入氢气,反应速率降低
D.2~8 min的化学反应速率v(NO2)=0.4 mol·L-1·min-1
7.反应mA(g)+nB(g)=wC(g)中,在同一时间段内测得:A每分钟减少0.15 mol·L-1,B每分钟减少0.05 mol·L-1,C每分钟增加0.1 mol·L-1,则下列叙述正确的是 ( )
A.在体积和温度不变的条件下,随着反应的进行,体系的压强逐渐增大
B.化学计量数之比是m∶n∶w=3∶1∶2
C.单位时间内反应物浓度的减少等于生成物浓度的增加
D.若在前10 s内A减少了x mol,则在前20 s内A减少了2x mol
8.一定温度下,在恒容密闭容器中发生反应:。当、、、的浓度不再变化时,下列说法正确的是
A.和全部转化为和
B.该反应已达到化学平衡
C.正、逆反应速率相等且等于零
D.、、、的浓度一定相等
9.在一密闭容器中加入A、B、C三种气体,保持一定温度,在s测得各物质的浓度如表所示。下列结论正确的是( )
测定时刻/s | ||||
6 | 3 | 2 | 2 | |
5 | 3.5 | 3 | 3 | |
1 | 2.5 | 3 | 3 |
A.s时反应已经停止
B.s内正、逆反应速率不相等
C.在容器中发生的反应为
D.s内A的平均反应速率为
10.某温度时,浓度均为的两种气体和,在体积恒定的密闭容器中反应生成气体,4s时、、的浓度分别是、、,若用、表示,则该反应的化学方程式可表示为
A. B.
C. D.
11. (双选)以表面覆盖Cu2Al2O4的二氧化钛为催化剂,可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。
下列说法错误的是
A.400℃时,催化剂的活性最高
B.250~300℃时,温度升高而乙酸生成速率降低的原因是催化剂的催化效率降低
C.300~400℃时,乙酸的生成速率升高的原因是催化剂的催化效率增大
D.300~400℃时,乙酸的生成速率升高的原因是温度升高
12.工业制硫酸中的一步重要反应是:SO2(g)+O2(g)SO3(g)。如果反应在密闭容器中进行,下列说法正确的是
A.恒容下充入Ne(g),该反应速率增大
B.达平衡时,SO2、O2、SO3的浓度相等
C.通过调控反应条件,可以改变反应的限度
D.恒容下混合气体的密度不再变化,则反应达到平衡状态
13.下列标志可表明对应反应达到平衡状态的是
选项 | 反应条件 | 可逆反应 | 标志 |
A | 恒温恒容 | 2SO2(g)+O2(g)2SO3(g) | 混合气体的密度不变 |
B | 恒温恒容 | 2NO(g)+O2(g)2NO2(g) | 混合气体颜色不变 |
C | 恒温恒压 | NH2COONH4(s)2NH3(g)+CO2(g) | NH3在混合气体中的 百分含量不变 |
D | 恒温恒压 | 2NO2(g)N2O4(g) | c(NO2)=2c(N2O4) |
14.在一定温度下,将1 mol A和2 mol B放入容积为5 L的某密闭容器中发生反应:
A(s)+2B(g)⇌C(g)+2D(g)。5 min后达到平衡,测得容器内B的浓度减少了0.2 mol·L-1,则下列叙述不正确的是( )
A.在5 min内该反应用C的浓度变化表示的反应速率为0.02 mol·L-1·min-1
B.平衡时B的转化率为50%
C.平衡时B的体积分数约为33.3%
D.初始时的压强与平衡时的压强比为4:5
15.下列设计的实验方案能达到相应实验目的的是
选项 | 实验目的 | 实验方案 |
A | 探究化学反应的限度 | 取5mL 0.1mol/L KI溶液,滴加0.1mol/L FeCl3溶液5~6滴,充分反应,可根据溶液中既含I2又含I-的实验事实判断该反应是可逆反应 |
B | 比较Mg与Al的金属活动性 | 常温下,将Mg、Al与NaOH溶液组成原电池 |
C | 探究不同催化剂对同一反应速率的影响 | 相同条件下,向两支盛有等体积等浓度H2O2溶液的试管中分别滴入5滴等浓度的CuSO4溶液和FeCl3溶液 |
D | 探究浓度对化学反应速率的影响 | 常温下,相同的铁片中分别加入足量的浓、稀硝酸,浓硝酸中铁片先溶解完 |
16.汽车尾气中产生的反应为。一定条件下,等物质的量的和在恒容密闭容器中反应,如图曲线a、b均表示该反应在温度T下的浓度随时间的变化。下列叙述正确的是( )
A.曲线b达到化学平衡比曲线a快
B.温度T下,随着反应的进行,混合气体的密度减小
C.曲线a可能加入了催化剂
D.反应达到平衡时,曲线a中的转化率更大
17. (双选)工业上可以用CO2来生产甲醇燃料。在体积为2 L的密闭容器中,充入l mol CO2和3 mol H2,一定条件下发生反应CO2(g)+3H2(g)CH3OH(g)+H2O(g)。测得CH3OH和CO2的物质的量随时间变化如图所示。下列描述正确的是
A.达到平衡时,H2的转化率为75%
B.3 min 时,CH3OH和CO2的浓度相等,达到了化学平衡状态
C.反应进行到10 min时,CO2的正逆反应速率相等,反应停止
D.反应开始到10 min,用CO2表示的反应速率为0.0375 mol·L-1·min-1
18.一定条件下,等物质的量的N2和O2在容积为2 L的恒容密闭容器中发生如下反应:N2(g)+O2(g)2NO(g),如图表示该反应过程中N2的物质的量n(N2)随反应时间(t)的变化。下列叙述错误的是
A.升高温度能加快该反应的速率
B.10 s内反应的平均速率为v(O2)=0.05 mol·L-1·s-1
C.10 s末O2的物质的量浓度为2 mol·L-1
D.a点对应的化学反应速率:v正(N2)=v逆(NO)
19.在一定温度下,某容器内的某一反应中,X、Y的物质的量随反应时间的变化曲线如图所示,下列表述正确的是( )
A.t1时,Y的浓度是X的浓度的2倍
B.反应的化学方程式为X2Y
C.t2时,反应的正、逆反应速率相等,达到平衡状态
D.t3时,X、Y的量不再变化,化学反应停止了,正、逆反应速率为零
20.某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
(实验原理)2KMnO4+5H2C2O4+3H2SO4==2MnSO4+10CO2↑+8H2O+K2SO4
(实验内容及记录)
实验编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液褪色至无色所需时间/min | |||
0.6 mol/L H2C2O4溶液 | H2O | 0.1 mol/L KMnO4溶液 | 3 mol/L H2SO4溶液 | ||
1 | 3.0 | 13.0 | 2.0 | 2.0 | 8.0 |
2 | 2.0 | 14.0 | 2.0 | 2.0 | 10.4 |
3 | 1.0 | V1 | V2 | 2.0 | 12.8 |
请回答:
(1)请完成上述实验设计表:V1=_________,V2=__________。
(2)根据上表中的实验数据,可以得到的结论是_________________________________。
(3)利用实验1中数据计算,反应速率为v(KMnO4)=_________________________。
(4)该小组同学依据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。
①该小组同学提出的假设是____________________________________________________。
②请你帮助该小组同学完成实验方案,并填写表中空白。
实验编号 | 室温下,试管中所加试剂及其用量 | 室温下溶液褪色至无色所需时间/min | ||||
0.6 mol/L H2C2O4溶液 | H2O | 0.1 mol/L KMnO4溶液 | 3 mol/L H2SO4溶液 | 少量_____ | ||
4 | 3.0mL | 13.0mL | 2.0mL | 2.0mL | t | |
③若该小组同学提出的假设成立,应观察到的现象是_______________________________。
21.(1)在反应A(g)+3B(g)=2C(g)中,若以物质A表示的该反应的化学反应速率为0.2 mol·L‒1·min‒1,则以物质B表示此反应的化学反应速率为_______ mol·L‒1·min‒1。
(2)在2 L的密闭容器中,充入2 mol N2和3 mol H2,在一定条件下发生反应,3s后测得N2为1.9 mol,则以H2的浓度变化表示的反应速率为_______。
(3)①将10 mol A和5 mol B放入容积为10 L的密闭容器中,某温度下发生反应:3A(g)+B(g)2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L‒1·s‒1,则在2s时,容器中有_______ mol A,此时C的物质的量浓度为_______。
②能说明该反应已达到平衡状态的是_______(填字母)。
a.v(A)=2v(B) b.容器内压强保持不变
c.3v逆(A)=v正(B) d.容器内混合气体的密度保持不变
③在密闭容器里,通入a mol A(g)、b mol B(g)、c mol C(g),发生上述反应,当改变下列条件时,反应速率会减小的是_______(填序号)。
①降低温度 ②加入催化剂 ③增大容器体积
22.CO和N2O是汽车尾气中污染大气的成分。一定条件下,通过下列转化反应:CO(g)+N2O(g)CO2(g)+N2(g)(放热反应),可治理CO和N2O产生的污染。
向体积相同的三个恒容密闭容器中均充入a mol CO(g)和a mol N2O(g)进行下列实验:
实验序号 | 反应温度 | 催化剂 |
Ⅰ | 恒温T1℃ | 无 |
Ⅱ | 恒温T1℃ | 有 |
Ⅲ | 初始温度T1℃,绝热容器 | 无 |
注:绝热容器的反应体系和外界环境无热交换
回答下列问题:
(1)实验Ⅰ、Ⅱ中c(N2)随时间t的变化曲线如下图,实验Ⅰ反应开始至平衡时间段内v(N2O)=___________mol·L-1·min-1。平衡时CO的体积分数:实验Ⅰ___________实验Ⅱ(填“大于”“小于”或“等于”)。
(2)某时刻向实验Ⅱ容器充入一定量X(g),使容器内压强增大。
①若X是CO(g),则反应速率___________(填“变大”“变小”或“不变”);
②若X是Ar(g)(不参与反应),则反应速率___________(填“变大”“变小”或“不变”)。
(3)下列叙述能说明转化反应到达平衡状态的有___________(填标号)。
A.v(CO2)=v(CO)
B.断裂n mol N≡N同时生成n mol CO2
C.的值不变
D.v正(N2O)=2v逆(CO)
E.气体的平均摩尔质量不变
(4)反应一段时间后,发现实验Ⅲ中反应速率增大,其原因是_________________________
_________________。
(5)转化反应CO(g)+N2O(g)CO2(g)+N2(g),在的催化作用下反应历程可分为:
第一步:Fe++N2O(g)=FeO++N2(g);
第二步:FeO++________=________+________(将化学方程式补充完整)。
23.减少氮的氧化物在大气中的排放是环境保护的重要内容。合理应用和处理氮及其化合物,在生产生活中有重要意义。
Ⅰ.雾霾严重影响人们的生活,雾霾的形成与汽车排放的NOx等有毒气体有关。
(1)通过活性炭对汽车尾气进行处理,相关原理为C(s)+2NO(g)N2(g)+CO2(g)。下列情况能说明该反应达到平衡状态的是_______。
A.2v正(NO)=v逆(CO2)
B.混合气体中N2的体积分数保持不变
C.单位时间内断裂1个N≡N同时生成1个C=O
D.恒温、恒容条件下,混合气体的密度保持不变
E.恒温、恒压条件下,混合气体的平均摩尔质量保持不变
(2)在催化转化器中,汽车尾气中CO和NO可发生反应2CO(g)+2NO(g)CO2(g)+N2(g),若在容积为10 L的密闭容器中进行该反应,起始时充入0.4 mol CO、0.2 mol NO,反应在不同条件下进行,反应体系总压强随时间的变化如图所示。
①实验b从开始至平衡时的反应速率v(CO)=_______________________;
②实验a中NO的平衡转化率为_________。
③与实验b相比,实验c改变的条件是_______________。
Ⅱ.为减少汽车尾气的污染,逐步向着新能源汽车发展。肼—空气燃料电池是一种碱性电池,无污染,能量高,有广泛的应用前景,其工作原理如图所示,
(3)回答下列问题:
①该燃料电池中正极通入的物质是_______,负极发生的反应式为____________________。
②电池工作时,OH-移向_______电极(填“a”或“b”)。
③当电池放电转移10 mol电子时,至少消耗燃料肼_______g。
专题08 化学实验题突破——高一化学下学期期末专项突破学案(鲁科版2019必修第二册): 这是一份专题08 化学实验题突破——高一化学下学期期末专项突破学案(鲁科版2019必修第二册),文件包含专题08化学实验题突破高一化学下学期期末专项突破鲁科版2019必修第二册解析版docx、专题08化学实验题突破高一化学下学期期末专项突破鲁科版2019必修第二册原卷版docx等2份学案配套教学资源,其中学案共20页, 欢迎下载使用。
专题06 工艺流程和无机推断题突破——高一化学下学期期末专项突破学案(鲁科版2019必修第二册): 这是一份专题06 工艺流程和无机推断题突破——高一化学下学期期末专项突破学案(鲁科版2019必修第二册),文件包含专题06工艺流程和无机推断题突破高一化学下学期期末专项突破鲁科版2019必修第二册解析版docx、专题06工艺流程和无机推断题突破高一化学下学期期末专项突破鲁科版2019必修第二册原卷版docx等2份学案配套教学资源,其中学案共21页, 欢迎下载使用。
专题03 易错突破——高一化学下学期期末专项突破学案(鲁科版2019必修第二册): 这是一份专题03 易错突破——高一化学下学期期末专项突破学案(鲁科版2019必修第二册),文件包含专题03易错突破高一化学下学期期末专项突破鲁科版2019必修第二册解析版docx、专题03易错突破高一化学下学期期末专项突破鲁科版2019必修第二册原卷版docx等2份学案配套教学资源,其中学案共16页, 欢迎下载使用。












