

2022-2023学年山东省滕州市高一(下)4月期中考试化学试卷及答案解析
展开2022-2023学年山东省滕州市高一(下)4月期中考试化学试卷
1. 2022年12月,中国航天员乘组完成首次在轨交接,中国航天员“天宫”会师创造历史。下列说法不正确的是( )
A. 航天器使用的太阳能电池帆板的主要成分是Si
B. 运载火箭的燃料偏二甲肼(化学式C2H8N2)为共价化合物
C. 天和核心舱的霍尔发动机燃料 54131Xe原子核中含77个中子
D. 航天员的耳机使用的双层蛋白质皮革属于新型无机非金属材料
2. 下列说法正确的是( )
A. 16O、 18O、 3H2是三种不同的核素
B. 23He和 24He互为同位素
C. 16O2、 18O2互为同素异形体
D. 同一元素形成的不同微粒具有相同的化学性质
3. 同一短周期元素X、Y、Z、W形成的最高价含氧酸的酸性依次增强,下列有关叙述正确的是( )
A. 单质沸点:X
C. 原子序数:X>Y>Z>W
D. 最高正价:X
( )
A. 锌电极发生氧化反应
B. H+向锌电极移动
C. 电子由铜电极经导线流向锌电极
D. 原电池工作一段时间后溶液的c(H+)不变
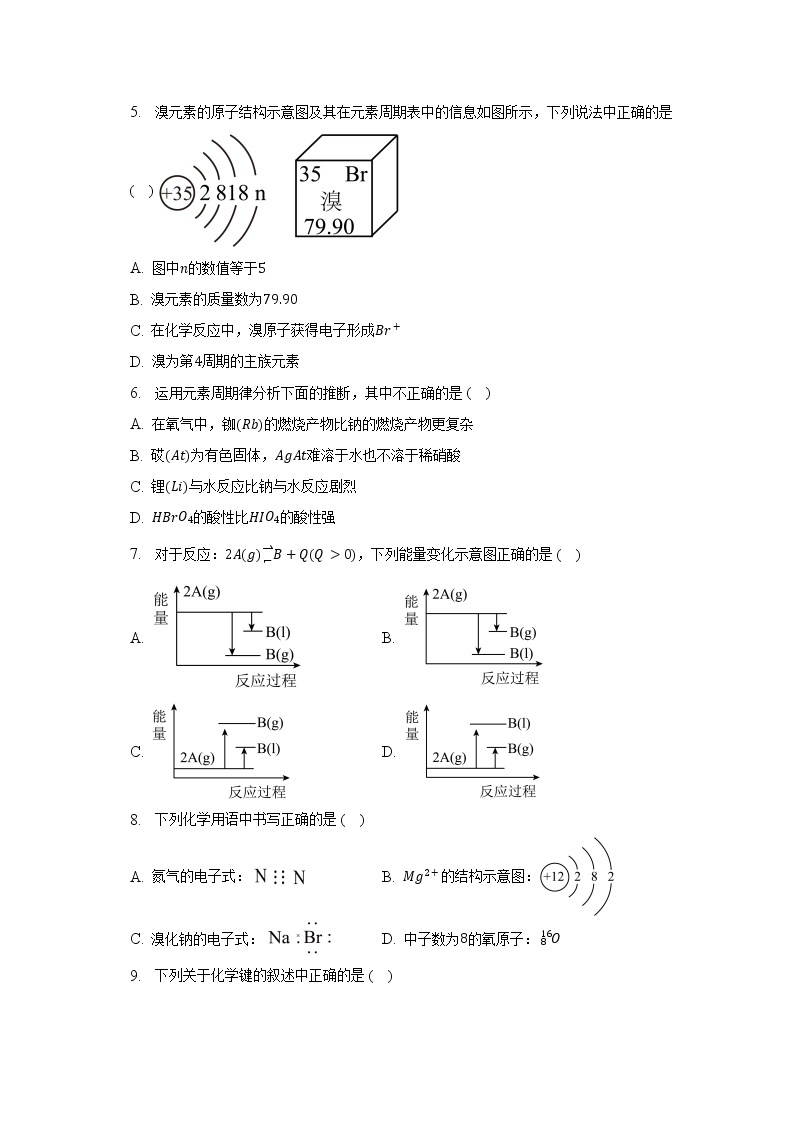
5. 溴元素的原子结构示意图及其在元素周期表中的信息如图所示,下列说法中正确的是( )
A. 图中n的数值等于5
B. 溴元素的质量数为79.90
C. 在化学反应中,溴原子获得电子形成Br+
D. 溴为第4周期的主族元素
6. 运用元素周期律分析下面的推断,其中不正确的是( )
A. 在氧气中,铷(Rb)的燃烧产物比钠的燃烧产物更复杂
B. 砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸
C. 锂(Li)与水反应比钠与水反应剧烈
D. HBrO4的酸性比HIO4的酸性强
7. 对于反应:2Ag⇀↽B+QQ>0,下列能量变化示意图正确的是( )
A. B.
C. D.
8. 下列化学用语中书写正确的是( )
A. 氮气的电子式: B. Mg2+的结构示意图:
C. 溴化钠的电子式: D. 中子数为8的氧原子: 816O
9. 下列关于化学键的叙述中正确的是( )
A. 化学键通常是指相邻的两个或多个原子之间强烈的相互作用
B. 两个原子之间的相互作用叫做化学键
C. 化学键存在于原子之间,也存在于分子之间
D. 离子键是阴、阳离子之间的相互吸引力
10. 2022年诺贝尔化学奖颁给了在“点击化学”领域做出贡献的科学家。我国科研人员发现了一种安全、高效的点击化学试剂FSO2N3。下列关于元素F、S、O、N的说法错误的是( )
A. 简单气态氢化物中最稳定的是HF
B. 元素非金属性最强的是F
C. F原子半径比N原子半径大
D. O元素在周期表中的位置是第2周期第VIA族
11. 如图表示1~18号元素(原子)的结构或性质随核电荷数递增的变化。无法由该图中曲线获知的是( )
A. 电子层数 B. 原子半径 C. 最高化合价 D. 最外层电子数
12. 不能作为卤族元素(氯、溴、碘)非金属性递变规律的判断依据的是
( )
A. 单质的氧化性 B. 氢卤酸的酸性
C. 卤化氢的热稳定性 D. 与氢气化合的难易程度
13. X、Y均为元素周期表中前20号元素,其简单离子的电子层结构相同,下列说法正确的是( )
A. 由 mXa+与 nYb−,得m+a=n−b
B. X2−的还原性一定大于Y−
C. X,Y一定不是同周期元素
D. 若X的原子半径大于Y,则气态氢化物的稳定性HmX一定大于HnY
14. 下列关于元素周期表的说法正确的是( )
A. 副族元素都是金属元素
B. 主族元素都是短周期元素
C. 在元素周期表中,每一纵行就是一个族
D. 元素周期表中每个长周期均包含32种元素
15. 如图所示,若锥形瓶内是水,分液漏斗内的液体也是水,向烧杯内滴加水时,发现U形管内液面左边低于右边,恢复到原温度后液面左边与右边基本相平,则烧杯内的物质是( )
A. 过氧化钠 B. 氧化钠 C. 钠 D. 氯化钠
16. 以下验证元素的金属性、非金属性强弱的实验,所用物品不合理的是( )
A. 比较钾、钠:Na、K、H2O
B. 比较镁、铝:MgCl2溶液、AlCl3溶液、NaOH溶液
C. 比较硫、氯:浓硫酸、高氯酸、pH试纸
D. 比较溴、碘:溴水、KI−淀粉试纸
17. 空气吹出法是目前“海水提溴”的主要方法之一,其工艺流程如图示。下列说法不正确的是( )
A. 步骤④中可用亚硫酸钠溶液代替SO2
B. 步骤③说明Br2具有挥发性
C. 步骤②中氧化0.3mol Br−理论上消耗3.36L氯气
D. 步骤④⑤是为了溴富集
18. 化学是以实验为基础的科学。如图(部分夹持装置省略)所示的实验方案正确的是( )
A
B
C
D
分离NH4Cl和I2固体
获得I2的CCl4溶液
证明非金属性强弱:Cl>C>Si
观察KCl的焰色试验的现象
A. A B. B C. C D. D
19. 科学家已获得了气态N4分子,其结构为正四面体形(如图所示)。已知断裂1molN−N键吸收193kJ能量,断裂1molN≡N键吸收946kJ能量,下列说法正确的是( )
A. N4属于一种新型的化合物
B. N4(g)4N(g)的过程中释放1002kJ能量
C. 1molN4转化为N2时要吸收734kJ能量
D. N4和N2互为同素异形体,N4转化为N2属于化学变化
20. W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数的变化如图。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强。下列说法不正确的是( )
A. 对应的简单离子的半径:X
D. Y的最高价氧化物对应的水化物具有强酸性
21. 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力。如图是元素周期表的一部分,回答下列问题。
B
C
N
O
F
Al
Si
P
S
Cl
Ga
Ge
As
Se
Br
In
Sn
Sb
Te
I
(1)周期表呈现的短周期元素中,次外层电子数等于其他电子层电子数之和的元素是_______(写原子结构示意图);上述周期表呈现的元素中,金属性最强的元素在周期表中处于第_______周期第_______族。
(2)Sn的最高正价为_______,写出Cl的最高价氧化物对应水化物的化学式_______。
(3)比较微粒半径大小:Al_______F;Al3+ _______F−(选填“>”或“<”)。
(4)元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。
①以下关于碱金属,说法不正确的是_______。
A.随电子层数增多,原子半径逐渐增大
B.随着核电荷数的增加,离子的氧化性逐渐增强
C.钾与氧气或水反应比钠的反应剧烈,也比铷、铯的反应更剧烈
D.原子易失去电子,呈现+1价
②原子数相同、价电子总数相同的粒子互称为等电子体。Y、Q是上述周期表中短周期元素,元素相关信息见下表。
Q
与H可形成QH3的10电子结构分子
Y
带两个负电荷的负离子与氖原子结构相同
硼元素与Y、Q形成互为等电子体负离子:BY2−、BQ2m−,则m值为_______。
22. 某同学设计实验以探究元素性质的递变规律,实验装置如图所示。
实验Ⅰ:根据元素最高价含氧酸的酸性强弱探究元素非金属性递变规律。已知A装置的烧瓶里装有大理石,分液漏斗里装有稀HNO3,B装置中装有饱和碳酸氢钠溶液,装置C中装有Na2SiO3溶液,试回答:
(1)A中反应的离子方程式为___________,C中可观察到的现象是___________
(2)B装置的作用是___________
(3)根据实验现象推知,碳酸、硝酸、硅酸的酸性强弱顺序是___________,由此得出碳、硅、氮三种元素非金属性的强弱顺序是___________
实验Ⅱ:已知常温下高锰酸钾与浓盐酸混合可产生氯气,利用该装置探究氯和溴元素的非金属性强弱。
(4)写出B装置中发生反应的离子方程式:___________
(5)C装置的作用是___________
(6)实验结论:氧化性___________,非金属性:___________
23. 现代社会的一切活动都离不开能量,化学反应在发生物质变化的同时伴随有能量变化,能量、速率与限度是认识和研究化学反应的重要视角。
(1)已知破坏1molH—H、1molO=O、1molH—O时分别需要吸收436kJ、498kJ、465kJ的能量。如图表示H2、O2转化为水反应过程的能量变化,则b表示的能量为_______。
(2)氢氧燃料电池是用于驱动电动汽车的理想能源。如图为电池示意图,该电池电极表面镀了一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:
①电池的负极反应物为_______。
②电池工作时K+向 _______移动(填“正极”或“负极”)。
③电池工作一段时间后电解质溶液的pH_______(填“增大”“减小”或“不变”)。
24. 海洋植物中富含一种人体必需的微量元素——碘。实验室模拟从海带中提取碘单质的流程图如下:
(1)提碘的原料一般选择海带或海藻,是因为_______。
(2)在实验室里把有机碘化物转化为碘离子往往需要灼烧操作,灼烧海带需要在_______中进行。
(3)若从绿色化学角度考虑,①处选Cl2不好的原因是 _______。
(4)操作I中,实验室可用如图仪器将I2富集到有机溶液X,该步操作的名称为_______;如图中所选用的有机溶剂可以是_______(选填编号)。
a.酒精 b.醋酸 c.四氯化碳 d.苯
(5)操作I中具体实验步骤为:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.检验分液漏斗旋塞和上口的瓶塞是否漏液;
C.把20mL碘水跟5mL四氯化碳加入分液漏斗中,并盖好玻璃塞;
D.倒转漏斗振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.旋开活塞,用烧杯接收下层溶液;
F.将分液漏斗。上口的玻璃塞打开或使塞上的凹槽对准分液漏斗口上的小孔;
G.从分液漏斗上口倒出上层溶液;
H.静止、分层。
实验步骤的正确顺序为_____→_____→_____→A→H→_____→_____→_____。
(6)为寻找氯水的替代品,某同学设计了如下实验来证明H2O2能否代替氯水。实验操作:将H2O2作为氧化剂滴加入溶液A中,取少量反应后的溶液于试管中,_______,则证明H2O2能代替氯水。请写出此反应的离子方程式 _______。
答案和解析
1.【答案】D
【解析】A.太阳能电池帆板的主要成分是硅单质,A正确;
B.运载火箭的燃料偏二甲肼(化学式 C2H8N2 )中各原子间均以共价键相结合,故为共价化合物,B正确;
C. 54131Xe 原子核中含131−54=77个中子,C正确;
D.蛋白皮革主要成分为蛋由质,其属于有机物,D错误;
故选D。
2.【答案】B
【解析】A. 3H2 是单质,不是核素,故A错误;
B. 23He 和 24He 质子数相同,中子数不等,互为同位素,故B正确;
C. 16O2 、 18O2 为氧气的两种不同分子微粒,不是同素异形体,故C错误;
D.同一元素形成的不同微粒化学性质不一定相同,如Na具有较强的还原性,而Na+没有还原性,只有弱氧化性,故D错误;
故选B。
3.【答案】D
【解析】同周期元素从左到右元素的非金属性依次增强,元素的非金属性越强,对应的最高价含氧酸的酸性越强,同一短周期元素X、Y、Z、W形成的最高价含氧酸的酸性依次增强,可说明非金属性X
B. 非金属性X
4.【答案】A
【解析】锌的活泼性比铜的活泼性大,电解质溶液为稀硫酸溶液,锌为负极,铜为正极。
A.锌电极为负极,失去电子,发生氧化反应,故A正确;
B.根据原电池“同性相吸”,则 H+ 向正极即Cu电极移动,故B错误;
C.电子由负极(Zn)电极经导线流向正极(Cu)电极,故C错误;
D.正极是氢离子得到电子变为氢气,因此原电池工作一段时间后溶液的 c(H+) 减小,故D错误;
故选A。
5.【答案】D
【解析】A.核电荷数等于核外电子数,故n=7,A错误;
B.溴元素的相对原子质量为79.90,B错误;
C.溴原子的最外层电子数为7,容易得到一个电子形成Br−,C错误;
D.溴为第4周期VIIA族元素,是主族元素,D正确;
故选D。
6.【答案】C
【解析】A.碱金属元素从上到下元素的金属性逐渐增强,金属性越强在氧气中燃烧的产物越复杂,金属铷比金属钠更活泼,因此铷(Rb)的燃烧产物比钠的燃烧产物更复杂,故 A正确;
B.卤族元素的单质从上到下颜色逐渐加深,碘单质为有色固体,所以砹(At)也为有色固体,溴化银和碘化银难溶于水也不溶于稀硝酸,所以AgAt难溶于水也不溶于稀硝酸,故B正确;
C.元素的金属性越强,对应的单质与水反应越剧烈,金属性:Na>Li,则钠与水反应比锂与水反应剧烈,故C错误;
D.元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,非金属性:Br>I,则HBrO4的酸性比HIO4的酸性强,故D正确;
故选C。
7.【答案】B
【解析】对于反应: 2Ag⇌Bg+QQ>0 ,该反应是放热反应,由于B(l)的能量比B(g)的能量低,因此 2A(g)→B(1) 放出的热量更多,故B符合题意。
故选B。
8.【答案】D
【解析】A.氮气的电子式:,故A错误;
B. Mg2+ 的结构示意图:,故B错误;
C.溴化钠是离子化合物,其电子式:,故C错误;
D.中子数为8的氧原子,其质量数为16,其原子符号: 816O ,故D正确;
故选D。
9.【答案】A
【解析】A.化学键通常是指相邻的两个或多个原子之间强烈的相互作用,故A正确;
B.化学键通常是指相邻的两个或多个原子之间强烈的相互作用,故B错误;
C.化学键只存在于相邻的两个或多个原子之间,不存在于分子之间,故C错误;
D.离子键是相邻的阴、阳离子之间的强烈的相互作用,不仅包括相互吸引力还包括相互排斥力,故D错误;
故选A。
10.【答案】C
【解析】A.F的非金属性最强,因此简单气态氢化物中最稳定的是HF,故A正确;
B.在整个元素周期表中F元素的非金属性最强,故B正确;
C.根据同电子层结构核多径小,则F原子半径比N原子半径小,故C错误;
D.O元素是8号元素,O原子核外电子排布为2、6,则O元素在周期表中的位置是第2周期第VIA族,故D正确;
故选C。
11.【答案】B
【解析】电子层数等于周期数,最外层电子数=最高化合价;同周期元素从左到右,半径依次减小,所以由该图中曲线无法获知的是原子半径,故选B。
12.【答案】B
【解析】非金属性比较的方法:
1.元素在周期表中的相对位置如:同主族元素自上而下,非金属性依次减弱,如F>CI>Br> I;
2.非金属单质与氢气化合的越容易,非金属性越强如:F2、Cl2、Br2、I2与H2化合由易到难,所以非金属性F>C1>Br>I;
3.气态氢化物的越稳定,非金属性越强如:稳定性HBr>HI>所以非金属性:Br>I;
4.最高价氧化物对应的水化物的酸性越强,非金属性越强如酸性:HClO4> HBrO4>则非金属性:Cl>Br;
5.非金属性强的元素的单质能置换出非金属性弱的元素的单质,Cl2+2NaBr=2NaCl+Br2;以此来解析;
A.非金属性越强,单质氧化性越强,则Cl2、Br2、I2的氧化性能作为Cl、Br、 I元素非
金属性递变规律的判断依据,故A不符合题意;
B.氢卤酸的酸性非金属性强弱无关,其酸性强弱不能作为Cl、Br、I元素非金属性递变规律的判断依据,故B符合题意;
C. HCl、HBr、HI的热稳定性与非金属性强弱有关,其氢化物稳定性能作为Cl、Br、I元素非金属性递变规律的判断依据,故C不符合题意;
D.与氢气化合的难易程度与非金属性强弱有关,与氢气化合的难易能作为Cl、Br、I元素非金属性递变规律的判断依据,故D不符合题意;
故选B。
13.【答案】B
【解析】A.由 mXa+与 nYb−,离子的电子层结构相同,则核外电子数相同,所以m−a=n+b,故A错误;
B.简单离子的电子层结构相同,X、Y位于同周期,为非金属元素,Y的原子序数大,则X2−的还原性一定大于Y−,故B正确;
C.简单离子的电子层结构相同,X、Y均为阴离子、或均为阳离子在同一周期,若一个为阳离子一个为阴离子,则一定不在同一周期,故C错误;
D.简单离子的电子层结构相同,X的原子半径大于Y,X可能为金属,则不存在气态氢化物,故D错误;
故选B。
14.【答案】A
【解析】A.副族元素在第3纵行到7纵行,第11纵行到12纵行,都是金属元素。故A正确;
B.主族元素有短周期元素,也有长周期元素,故B错误;
C.在元素周期表中,18个纵行,但只有16个族,第8、9、10三个纵行为第VIII族,故C错误;
D.元素周期表中第4周期、第5周期包含18种元素,第6周期、第7周期包含32种元素,故D错误;
故选A。
15.【答案】B
【解析】若锥形瓶内是水,分液漏斗内的液体也是水,向烧杯内滴加水时,发现U形管内液面左边低于右边,说明反应放热,锥形瓶中气体受热膨胀,恢复到原温度后液面左边与右边基本相平,说明冷却后锥形瓶中压强恢复原来状况,则反应过程中没有气体生成,据此分析。
A. 过氧化钠溶于水放出热量并生成氧气,使容器内温度升高,压强增大,U形管内液体慢慢右移,由于反应生成氧气,锥形瓶中气体增多,压强变大,所以恢复到原温度后液面左边仍然比右边低,故A错误;
B. 氧化钠与水反应放出热量,使容器内温度升高,压强增大,U形管内液体慢慢右移,反应中没有气体生成,恢复到原温度后液面左边与右边基本相平,故B正确;
C. 钠加入水中放热并生成氢气,使容器内温度升高,压强增大,U形管内液体慢慢右移,但恢复到原温度后液面左边仍然比右边低,故C错误;
D. 氯化钠与水不反应,溶于水热效应不明显,故U形管内液体几乎不移动,故D错误。
故选:B。
16.【答案】C
【解析】A.元素的金属性越强,金属单质与水反应越剧烈,则可以比较钾、钠与水反应的剧烈程度判断元素的金属性强弱,故A正确;
B.元素的金属性越强,氢氧化物的碱性越强,氢氧化镁不溶于氢氧化钠溶液,氢氧化铝能溶于氢氧化钠溶液,说明氢氧化镁的碱性强于氢氧化铝,镁元素的金属性强于铝元素,故B正确;
C.浓硫酸可以使试纸脱水碳化,故不能用pH试纸测定浓硫酸的酸性,故C错误;
D.非金属单质的氧化性越强,元素的非金属性越强,溴水与碘化钾发生置换反应生成碘,生成的碘遇淀粉变蓝色,试纸变蓝色说明溴单质的氧化性大于碘单质,溴元素的非金属性强于碘元素,故D正确;
故选C。
17.【答案】C
【解析】苦卤中含有溴离子,在酸性条件下通入氯气,可发生置换反应生成溴单质,吹入空气,将溴单质分离出来,然后溴单质与二氧化硫发生反应生成HBr和硫酸,再通入氯气,生成溴单质,然后通过蒸馏、分液得到液溴。
A.Na2SO3也可以被溴氧化,吸收溴,故步骤④中可用亚硫酸钠溶液代替SO2,A项正确;
B.可用空气吹出Br2,则步骤③说明Br2具有挥发性,B项正确;
C.氯气存在温度压强未知,无法判断氯气的体积,C项错误;
D.步骤③已将Br2吹出,步骤④又重新用SO2的水溶液吸收Br2,步骤⑤再用氯气将HBr氧化为Br2,故步骤④⑤的目的是提高溴的含量,即富集溴,D项正确;
故选C。
18.【答案】B
【解析】A.氯化铵受热分解生成氨气和氯化氢,氯化氢和氨气在冷处反应生成氯化铵,单质碘易升华,因此不能用加热法分离 NH4Cl 和I2固体,故A不符合题意;
B.单质碘易溶于四氯化碳,用萃取法萃取碘水中的单质碘,再分液,故B符合题意;
C.盐酸易挥发,盐酸和碳酸钠反应生成二氧化碳,二氧化碳气体中混有HCl,而且因此使硅酸钠生成硅酸的可能是二氧化碳,也可能是HCl,HCl不是Cl的最高价含氧酸,因此不能得出非金属性强弱C>Si,故C不符合题意;
D.观察KCl的焰色试验的现象应透过蓝色钴玻璃片观察,故D不符合题意;
故选B。
19.【答案】D
【解析】A. N4 属于一种新型的单质,A项错误;
B. N4(g)4N(g) 的过程中吸收的能量为 6×193kJ=1158kJ ,B项错误;
C. 1mol N4 转化为 N2 时的能量变化为 6×193kJ−2×946kJ=−734kJ ,即放出734kJ能量,C项错误;
D. N4 和 N2 均为氮元素形成的单质,互为同素异形体, N4 转化为 N2 属于化学变化,D项正确。
20.【答案】D
【解析】由图象和题干描述可知,W为O元素,X为Na元素,Y为Si元素,Z为Cl元素,据此回答。
A.O2−、Na+离子电子层结构相同,核电荷数越大,离子半径越小,故离子半径:O2−>Na+,A正确;
B.非金属性Si
D.Y的最高价氧化物对应的水化物为H2SiO3,为弱酸,D错误;
故选D。
21.【答案】(1);五;ⅢA
(2)+4;HClO4
(3)>;<
(4)①BC
②3
【解析】(1)短周期元素中,次外层电子数等于其他电子层电子数之和的元素是S元素,S的原子序数为16,核外有3个电子层,每一个电子层上排布的电子数为分别2、8、6,其原子结构示意图为;同周期从左到右元素的金属性逐渐减弱,同主族从上到下元素的金属性逐渐增强,则上述周期表呈现的元素中,金属性最强的元素为In,与Al同主族,在Al的下面2个周期,则In在元素周期表中的位置为第五周期第ⅢA族;
(2)Sn位于第ⅣA族,最外层电子数为4,最高正价为+4价;Cl的最高价氧化物对应的水化物为高氯酸,其化学式为HClO4;
(3)电子层数越多,原子半径越大,Al有3个电子层,F有2个电子层,因此原子半径:Al>F;电子层数相同时,核电荷数越大,微粒半径越小,Al3+和F−均有2个电子层,Al的核电荷数比F大,因此离子半径:Al3+
B.碱金属的还原性越强,其离子越难被还原成金属单质,氧化性越弱,因此随着核电荷数的增加,碱金属的还原性增强,离子的氧化性逐渐减弱,故B错误;
C.铷、铯的金属性比钾强,则铷、铯与氧气或水反应比钾更剧烈,故C错误;
D.碱金属的最外层电子数均为1,容易失去1个电子形成+1价阳离子,故D正确;
故选BC;
②Q与H可形成QH3的10电子结构分子,H含有1个电子,则Q含有7个电子,Q为N元素,Y带两个负电荷的负离子与氖原子结构相同,则Y为O元素, BY2− 为 BO2− ,其价电子数为16, BQ2m− 为 BN2m− ,3+5×2+m=16,解得m=3。
22.【答案】(1)CaCO3+2H+=Ca2++CO2↑+H2O;溶液变浑浊
(2)除去二氧化碳中混有的硝酸蒸气
(3)HNO3>H2CO3>H2SiO3;N>C>Si
(4)Cl2+2Br−=Br2+2Cl−
(5)吸收尾气,防止氯气污染环境
(6) Cl2>Br2;Cl>Br
【解析】(1)A中硝酸与碳酸钙反应产生二氧化碳:CaCO3+2HNO3=Ca(NO3)2+CO2↑+H2O,证明碳酸的酸性比硅酸强,C中发生反应:Na2SiO3+CO2+H2O=H2SiO3↓+Na2CO3或Na2SiO3+2CO2+2H2O===2NaHCO3+H2SiO3↓,因此C中产生白色沉淀或溶液变浑浊。
(2)由于硝酸具有挥发性,为避免硝酸与硅酸钠反应而干扰二氧化碳与硅酸钠溶液反应,必须净化二氧化碳,利用饱和碳酸氢钠溶液吸收硝酸蒸气。
(3)由实验现象可知三种酸中,硝酸酸性最强,硅酸酸性最弱,即HNO3>H2CO3>H2SiO3;元素的非金属性越强,最高价含氧酸的酸性就越强,由此推知,氮的非金属性最强,硅的非金属性最弱,即非金属性:N>C>Si。
(4)题目已限制探究氯与溴的非金属性强弱,所以B中应装溴化钾或溴化钠溶液,氯气能够置换出溴,离子方程式为:Cl2+2Br−=Br2+2Cl−。
(5)氯气能够与碱反应,由于尾气中含有氯气,故要用碱溶液吸收,以避免污染环境。
(6)根据置换反应可得出单质的氧化性强弱:Cl2>Br2;单质的氧化性越强,元素的非金属性越强,所以非金属性:Cl>Br。
23.【答案】(1)490 kJ
(2)①H2
②正极
③减小
【解析】(1)已知破坏1 mol H—H、1 mol O=O、1 mol H—O时分别需要吸收436 kJ、498 kJ、465 kJ的能量,则b=465 kJ×4−436 kJ×2−498 kJ=490kJ;
(2)从图中可以看出,通H2的电极为负极,通O2的电极为正极。
①电池的负极,H2失电子产物与电解质反应生成水;
②电池工作时,阳离子向正极移动,则K+ 向正极移动;
③电池工作一段时间后,n(OH−)不变,但H2O的质量增大,溶液的体积增大,所以c(OH−)减小,电解质溶液的pH减小。
24.【答案】(1)海带或海藻中碘元素的含量高,且原料便宜
(2)坩埚
(3)氯气有毒,易对空气造成污染
(4)萃取分液;c
(5)B;C;D;F;E;G
(6)滴加淀粉溶液,若溶液变蓝或者加入CCl4振荡,若下层呈紫色;H2O2+2I−+2H+=I2+2H2O
【解析】干海带经过灼烧后浸泡过滤获得含有碘离子的溶液A,加稀硫酸酸化后通入氯气将碘离子氧化成碘单质。向溶液B中加入有机溶剂萃取水中的碘单质后分液获得有机溶液X,再蒸馏获得碘单质。
(1)海带或海藻中碘元素的含量高,且原料便宜,故提碘的原料一般选择海带或海藻;
(2)灼烧海带需要在坩埚中进行,还需要酒精灯和泥三角;
(3)若从绿色化学角度考虑,①处选Cl2不好的原因是氯气有毒,易对空气造成污染。
(4)操作I中,实验室可用如图仪器将I2富集到有机溶液X,该步操作的名称为萃取分液;
a.酒精和水互溶,不能做萃取剂,a错误;
b.醋酸和水互溶,不能做萃取剂,b错误;
c.四氯化碳与水互不相溶且不反应,密度比水大在下层,c正确;
d.苯与水互不相溶且不反应,但密度比水小在上层,d错误;
故选c;
(5)操作为查漏→装液→振荡→静置→分液,则步骤为B→C→D→A→H→F→E→G;
(6)将H2O2作为氧化剂滴加入溶液A中,取少量反应后的溶液于试管中,滴加淀粉溶液,若溶液变蓝或者加入CCl4振荡,若下层呈紫色,则证明H2O2能代替氯水,双氧水与碘离子发生的反应:H2O2+2I−+2H+=I2+2H2O。
山东省枣庄市滕州市2023-2024学年高一上学期期中考试化学试题含答案: 这是一份山东省枣庄市滕州市2023-2024学年高一上学期期中考试化学试题含答案,共19页。试卷主要包含了试卷时长90分钟,满分100分,1mlFe在0, 现需配制1L含浓度均为0等内容,欢迎下载使用。
山东省滕州市2021-2022学年高一下学期期中考试化学试题: 这是一份山东省滕州市2021-2022学年高一下学期期中考试化学试题,共8页。试卷主要包含了 下列说法正确的是, 下列关于化学键的叙述错误的是等内容,欢迎下载使用。
2021-2022学年山东省滕州市第一中学高一(下)月考化学试卷(3月)(含答案解析): 这是一份2021-2022学年山东省滕州市第一中学高一(下)月考化学试卷(3月)(含答案解析),共11页。试卷主要包含了 下列化学用语表达正确的是,8mlB等内容,欢迎下载使用。












