




初中化学中考复习 中考化学总复习优化设计第一板块基础知识过关第三单元物质构成的奥秘课件
展开一、物质的构成1.分子(1)定义。分子是保持物质化学性质的最小粒子。(2)分子的基本性质。①质量和体积都很小。②分子在不停地运动。温度越高,分子运动越快。③分子之间有间隔。④同种物质的分子化学性质相同,不同种物质的分子化学性质不同。(3)相对分子质量。化学式中各原子的相对原子质量的总和。(4)分子观点的应用。①运用分子观点解释生活中常见的现象:我们可用分子来解释物质的扩散、溶解、蒸发、挥发等现象;用分子间的间隙解释物质的“三态”变化等。
②运用分子观点解释某些概念。a.物理变化和化学变化。由分子构成的物质,发生物理变化时分子本身未变,发生化学变化时分子本身发生了变化,变成了其他物质的分子。如水变成水蒸气,水分子本身没有变,只是分子间的间隔变大,这是物理变化;水通直流电,水分子发生了变化,生成了氢分子和氧分子,这是化学变化。b.纯净物和混合物。由同种分子构成的物质是纯净物,如水是由水分子构成的,它的组成和性质是固定的;不同种分子构成的物质是混合物,如空气是由氮气分子、氧气分子等构成的,它的组成不固定,混合物中各物质仍保持各自原来的性质。
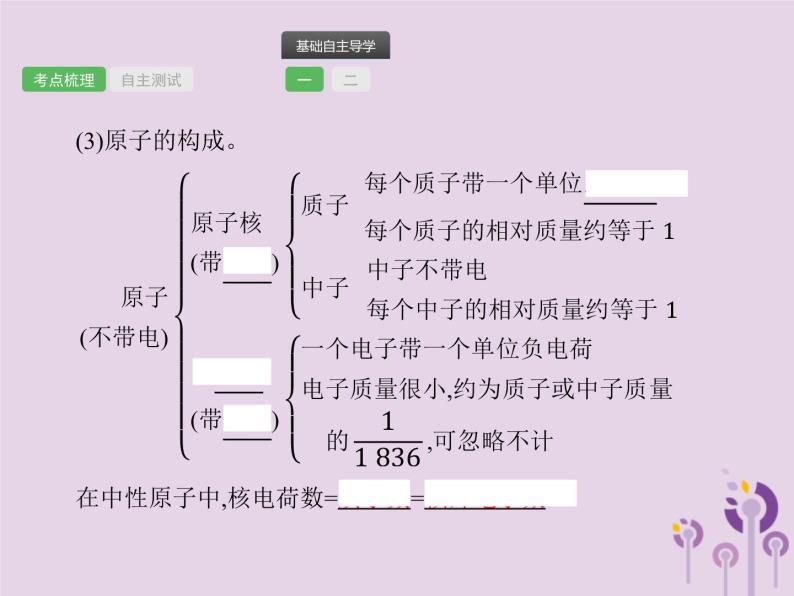
2.原子(1)定义。原子是化学变化中的最小粒子。(2)原子的基本性质。①原子的体积和质量都很小。②原子在不断运动。③原子之间有一定的间隔。④原子在化学变化中不可再分,只是重新组合。
在中性原子中,核电荷数=质子数=核外电子数
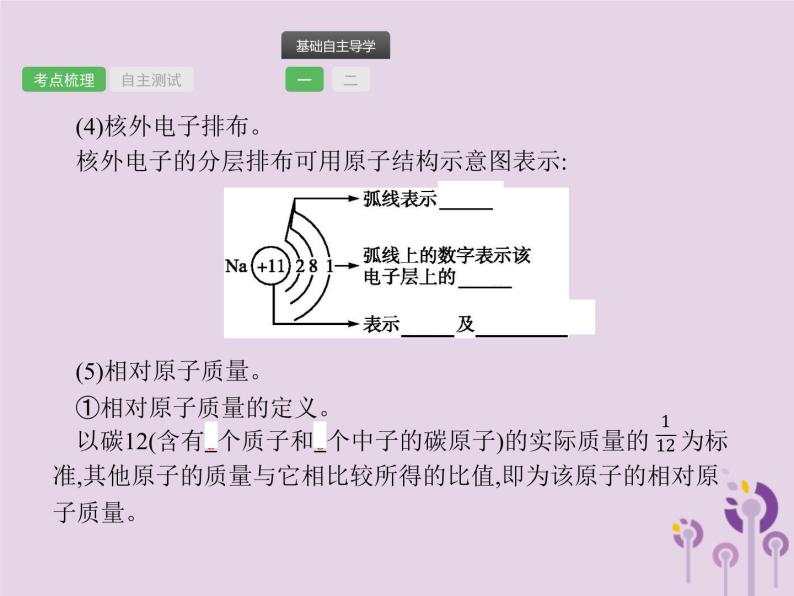
(4)核外电子排布。核外电子的分层排布可用原子结构示意图表示:(5)相对原子质量。①相对原子质量的定义。以碳12(含有6个质子和6个中子的碳原子)的实际质量的 为标准,其他原子的质量与它相比较所得的比值,即为该原子的相对原子质量。
②求算公式。③原子的近似相对原子质量。近似相对原子质量=质子数+中子数
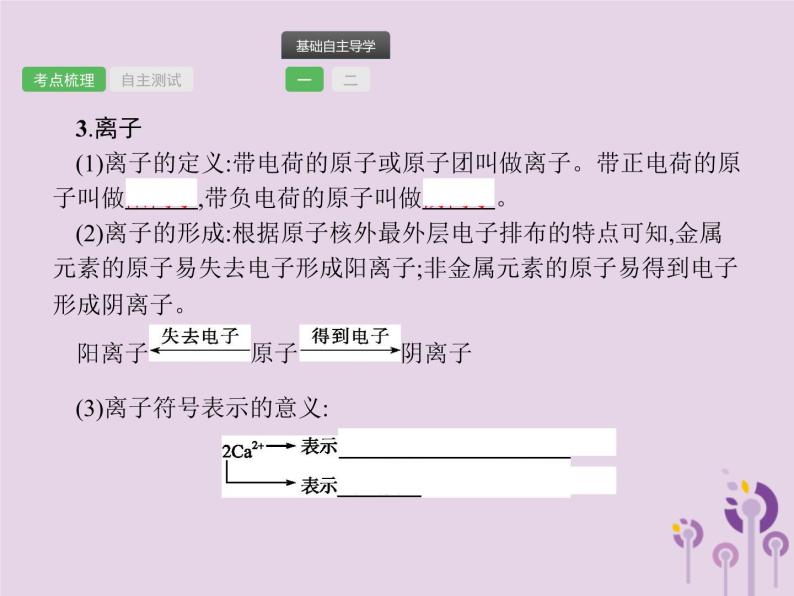
3.离子(1)离子的定义:带电荷的原子或原子团叫做离子。带正电荷的原子叫做阳离子,带负电荷的原子叫做阴离子。(2)离子的形成:根据原子核外最外层电子排布的特点可知,金属元素的原子易失去电子形成阳离子;非金属元素的原子易得到电子形成阴离子。(3)离子符号表示的意义:
二、物质的组成1.元素(1)元素定义。元素是具有相同核电荷数(即核内质子数)的一类原子的总称。(2)地壳中元素的含量(质量分数)占前四位的是氧、硅、铝、铁。(3)元素符号的意义。②对于单质是由单原子构成的,还表示这种单质。
③元素符号前面加上数字时,只能表示原子,如:2N只能表示两个氮原子。2.元素周期表(1)元素周期表的结构:共有7个横行,18个纵行。每一个横行叫做一个周期,每1个纵行叫做一个族(8、9、10三个纵行共同组成一个族)。(2)原子序数:为了便于查找,元素周期表按元素原子核电荷数递增的顺序给元素编了号,叫做原子序数。原子中,原子序数=核电荷数=质子数=核外电子数。(3)元素周期表中对金属元素、非金属元素用不同的颜色做了区分,并标明了元素的相对原子质量。
(4)每一格(以氢元素为例):
1.下列关于分子、原子、离子的说法不正确的是( )A.二氧化碳、水、氨气都是由分子构成的物质B.氯化钠、硫酸铜都是由离子构成的物质C.铁、铜、汞等金属单质都是由原子构成的物质D.氧气、硅、金刚石等非金属单质都是由分子构成的物质解析:硅、金刚石是由原子构成的单质,D项错误。答案:D
2.下列关于原子的叙述正确的是( )①一切原子都是由质子、中子和电子构成的②原子总是在不断运动着③原子是化学变化中的最小粒子④原子由原子核和核外电子构成⑤原子中不存在电荷,因而原子不带电A.②③④B.①②④C.①③⑤D.①②③④⑤
解析:有的原子核中没有中子,例如氢原子中没有中子,所以①说法错误;原子和分子都在不断运动着,所以②说法正确;化学变化中分子分成原子,原子再重新组合成新的分子,所以说原子是化学变化中的最小粒子,所以③说法正确;原子由原子核和核外电子构成,所以④说法正确;原子核中的质子带正电荷,核外电子带负电荷,所以⑤说法错误。答案:A
3.对下列一些事实的解释不正确的是( )
解析:由于原子间有间隔,汞原子的间隔随温度的升高而增大,随温度的降低而减小,所以,温度计中的水银热胀冷缩,原子的大小并没有发生变化。答案:C
4.某药品说明书中标明:本品每克含碘150 mg,镁65 mg,铜2 mg,锌1.5 mg,锰1 mg。这里所标的各成分是指( )A.分子B.原子C.元素D.离子解析:碘、镁、锌、铜、锰分别是指具有相同质子数的一类原子的统称,故这里所标的各成分是指元素。答案:C
5.下列说法中正确的是( )A.当水结成冰时,分子的运动就停止了B.电子数相同的微粒化学性质相同C.分子都是由不同原子构成的
解析:A.水结成冰后不再流动,是由于水由液态变成固体,分子还是在不断地运动,故错误;B.原子核外最外层电子数决定元素的化学性质,而不是电子数,如钠离子和氖原子的电子数相同,但化学性质不同,故错误;C.分子可以是由同种原子构成的,如H2,也可以是由不同种原子构成的,如H2O,故错误;D.质子数决定了元素的种类,由微粒结构示意图可知,二者具有相同的质子数和不同的电子数,所以属于同种元素的不同微粒,故正确。答案:D
6.根据下列微粒的结构示意图,回答下列问题。
(1)图中共表示了 种元素的微粒,其中表示阴离子的是 (填序号),其离子符号为 ,其中表示稀有气体原子的是 (填序号)。(2)B属于 (填“金属”或“非金属”)元素,B原子在化学反应中形成的离子符号为 。 (3)B、C元素形成的化合物的化学式为 。 (4)某元素X形成的化合物的化学式为Na2X,则X的原子结构示意图可能是 (填序号)。
解析:(1)质子数决定元素的种类,由微粒的结构示意图可知,核内质子数不同的有4种,所以,图中共表示了4 种元素的微粒;在D的微粒的结构示意图中,核内质子数(8)<核外电子数(10),属于阴离子;稀有气体的原子最外层有8个电子(或最外层是第一层有2个电子)时,故E属于稀有气体原子。(2)由B微粒的结构示意图可知,核内质子数为12,是镁元素,属于金属元素。由于镁原子最外层的电子数是2,在反应中易失去最外层的2个电子,形成镁离子,符号为Mg2+。(3)由于B元素是镁元素,其化合价为+2价,C元素是氯元素,原子的最外层的电子数是7,在反应中易得到1个电子,因此其化合价为-1价,所以B、C元素形成的化合物的化学式是MgCl2。(4)化合物Na2X中钠的化合价为+1价,根据化合物中各元素的化合价代数和为零可知,X的化合价为-2价,故X的最外层电子数为6,可能是图示中的A。
答案:(1)4 D O2- E(2)金属 Mg2+(3)MgCl2(4)A
7.图1是元素周期表中铟元素的相关信息,图2是铟原子的结构示意图(当电子层达到或超过四层时,倒数第二层不超过18个电子),回答下列问题:
(1)铟元素属于 (填“金属”或“非金属”)元素,其原子核外共有 个电子层。 (2)在化学反应中,铟原子容易 (填“失去”或“得到”)电子形成铟离子,铟离子的化学符号为 。 (3)画出第13号元素的原子结构示意图 ,该元素与铟元素在元素周期表中处于同一 (填“周期”或“族”)。
解析:(1)铟元素汉字名称的偏旁是“金”,可见属于金属元素;其核外有5个电子层;(2)铟原子最外层有3个电子,在化学反应中易失去最外层的3个电子而带3个单位的正电荷;(3)13号元素是铝元素,其原子结构示意图为 ,其原子最外层与铟原子最外层都是3个电子,故位于同一族。答案:(1)金属 5 (2)失去 In3+ (3) 族
归类示例一 构成物质的微粒【例1】 对于构成物质的分子、原子和离子的认识,下列说法正确的是( )A.构成分子的原子能保持该物质的化学性质B.原子得失电子变成离子后,元素的种类发生了变化C.两种原子的质量之比等于它们的相对原子质量之比D.离子之间存在着相互作用,分子之间没有相互作用解析:由分子构成的物质,保持其化学性质的最小微粒是分子,构成分子的原子不能保持该物质的化学性质,故A错误;原子得失电子变成离子后,质子数不变,故元素的种类不发生变化,故B错误;两种原子的质量之比等于它们的相对原子质量之比,故C正确;分子、原子、离子之间都存在着相互作用,故D错误。答案:C
归类示例二 粒子的基本性质【例2】 用微粒的知识解释生活中的一些现象,其中错误的是( )
解析:NaCl是由离子构成的,离子是不断运动的,所以,向汤中加入少量的NaCl整锅汤变咸,C项错误。答案:C
归类示例三 粒子结构示意图【例3】 下列粒子结构示意图中,表示阳离子的是( )
解析:当核内质子数大于核外电子数时,属于阳离子,C中核内质子数大于核外电子数,是阳离子结构示意图;A中核内质子数小于核外电子数,是阴离子结构示意图;B、D中核内质子数等于核外电子数,是原子结构示意图。答案:C
归类示例四 物质的元素组成【例4】 碳元素与氧元素的本质区别是( )A.质子数不同B.电子数不同C.中子数不同D.最外层电子数不同解析:元素是具有相同核电荷数(即质子数)的一类原子的总称,因此,同种元素的原子,质子数一定相同,不同种元素的原子,质子数一定不同。答案:A
归类示例五 元素周期表【例5】 如图是某元素的原子结构示意图和该元素在元素周期表中的单元格,下列说法不正确的是( )A.该元素属于金属元素B.该原子在化学变化中容易失去电子C.该原子的大小主要决定于核外电子的运动空间D.该原子的质量由构成其原子的质子和电子决定
解析:原子的质量主要集中在原子核上,原子核是由质子和中子构成的,因此原子的质量由构成其原子的质子和中子决定,故D错误。答案:D
归类示例六 化学符号表示的意义【例6】 对于下列几种化学符号,有关说法正确的是( )①H ②Fe2+ ③Cu ④P2O5 ⑤Fe3+ ⑥NaClA.能表示一个分子的是①④⑥B.表示物质组成的化学式是③④⑥C.②⑤的质子数相同,化学性质也相同D.④中的数字“5”表示五氧化二磷中有5个氧原子解析:①H可表示1个氢原子或氢元素;④P2O5可表示1个五氧化二磷分子;⑥NaCl是由离子构成的,故A错误;②Fe2+、⑤Fe3+分别表示亚铁离子、铁离子,它们的质子数相同,但它们的最外层电子数不同,化学性质不同,故C错误;④P2O5中的“5”表示1个五氧化二磷分子中含有5个氧原子,故D错误。答案:B
初中化学中考复习 中考化学总复习优化设计第一板块基础知识过关第七单元燃料及其利用课件: 这是一份初中化学中考复习 中考化学总复习优化设计第一板块基础知识过关第七单元燃料及其利用课件,共36页。PPT课件主要包含了考点梳理,自主测试,4能源的分类,归类示例一,归类示例二,归类示例三,归类示例四等内容,欢迎下载使用。
初中化学中考复习 中考化学总复习优化设计第一板块基础知识过关第一单元走进化学世界课件: 这是一份初中化学中考复习 中考化学总复习优化设计第一板块基础知识过关第一单元走进化学世界课件,共51页。PPT课件主要包含了考点梳理,自主测试,物质的变化,2给液体加热,归类示例一,归类示例二,归类示例三,归类示例四,归类示例五,归类示例六等内容,欢迎下载使用。
初中化学中考复习 中考化学总复习优化设计第一板块基础知识过关第五单元化学方程式课件: 这是一份初中化学中考复习 中考化学总复习优化设计第一板块基础知识过关第五单元化学方程式课件,共36页。PPT课件主要包含了考点梳理,自主测试,书写步骤,归类示例一,归类示例二,归类示例三,归类示例四等内容,欢迎下载使用。












