

- 课时作业 17 铁及其化合物之间的转化关系 试卷 1 次下载
- 课时作业 18 硫及其氧化物 试卷 1 次下载
- 课时作业 19 硫酸、酸雨及其防治 试卷 1 次下载
- 课时作业 20 氮气与氮的氧化物 试卷 1 次下载
- 课时作业 21 氨与铵盐 试卷 2 次下载
高中鲁科版 (2019)第3章 物质的性质与转化微项目 论证重污染天气“汽车限行”的合理性——探讨社会性科学议题课后练习题
展开课时作业23 论证重污染天气“汽车限行”的合理性
[学业达标]
1.世界大学生夏季运动会是规模仅次于夏季奥运会的世界级综合性运动会。2021年第31届世界大学生运动会将在成都举办。“绿色”是成都的城市发展理念,也是这次运动会的组织理念。下面有关说法不正确的是( )
A.成都市目前推广使用的清洁燃料压缩天然气(CNG)和液化石油气(LPG)的主要成分均是烃类
B.兴建运动会场馆所用到的金属材料中可能含有非金属元素
C.“绿色化学”的核心是应用化学原理对环境污染进行治理
D.新能源汽车的使用有助于减少氮氧化物的排放
2.当前,汽车尾气已成为许多城市空气的主要污染源。研究表明,含TiO2的混凝土或沥青可以部分消除汽车尾气中的氮氧化物,其原理如下:
下列关于该“消除”过程的叙述不正确的是( )
A.部分光能转变为化学能
B.消除总变化为NOx+O2+H2O―→HNO3
C.消除反应能全天候发生
D.使用纳米TiO2的消除效率更高
3.SO2废气的回收利用方案如图所示。下列说法错误的是( )
A.废气与氨水混合一定发生反应2NH3·H2O+SO2===2NH+SO+H2O
B.Y中含有NH4HSO3
C.气体a既有氧化性又有还原性
D.(NH4)2S2O8是一种纯净物
4.三效催化剂是最为常见的汽车尾气催化剂,在催化剂表面物质转化的关系如图所示,下列说法正确的是( )
A.在转化过程中,氮元素均被还原
B.依据图示判断催化剂不参与储存和还原过程
C.还原过程中生成0.1 mol N2,转移电子数为0.5NA
D.三效催化剂能有效实现CO、NOx及CxHy的净化
5.汽车排放的尾气中含有NO2,NO2是城市大气污染的主要污染物之一。在日光照射下,NO2发生一系列光化学烟雾的循环反应,从而不断产生O3,加重空气污染。反应过程为①2NO2―→2NO+2O,②2NO+O2―→2NO2,③O+O2―→O3。下列对该反应过程及生成物叙述正确的是( )
A.NO2只起催化剂作用
B.NO起催化剂作用
C.NO2只起氧化剂作用
D.O3与O2为同素异形体
6.下列现象的产生,与氮循环无关的是( )
A.光化学烟雾 B.白色污染
C.水体富营养化 D.酸雨
7.如图表示汽车尾气净化器处理汽车尾气的过程。有关叙述不正确的是( )
A.CO氧化为CO2所需氧来源于NOx
B.汽车安装这种净化器后,能避免铅污染
C.Pt-Rh催化剂化学反应前后质量不变
D.使用该净化器能减少酸雨的发生
8.汽车彻底改变了我们的生活,成为我们不可或缺的交通工具之一。汽车尾气系统中的催化转化器,可有效降低尾气中的CO、NO和NO2等向大气的排放,在催化转化器的前半部发生的反应为2CO(g)+2NO(g)⇌2CO2(g)+N2(g)。下列关于反应2CO(g)+2NO(g)⇌2CO2(g)+N2(g)的说法正确的是( )
A.CO是氧化剂 B.CO发生氧化反应
C.NO被氧化 D.NO是还原剂
9.随着我国汽车年销量的大幅增加,给空气造成了很大的污染。汽车尾气装置里,气体在催化剂表面吸附与解吸作用的过程如图所示,下列说法正确的是 ( )
A.反应中NO为氧化剂,N2为氧化产物
B.汽车尾气的主要污染成分包括CO、NO和N2
C.反应中CO为氧化剂,CO2为氧化产物
D.催化转化总反应的化学方程式为2NO+O2+4CO4CO2+N2
[等级突破]
10.汽车尾气主要含有CO2、CO、SO2、NOx等,汽车尾气逐渐成为城市空气污染的主要来源之一。
(1)汽车尾气中的CO来自 ,NO来自 。
(2)汽车尾气对环境和人体的危害主要有 。
A.光化学烟雾:NOx在紫外线照射下与碳氢化合物发生反应形成的有毒烟雾
B.酸雨:NOx排入大气中后,与水反应生成HNO3和HNO2,随雨雪降到地面
C.破坏臭氧层:NO2可使平流层中的臭氧减少,导致地面紫外线辐射量增加
D.NO与血红蛋白结合使人中毒
(3)汽车尾气中的CO、NOx在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出NO被CO还原的化学方程式: 。
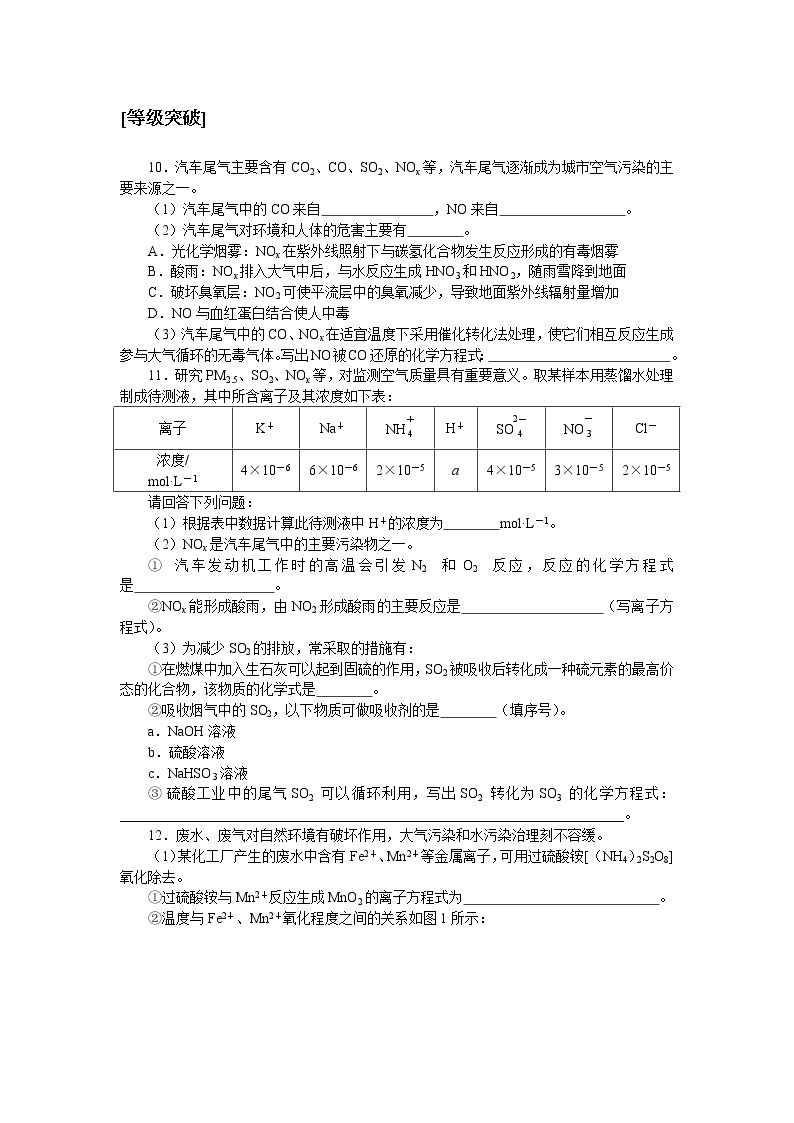
11.研究PM2.5、SO2、NOx等,对监测空气质量具有重要意义。取某样本用蒸馏水处理制成待测液,其中所含离子及其浓度如下表:
离子 | K+ | Na+ | NH | H+ | SO | NO | Cl- |
浓度/ mol·L-1 | 4×10-6 | 6×10-6 | 2×10-5 | a | 4×10-5 | 3×10-5 | 2×10-5 |
请回答下列问题:
(1)根据表中数据计算此待测液中H+的浓度为 mol·L-1。
(2)NOx是汽车尾气中的主要污染物之一。
①汽车发动机工作时的高温会引发N2和O2反应,反应的化学方程式是 。
②NOx能形成酸雨,由NO2形成酸雨的主要反应是 (写离子方程式)。
(3)为减少SO2的排放,常采取的措施有:
①在燃煤中加入生石灰可以起到固硫的作用,SO2被吸收后转化成一种硫元素的最高价态的化合物,该物质的化学式是 。
②吸收烟气中的SO2,以下物质可做吸收剂的是 (填序号)。
a.NaOH溶液
b.硫酸溶液
c.NaHSO3溶液
③硫酸工业中的尾气SO2可以循环利用,写出SO2转化为SO3的化学方程式:________________________________________________________________________。
12.废水、废气对自然环境有破坏作用,大气污染和水污染治理刻不容缓。
(1)某化工厂产生的废水中含有Fe2+、Mn2+等金属离子,可用过硫酸铵[(NH4)2S2O8]氧化除去。
①过硫酸铵与Mn2+反应生成MnO2的离子方程式为 。
②温度与Fe2+、Mn2+氧化程度之间的关系如图1所示:
图1
实验过程中应将温度控制在 。Fe2+被氧化后形成胶体絮状粒子,常加入活性炭处理,加入活性炭的目的为 。
③H2O2也有较强的氧化性,在实际生产中不用H2O2氧化Mn2+的原因是________________________________________________________________________
________________________________________________________________________。
(2)工业上废气中的SO2可用Na2CO3溶液吸收,反应过程中溶液组成的变化如图2所示。
图2
①吸收初期(图中A点以前)反应的化学方程式为 。
②C点高于B点的原因是 。
课时作业23 论证重污染天
气“汽车限行”的合理性
1.解析:压缩天然气(CNG)的主要成分是甲烷,液化石油气(LPG)的成分是丙烷、丁烷等,所以这两类燃料的主要成分都是烃类,故A正确;合金可能含有非金属元素,故B正确;“绿色化学”的核心是从源头上控制污染,而不是治理污染,故C错误;新能源汽车的使用可减少化石燃料的使用,可减少常规汽车的使用,能减少氮氧化物的排放,故D正确。
答案:C
2.解析:在TiO2的催化作用下紫外线提供能量,部分光能转变为化学能,故A项正确;题中示意图表明,在TiO2的催化作用下紫外线提供能量,发生反应:NOx+O2+H2O―→HNO3,故B项正确;没有紫外线时上述反应不能发生,故C项错误;纳米与紫外线接触面积更大,将产生更多的光生电子和光生空穴,从而消除更多的NOx,故D项正确。
答案:C
3.解析:废气用氨水吸收一定发生反应2NH3·H2O+SO2===2NH+SO+H2O,所以A项正确;(NH4)2SO3与过量H2SO4反应生成(NH4)2SO4、SO2和H2O,Y为(NH4)2SO4和过量的H2SO4,不含NH4HSO3,所以B项错误;气体a为SO2,SO2中S元素的化合价为+4价,既有氧化性又有还原性,所以C项正确;(NH4)2S2O8是一种化合物,属于纯净物,D项正确。
答案:B
4.解析:在储存过程中,N元素被氧化生成硝酸钡,所以A项错误;BaO做催化剂,参与反应过程,所以B项错误;由硝酸钡生成氮气,N由+5价变为0价,因此生成0.1 mol N2转移1 mol电子,所以C项错误;由图示可知,三效催化剂能有效实现CO、NOx和CxHy三种成分的净化,所以D项正确。
答案:D
5.解析:反应过程①+②得O2―→2O,③O+O2―→O3,NO2起催化剂作用,反应过程中NO2还做氧化剂,A、B、C项错误;O3与O2属于同素异形体,D项正确。
答案:D
6.解析:光化学污染是氮的氧化物和有机烃类在光作用下的一系列复杂变化,与氮循环有关;白色污染是指难降解的塑料垃圾(多指塑料袋)对环境的污染;水体富营养化是指水中的氮、磷等元素浓度过大造成的水污染,会导致藻类疯长,从而引起水中缺氧,导致水生生物大量死亡,与氮循环有关;酸雨是二氧化硫和氮氧化物与雨水作用的结果,与氮循环有关。
答案:B
7.解析:由题目的信息可知,CO氧化为CO2所需的氧来源于氮的氧化物,A项正确;汽车安装这种净化器后,能避免一氧化碳、氮的氧化物造成的空气污染,但不能避免铅污染,B项错误;PtRh催化剂在化学反应前后质量和化学性质都不变,C项正确;氮的氧化物也会造成酸雨,因此使用该净化器能减少酸雨的发生,D项正确。
答案:B
8.解析:反应2CO(g)+2NO(g)⇌2CO2(g)+N2(g)中,C元素的化合价升高,被氧化,则CO为还原剂,发生氧化反应;N元素的化合价降低,被还原,则NO是氧化剂,故B正确。
答案:B
9.解析:根据题图可知,总反应中氮元素化合价降低,一氧化氮为氧化剂,氮气是还原产物,故A错误;氮气不是污染成分,故B错误;反应中碳元素化合价升高,一氧化碳为还原剂,故C错误;根据题图可知发生的反应为2NO+O2===2NO2、2NO2+4CO4CO2+N2,由两式可得总反应为2NO+O2+4CO4CO2+N2,故D正确。
答案:D
10.解析:(1)一氧化碳是由汽油不完全燃烧产生的;N2与O2在汽车汽缸内的高温环境下反应可生成NO。(2) NOx在紫外线照射下与碳氢化合物发生反应形成的有毒烟雾,称为光化学烟雾,故A正确;NOx能形成硝酸型酸雨,故B正确;NO2能破坏臭氧层,故C正确;NO易与血红蛋白结合使人中毒,故D正确。(3)汽车尾气中的CO、NOx在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体,NO被CO还原的化学方程式为2CO+2NON2+2CO2。
答案:(1)汽油的不完全燃烧 N2与O2在汽车汽缸内的高温环境下的反应 (2)ABCD (3) 2CO+2NON2+2CO2
11.解析:(1)根据溶液呈电中性可得c(K+)+c(Na+)+c(NH)+c(H+)=2c(SO)+c(NO)+c(Cl-),所以c(H+)=1×10-4 mol·L-1。(2)①汽车发动机工作时的高温会引发N2和O2反应,反应的化学方程式是N2+O22NO。②NOx能形成酸雨,NO2形成酸雨的离子方程式为3NO2+H2O===2H++2NO+NO。(3)①在燃煤中加入生石灰,氧化钙和二氧化硫反应生成亚硫酸钙,亚硫酸钙被氧气氧化为硫酸钙,故硫元素最高价态的化合物为CaSO4。②氢氧化钠溶液可以吸收二氧化硫,生成亚硫酸氢钠或亚硫酸钠,故a正确;硫酸不能吸收二氧化硫,故b错误;NaHSO3溶液不能吸收二氧化硫,故c错误。③硫酸工业中的尾气SO2可以循环利用,SO2转化为SO3的化学方程式为2SO2+O22SO3。
答案:(1)1×10-4 (2)①N2+O22NO ②3NO2+H2O===2H++2NO+NO (3)①CaSO4 ②a ③2SO2+O22SO3
12.解析:(1)①过硫酸铵与Mn2+反应生成MnO2,反应的离子方程式为S2O+2H2O+Mn2+===4H++2SO+MnO2↓;②根据图1可知:80℃时Fe2+、Mn2+氧化程度接近1.0,故实验过程中可将温度控制在80℃;Fe2+被氧化后形成胶体絮状粒子,常加入活性炭处理,加入活性炭的目的为吸附胶体粒子形成沉淀;③H2O2也有较强的氧化性,在实际生产中不用H2O2氧化Mn2+的原因是锰的化合物可催化H2O2分解,使消耗的H2O2增多。(2)①由图2可知吸收初期(图中A点以前)NaHCO3和Na2SO3的量明显增加,则发生反应的化学方程式为2Na2CO3+SO2+H2O===2NaHCO3+Na2SO3;②根据钠原子守恒,可知NaHSO3的物质的量是Na2CO3的2倍,所以NaHSO3的百分浓度比Na2CO3的大。
答案:(1)①S2O+2H2O+Mn2+===4H++2SO+MnO2↓
②80℃(80℃~90℃区间均可) 吸附胶体粒子形成沉淀 ③锰的化合物可催化H2O2分解,使消耗的H2O2增多 (2)①2Na2CO3+SO2+H2O===2NaHCO3+Na2SO3 ②NaHSO3的物质的量是Na2CO3的2倍
高中化学鲁科版 (2019)必修 第一册第3章 物质的性质与转化微项目 论证重污染天气“汽车限行”的合理性——探讨社会性科学议题一课一练: 这是一份高中化学鲁科版 (2019)必修 第一册第3章 物质的性质与转化微项目 论证重污染天气“汽车限行”的合理性——探讨社会性科学议题一课一练,共5页。
高中化学课时作业23防治二氧化硫对环境的污染含解析苏教版必修1: 这是一份高中化学课时作业23防治二氧化硫对环境的污染含解析苏教版必修1,共6页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
高中化学鲁科版 (2019)必修 第一册微项目 论证重污染天气“汽车限行”的合理性——探讨社会性科学议题课时练习: 这是一份高中化学鲁科版 (2019)必修 第一册微项目 论证重污染天气“汽车限行”的合理性——探讨社会性科学议题课时练习,共6页。试卷主要包含了研究PM2等内容,欢迎下载使用。













