


2023届高三化学高考备考一轮复习化学工艺流程综合(Ⅱ卷)考题预测课件
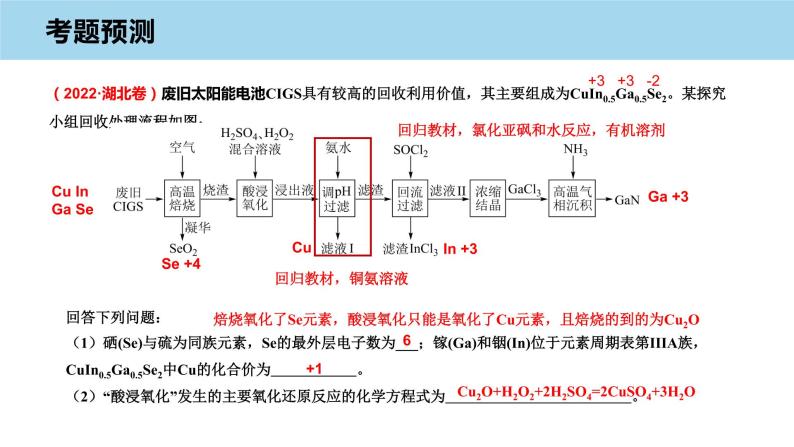
展开(2022·湖北卷)废旧太阳能电池CIGS具有较高的回收利用价值,其主要组成为。某探究小组回收处理流程如图:
回答下列问题:(1)硒(Se)与硫为同族元素,Se的最外层电子数为___;镓(Ga)和铟(In)位于元素周期表第IIIA族,中Cu的化合价为 。(2)“酸浸氧化”发生的主要氧化还原反应的化学方程式为 。
Cu In Ga Se
+3 +3 -2
焙烧氧化了Se元素,酸浸氧化只能是氧化了Cu元素,且焙烧的到的为Cu2O
Cu2O+H2O2+2H2SO4=2CuSO4+3H2O
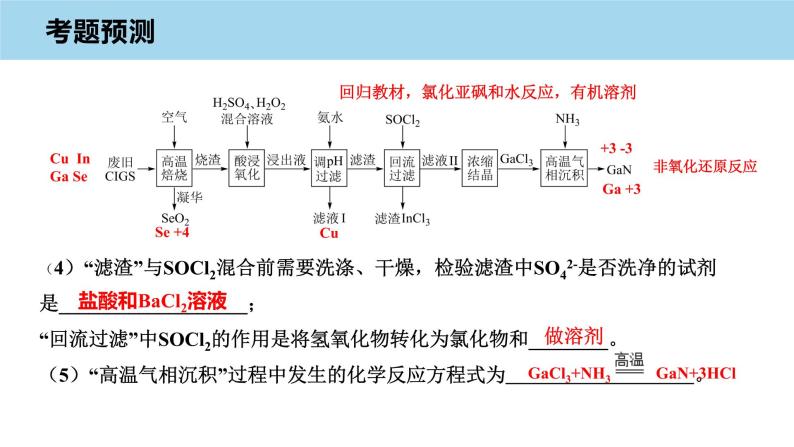
回归教材,氯化亚砜和水反应,有机溶剂
(4)“滤渣”与SOCl2混合前需要洗涤、干燥,检验滤渣中SO42-是否洗净的试剂是___________________;“回流过滤”中SOCl2的作用是将氢氧化物转化为氯化物和________。(5)“高温气相沉积”过程中发生的化学反应方程式为 。
Cu In Ga Se
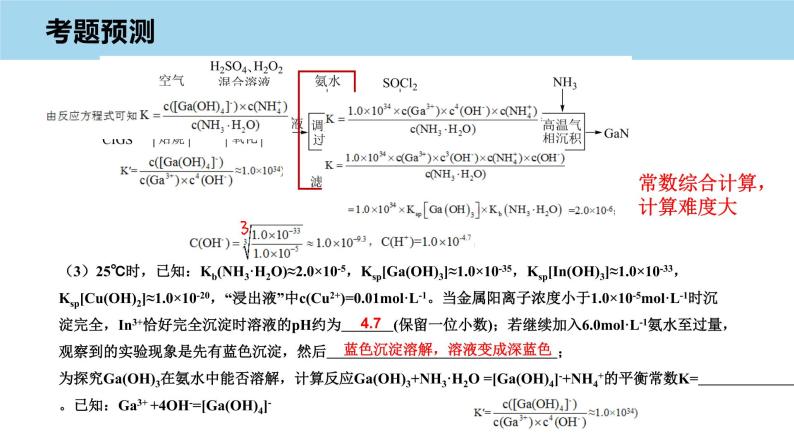
(3)25℃时,已知:Kb(NH3·H2O)≈2.0×10-5,Ksp[Ga(OH)3]≈1.0×10-35,Ksp[In(OH)3]≈1.0×10-33,Ksp[Cu(OH)2]≈1.0×10-20,“浸出液”中c(Cu2+)=0.01ml·L-1。当金属阳离子浓度小于1.0×10-5ml·L-1时沉淀完全,In3+恰好完全沉淀时溶液的pH约为 (保留一位小数);若继续加入6.0ml·L-1氨水至过量,观察到的实验现象是先有蓝色沉淀,然后 ;为探究Ga(OH)3在氨水中能否溶解,计算反应Ga(OH)3+NH3·H2O =[Ga(OH)4]-+NH4+的平衡常数K= 。已知:Ga3+ +4OH-=[Ga(OH)4]-
蓝色沉淀溶解,溶液变成深蓝色
常数综合计算,计算难度大
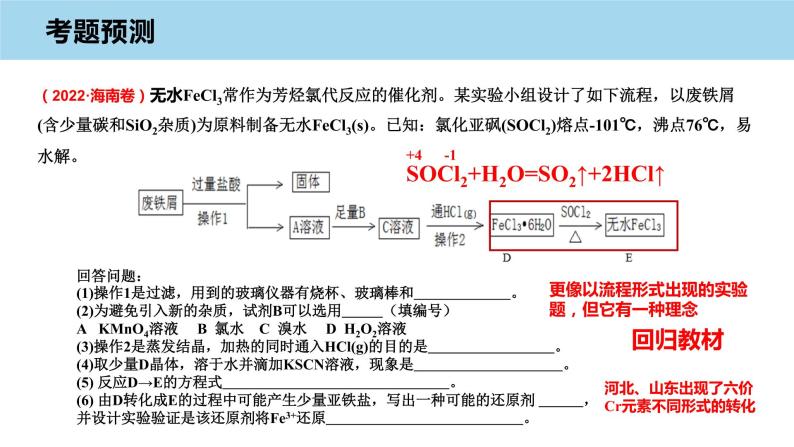
(2022·海南卷)无水FeCl3常作为芳烃氯代反应的催化剂。某实验小组设计了如下流程,以废铁屑(含少量碳和SiO2杂质)为原料制备无水FeCl3(s)。已知:氯化亚砜(SOCl2)熔点-101℃,沸点76℃,易水解。
回答问题:(1)操作1是过滤,用到的玻璃仪器有烧杯、玻璃棒和 。(2)为避免引入新的杂质,试剂B可以选用 (填编号)A KMnO4溶液 B 氯水 C 溴水 D H2O2溶液(3)操作2是蒸发结晶,加热的同时通入HCl(g)的目的是 。(4)取少量D晶体,溶于水并滴加KSCN溶液,现象是 。(5) 反应D→E的方程式 。(6) 由D转化成E的过程中可能产生少量亚铁盐,写出一种可能的还原剂 ,并设计实验验证是该还原剂将Fe3+还原 。
更像以流程形式出现的实验题,但它有一种理念
SOCl2+H2O=SO2↑+2HCl↑
河北、山东出现了六价Cr元素不同形式的转化
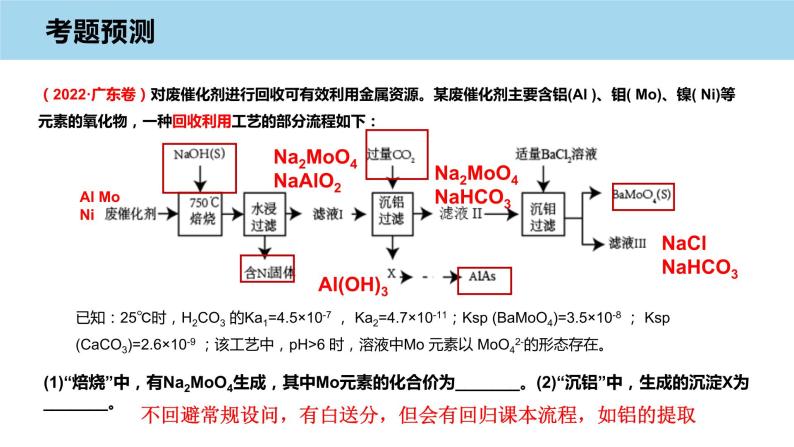
(2022·广东卷)对废催化剂进行回收可有效利用金属资源。某废催化剂主要含铝(Al )、钼( M)、镍( Ni)等元素的氧化物,一种回收利用工艺的部分流程如下:
已知:25℃时,H2CO3 的Ka1=4.5×10-7 , Ka2=4.7×10-11;Ksp (BaMO4)=3.5×10-8 ; Ksp (CaCO3)=2.6×10-9 ;该工艺中,pH>6 时,溶液中M 元素以 MO42-的形态存在。
(1)“焙烧”中,有Na2MO4生成,其中M元素的化合价为_______。(2)“沉铝”中,生成的沉淀X为_______。
不回避常规设问,有白送分,但会有回归课本流程,如铝的提取
Na2MO4NaHCO3
Na2MO4NaAlO2
(4)①滤液Ⅲ中,主要存在的钠盐有NaCl和Y,Y为_______。②往滤液Ⅲ中添加适量NaCl固体后,通入足量_______(填化学式)气体,再通入足量CO2 ,可析出Y 。(5)高纯AlAs (砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致密保护膜为一种氧化物,可阻止H2O2刻蚀液与下层GaAs (砷化镓)反应。该氧化膜是 。
回归课本流程,侯氏制碱法和致密氧化膜
题在课外 理在书中
(3)“沉钼”中, 为7.0。①生成 BaMO4的离子方程式为 。②若条件控制不当,BaCO3 也会沉淀。为避免 BaMO4中混入BaCO3 沉淀,溶液中c(HCO3-):c(MO42-) =_______(列出算式)时,应停止加入BaCl2溶液。
c(CO32-):c(MO42-) = Ksp之比 ,再根据Ka2找出c(CO32-):c(HCO3-)关系代入整理即可
通过横比22年高考题,我们不难发现,工艺流程题的呈现方式比较稳定,设问也不回避常见考点,常考常新,陌生元素如 M、Ce等元素的出现让我们防不胜防,同时计算难度加大(不是直来直去的那种),20、21江苏题连续两年出现补充流程,但有些设问又落实到课本的工艺流程,如湖北题、福建题都有此特点,还有陌生方程式的书写也复杂了不少,如河北卷、湖南卷等。在此我不再一一列举,在配套的练习中这些都有所涉及。
我们如何应对呢?我们不可能将所有陌生元素的知识全部补充到位,也没必要都去记住,我们看高考出题人的指导思想:
高考就是考察学生的知识迁移运用能力,即应该具备在认知模型的框架下学习的一种思维方式,在高中知识的支撑下去解题。
认知模型的建立就是我们积累、储备化工知识,熟悉教材中的工艺涉及的操作方法和思路,越简单的问题越要明确原理,夯实基础,记忆答题术语,规范作答,只有这样才能形成一定的解题方法,才能灵活运用。
教材常见化学工艺海水提溴、海水提镁、海水提碘 氯碱工业------侯氏制碱法工业制硅并提纯 工业制玻璃电镀、金属冶炼 硫酸工业、硝酸工业
重要考点——铵盐的作用
(2022·山东卷)以菱镁矿(主要成分为MgCO3,含少量SiO2,Fe2O3和A12O3)为原料制备高纯镁砂的工艺流程如下:已知浸出时产生的废渣中有SiO2,Fe(OH)3和Al(OH)3。下列说法错误的是
浸出镁的反应为 MgO+2NH4Cl=MgCl2+2NH3↑+H2O
重要考点——铵盐的作用及陌生方程式书写
SiO2 Fe(OH)3 Al(OH)3
(2022·全国乙卷)磁选后的炼铁高钛炉渣,主要成分有有 SiO2、TiO2、Al2O3、MgO、CaO以及少量的Fe2O3 。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
(1)“焙烧”中, SiO2、TiO2 几乎不发生反应, Al2O3、MgO、CaO、Fe2O3 转化为相应的硫酸盐,写出 Al2O3转化为(NH4)Al(SO4)2 的化学方程式_______。
Al2O3+ (NH4) 2SO4 = (NH4)Al(SO4)2
NH4+=NH3+H+
(2022·河北模拟)合理利用工厂烟灰,变废为宝,对保护环境具有重要意义。以某钢铁厂烟灰(主要成分为ZnO,并含少量的CuO、MnO2、Fe2O3等)为原料制备氧化锌的工艺流程如下:
(1)“浸取”工序中加入过量氨水的目的:①使ZnO、CuO溶解,转化为[Zn(NH3)4]2+和[Cu(NH3)4]2+配离子;
ZnO+2NH3·H2O+2NH4+ =[Zn(NH3)4]2++3H2O
MnO2 Fe2O3
Zn+[Cu(NH3)4]2+=Cu+[Zn(NH3)4]2+
(2021·江苏卷)实验室以工业废渣(主要含CaSO4·2H2O,还含少量SiO2、Al2O3、Fe2O3)为原料制取轻质CaCO3和(NH4)2SO4晶体,其实验流程如下:
(2)将氨水和NH4HCO3溶液混合,可制得(NH4)2CO3溶液,其离子方程式为 ;浸取废渣时,向(NH4)2CO3溶液中加入适量浓氨水的目的是 。
CO32-+NH4++H2O = HCO3-+NH3·H2O, 加入适量浓氨水,水解平衡逆向移动,溶液中CO32-的浓度增大,反应CaSO4(s)+CO32-(aq)= CaCO3(s)+SO42-(aq)正向移动,促进CaSO4的转化。
(2020·新课标Ⅰ)钒具有广泛用途。黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、镁的铝硅酸盐,以及SiO2、Fe3O4。采用以下工艺流程可由黏土钒矿制备NH4VO3。
高考题中出现的使金属离子形成沉淀的方式有多种,根据需要利用Ksp的数据我们可以进行判断,有一类金属碳酸盐沉淀的生成常使用NH4HCO3作为沉淀剂,有时还加入氨水。为什么不使用NaHCO3或Na2CO3来提供CO32-呢?
2019江苏(4)沉铁:将提纯后的FeSO4溶液与氨水-NH4HCO3混合溶液反应,生成FeCO3沉淀。①生成FeCO3沉淀的离子方程式为 。
Fe2++HCO3-=FeCO3 ↓ + H+
②设计以FeSO4溶液、氨水- NH4HCO3混合溶液为原料,制备FeCO3的实验方案:___________。【FeCO3沉淀需“洗涤完全”,Fe(OH)2开始沉淀的pH=6.5】。
Fe2++HCO3-+NH3=FeCO3 ↓ + NH4+
Fe2++2HCO3-=FeCO3 ↓ + H2O + CO2 ↑
NH4HCO3+NH3 =(NH4)2CO32(NH4)2CO3 +H2O+2MgSO4=2(NH4)2SO4+CO2+Mg(OH)2 · MgCO3
特点:和NaHCO3比较溶解度大,溶液接近中性,廉价,受热易分解在溶液中不残留,过量不易引起杂质Na2CO3与弱碱阳离子易互促水解,产生氢氧化物
2024届高三化学高考备考一轮复习工艺流程专题课件: 这是一份2024届高三化学高考备考一轮复习工艺流程专题课件,共3页。PPT课件主要包含了思维模型和方法模型,真题演练,产品分离提纯,蒸发浓缩趁热过滤,条件控制,温度控制,高考真题·导向等内容,欢迎下载使用。
2024届高三化学一轮复习 2023年高考试题分析与备考策略——化学工艺流程模块课件: 这是一份2024届高三化学一轮复习 2023年高考试题分析与备考策略——化学工艺流程模块课件,共3页。PPT课件主要包含了命题内容,命题角度,考什么,真题示例,试题结构,结构模型,思维模型,三条思维主线,思维建模,工业流程等内容,欢迎下载使用。
2023届高三化学高考备考一轮复习有机化学基础(Ⅱ卷)考题预测课件: 这是一份2023届高三化学高考备考一轮复习有机化学基础(Ⅱ卷)考题预测课件,共45页。PPT课件主要包含了命题方向,回眸高考,模型建构,考题预测,教学策略,官能团名称,西城区一模,考点1,考点7,考点6等内容,欢迎下载使用。












