2022中考化学实验探究题:物质成分探究(易错型)(无答案)
展开(考频:★★★★★)
1. 松花蛋,又称皮蛋.其中一种加工工艺的主要原料配方为:鸭蛋,水,生石灰,纯碱,食盐.加工时,将纯碱、食盐加入容器中,加沸水溶解,再慢慢加入生石灰充分反应,冷却后得到料液,再加入鸭蛋浸渍. 请回答下列问题:
(1) 鸭蛋中富含的营养素有水和________.
(2) 生石灰加入沸水中,水能持续保持沸腾,其原因是_______.
(3) 静置后,取少量的上层料液,稀释后滴加无色酚酞试液,料液应变 为________色
(4) 同学们对上层料液的成分产生了兴趣,请你一起参加他们的探究活动.
【提出问题】
料液中含有哪些溶质?
【交流讨论】
①一定含有________
②可能还含有其它溶质
甲同学推断只有Ca(OH)2
乙同学推断只有Na2CO3
丙同学推断有Ca(OH)2、Na2CO3
通过进一步讨论,大家一致认为丙同学的推断是错误的,理由________(用化学方程式表示).
(5) 【实验探究】
我打算取上层清液滴加硫酸铜溶液,产生蓝色沉淀,证明甲同学的结论正确,但桐桐否定了我的做法,她的原因是________,为验证甲的推断是正确的,她又做了如下探究实验.
(6) 【探究结论】
甲同学的推断是正确的.
【知识应用】
皮蛋中因为剩余一些碱性物质而有涩味,所以食用时加入一些食醋除去这些涩味,原因为________.
【反思拓展】
剩余液体不能直接排放到下水道,否则会污染水源.
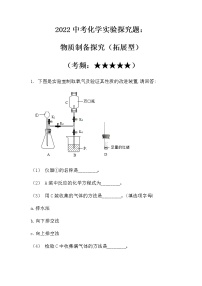
2. Ca(OH)2变质得到Ca(OH)2和CaCO3的混合物。李琳同学设计了如下图的实验装置来测定CaCO3的含量,她用气密性良好的装置装上药品并通一会儿氮气后关闭止水夹,再打开分液漏斗活塞。提示:碱石灰(可以吸收CO2和H2O)浓硫酸均足量,稀盐酸不考虑其挥发性。
(1) 通入N2的原因之一是N2的化学性质________(填活泼或者不活泼)。
(2) 甲装置中发生中和反应的化学方程式为________。
(3) 浓硫酸的作用是________。
(4) 测定CaCO3的含量需要测定两个物理量,其中一个物理量为样品的质量。
①另一个物理量为________(填序号)。
A 滴下的稀盐酸质量
B 反应前后乙装置增加的质量
C 反应前后丙装置增加的质量
D 反应前后丁装置增加的质量
②若去掉丁装置,测得CaCO3含量________(填“偏高”、“偏低”或“不变")。
③甲装置中反应结束后打开止水夹再通入一会儿N2的目的是________。
3. 某校化学兴趣小组同学向盛有一定量生石灰的烧杯中加入碳酸钠溶液,充分反应后冷却至室温;过滤、洗涤、干燥得到固体A和溶液B并对固体A和溶液B的成分展开了探究。
(1) 上述实验中发生的化学反应有:
①CaO+H2O=Ca(OH)2;
②________(写化学方程式)。
(2) 探究活动Ⅰ:固体A的成分是什么?
【猜想假设】
小雨猜想是CaCO3 ,
小亮猜想是CaCO3和Ca(OH)2。
小亮猜想含有Ca(OH)2的理由是 ________。
(3) 【实验验证】
1.小雨取少量固体A于试管中,加入足量的稀盐酸,有气泡产生,证明自己的猜想正确。
2.小亮取少量固体A于试管中,加入足量水振荡,静置,向上层清液中滴加无色酚酞溶液,观察到________,证明自己的猜想正确。
【反思评价】
同学们经过讨论后认为小雨的实验不足以确定固体A的成分,理由是________。结合两位同学的实验,证明了小亮的猜想是正确的,由此确定了固体A的成分。
(4) 探究活动Ⅱ:溶液B中溶质的成分是什么?
【猜想假设】
猜想一:NaOH;
猜想二:NaOH、Na2CO3;
猜想三:________ 。
【讨论交流】
结合对固体A成分的探究,同学们认为猜想三是正确的,理由是________ 。
【实验验证】
取少量溶液B于试管中,滴加________溶液,产生白色沉淀,证明猜想三正确。
4. 化学兴趣小组的同学进行了以下实验:向烧杯中加入变质的氢氧化钙固体和一定量的稀盐酸,一段时间后固体全部溶解。他们对所得溶液中的溶质成分进行了探究。
(1) Ⅰ.探究烧杯内溶液中溶质的成分。
【提出问题】
该烧杯内溶液中的溶质是什么?
【猜想】
猜想一:________;
猜想二:CaCl2和HCl;
猜想三: CaCl2、Ca(OH)2;
猜想四: CaCl2、Ca(OH)2和HCl;
根据所学知识判断,________一定不成立。
(2) 【查阅资料】
氯化钙溶液呈中性,碳酸钠溶液呈碱性。
【进行实验】
实验步骤:取少量烧杯内溶液加入试管中,滴入几滴酚酞溶液,振荡。
实验现象1:________。
结论:猜想三不成立。
实验步骤:取少量烧杯内溶液加入另一支试管中,逐滴加入碳酸钠溶液至过量。
实验现象2:________。
结论:猜想一不成立,猜想二成立。
(3) 【反思与拓展】
酸性较强的液体直接进入下水道,会污染环境。要处理上述烧杯内的溶液,使其溶质只含有CaCl2 , 应向烧杯中加入过量的( )。
A . CaO
B . CaCO3
C . Ca(OH)2
(4) 氢氧化钠在空气中变质的化学方程式________。
(5) Ⅱ.取50g含CaCl2和HCl的混合溶液,向其中逐滴滴入溶质质量分数为5.3%的碳酸钠溶液,同时充分搅拌。测得生成的气体和沉淀的质量与加入的碳酸钠溶液的质量关系如下图所示。
①由图可知,当碳酸钠溶液质量加到________ g时,溶液中盐酸恰好反应完。
②原烧杯溶液中氯化钙的质量分数________。(请写出计算过程)
5. 在一次用餐中,某同学对燃料“固体酒精”产生了好奇,于是对其成分进行了探究.
[查阅资料]
①固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成的;
②氯化钙和氯化钡溶液均呈中性.
③Na2CO3溶液呈碱性
[提出问题]
固体氢氧化钠是否变质?
(1) 【猜想假设】
猜想①:固体氢氧化钠没有变质.
猜想②:固体氢氧化钠全部变质为Na2CO3 .
猜想③:________.
(2) 【设计方案】
取少量固体酒精于烧杯中,加入足量的水充分溶解后静置,发现烧杯底部有白色沉淀,写出产生沉淀的化学方程式________.
(3) 为进一步确定氢氧化钠变质的程度,他取烧杯中上层清液加入足量的氯化钡溶液,充分反应后滴加酚酞溶液,酚酞溶液变红.
【实验结论】
固体酒精中氢氧化钠部分变质.
【反思与交流】
实验中加入足量氯化钡溶液的目的是________.
(4) 【拓展延伸】
同学们设计了下列两套装置进行实验: 用胶头滴管吸取某种液体,锥形瓶中充入一种气体或放入一种固体物质,挤压胶头滴管.一段时间后,两装置中气球明显胀大.
①甲装置中可能发生反应的方程式是________.
②若乙装置中胶头滴管吸取的是稀盐酸,则锥形瓶中放入的固体可能是________.
③要除去部分变质的氢氧化钠溶液中的杂质,可选择的________(填序号)
A.Ba(OH)2
B.CaCl2
C.H2SO4 .
6. 随着对新型冠状病毒的认识越来越深入,人们发现戴口罩、勤洗手,给自己居住和生活的环境消毒,都是预防新型冠状病毒的有效办法。其中“84”消毒液能用于日常生活的消毒灭菌。某化学兴趣小组对一瓶敞口放置的“84”消毒液成分进行探究。
【提出问题】
该敞口久置的“84”消毒液中溶质有哪些?
【查阅资料】
⑴“84”消毒液主要成分是次氯酸钠(NaClO)和氯化钠;NaClO为有效成分,有腐蚀性并易与空气中的CO2反应(2NaClO+CO2+H2O=2HClO+Na2CO3)。
⑵NaClO溶液、HClO都具有漂白、杀菌、消毒功效。
⑶HClO不稳定受热或光照条件下会发生分解。
(1) 【提出猜想】
Ⅰ.“84”消毒液没有变质
Ⅱ. ________
Ⅲ.“84”消毒液完全变质。
(2) 【实验探究】
为了验证猜想,设计如下方案
【得出结论】
综上所述,该敞口久置的“84”消毒液中溶质一定有________ 。 (3) 【交流反思】
生活中,“84”消毒液贮藏时应注意________;一般不用“84”消毒液对蔬菜、水果进行消毒,其原因可能是________ 。
【拓展延伸】
“84”消毒液中的NaClO与盐酸反应生成氯化钠、水和有毒的氯气。因此,“84”消毒液________(填“能”或“不能”)与洁厕灵(主要成分为盐酸)混合使用。
7. (1) 某饮用水中含有较多Ca(HCO3)2和Mg(HCO3)2 , 该水属于________(填“硬水”或“软水”),常用来烧开水的铝制水壶壶底有一层水垢。某实验小组对该水垢进行探究实验。
(2) [提出问题]
该水垢的主要成分是什么?
[查阅资料]
①水垢主要是由两种化合物组成的混合物。
②CaCO3、Mg(OH)2难溶于水,Ca(OH)2、MgCO3微溶于水。
[猜想与假设]
猜想一:Mg(OH)2、Ca(OH)2;
猜想二:________;
猜想三:CaCO3、Mg(OH)2;
猜想四:Ca(OH)2、MgCO3。
[设计实验]
(3) [结论与反思]
①通过以上实验得出结论猜想三成立。
②请说出理由:________。
(4) 写出实验③中CaCO3与盐酸反应的化学方程式:________。
[拓展与提升]
已知CaCO3、Mg(OH)2既能溶于盐酸也能溶于醋酸。如果让你处理该水壶中水垢,最好选择盐酸还是醋酸?说说你选择的理由:________。
实验步骤
实验现象
取少量上层料液,滴加________
________
另取少量上层料液,滴加________
产生白色沉淀
实验操作
实验现象
结论
⑴往盛有少量消毒液的试管中加入足量______,振荡。
产生大量气泡
猜想________不成立,化学方程式为________ 。
⑵向盛有蓝色布条的试管中加入适量该消毒液,放置一段时间。
蓝色布条________。(填“褪色”或“不褪色”)
猜想Ⅱ不成立,猜想Ⅲ成立。
实验步骤
实验现象
解释或结论
①取适量水垢于试管中加入足量水,充分振荡,再滴入几滴酚酞溶液
无明显现象
说明水垢中没有________(填化学式)
②取①的上层清液滴入稀盐酸中
无明显现象
说明水垢中没有________(填化学式)
③将①中上层液体倒出,向试管中加足量盐酸,并将涂有澄清石灰水的玻璃片盖在试管口
试管中的现象________,玻璃片上石灰水变浑浊
说明水垢中有CaCO3
④向③实验后的试管中加入足量氢氧化钠溶液
出现白色沉淀
说明水垢中有Mg(OH)2
2022中考化学实验探究题:物质制备类(冲刺型)(无答案): 这是一份2022中考化学实验探究题:物质制备类(冲刺型)(无答案),共14页。试卷主要包含了8g,6g.等内容,欢迎下载使用。
2022中考化学实验探究题:物质制备类(必考型)(无答案): 这是一份2022中考化学实验探究题:物质制备类(必考型)(无答案),共9页。
2022中考化学实验探究题:物质制备类(拔高型)(无答案): 这是一份2022中考化学实验探究题:物质制备类(拔高型)(无答案),共12页。试卷主要包含了 化学是一门以实验为基础的科学等内容,欢迎下载使用。