
湖北省华中师范大学第一附属中学2022---2023学年高一上学期新生入学测试化学试题(Word版含答案)
展开华中师大一附中2022级新生入学测试
化 学 试 题
满分: 100分 时限: 75分钟
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5 Ca 40 Fe 56 Ba 137
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.化学与生活密切相关,下列不涉及化学变化的是
A.乙酸钠过饱和溶液析出晶体并放热 B.北京冬奥会场馆使用CO2跨临界直冷制冰
C.科学家成功将CO2转化为淀粉或葡萄糖 D.切开的苹果放置后切面变色
2. 古医典富载化学知识,下述之物见其氧化性者为
A. 金(Au):“虽被火亦未熟"
B. 石灰(CaO):“以水沃之,即热蒸而解”
C. 石硫黄(S):“能化……银、铜、铁,奇物”
D. 石钟乳():“色黄,以苦酒(醋)洗刷则白”
3. 湖北省“铅锡刻镂技艺”是国家级非物质文化遗产之一,其为青铜器中繁复纹饰及铭文的制作与修复提供了高质高效的解决方案。下列说法错误的是
A. 锡在化学反应中易失电子 B. 铅锡合金适合做飞机的外壳材料
C. 铅锡合金熔点低于锡 D. 锡和铅最外层电子数相同
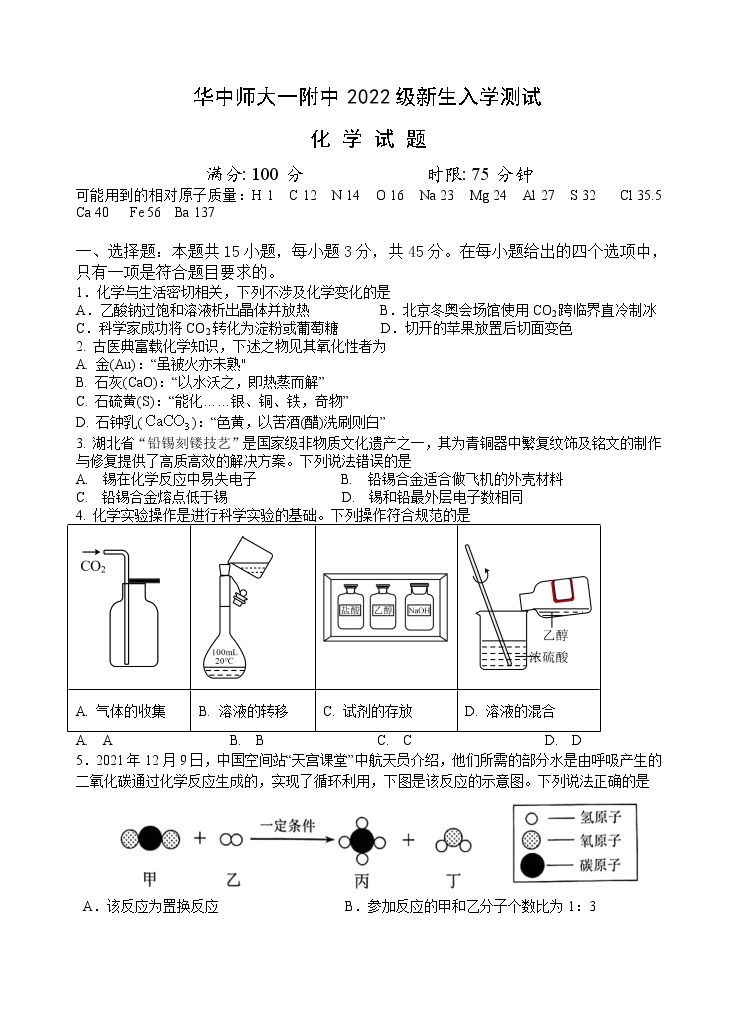
4. 化学实验操作是进行科学实验的基础。下列操作符合规范的是
A. 气体的收集 | B. 溶液的转移 | C. 试剂的存放 | D. 溶液的混合 |
A. A B. B C. C D. D
5.2021年12月9日,中国空间站“天宫课堂”中航天员介绍,他们所需的部分水是由呼吸产生的二氧化碳通过化学反应生成的,实现了循环利用,下图是该反应的示意图。下列说法正确的是
A.该反应为置换反应 B.参加反应的甲和乙分子个数比为1:3
C.甲和丙中碳元素的化合价不同 D.参加反应的甲和生成的丙质量比为1:1
6.下列关于各组物质的分类及说法正确的有几项
①混合物:氯水、漂白粉、水银、食醋、石灰水、CuSO4·5H2O
②胶体:饱和氯化铁溶液、蔗糖溶液、牛奶
③酸性氧化物:Mn2O7、CO2、NO、P2O5,碱性氧化物:Na2O、Na2O2、CaO、Al2O3
④酸:HCl、NaHCO3、H2SO4 , 碱:NaOH、Ba(OH)2、Na2CO3
⑤盐:KMnO4、MgCl2、H2O2、酒精
⑥电解质:BaSO4、NH3、NaOH、纯醋酸
⑦同素异形体:C60、C80、金刚石、石墨
⑧根据酸分子中含有的氢原子个数,将酸分为一元酸、二元酸和多元酸
⑨根据是否有丁达尔效应将分散系分为溶液、胶体和浊液
⑩根据化合物在水溶液中是否能导电分为电解质和非电解质
A.1 B.2 C.3 D.5
7. 能正确表示下列反应的离子方程式为
A.碳酸镁与稀盐酸反应:CO + 2H+ = CO2↑+ H2O
B.向CaCl2溶液中通入CO2:Ca2+ + H2O + CO2 = CaCO3↓ + 2H+
C.过氧化钠与水反应:Na2O2 + H2O = 2Na+ + 2OH- + O2↑
D. 将等物质的量浓度的Ba(OH)2和NH4HSO4溶液以体积比1∶2混合:
Ba2+ + 2OH- + 2H+ + SO= BaSO4↓ + 2H2O
8.室温下,下列各组离子在指定溶液中能大量共存的是
A.无色透明的溶液中:Fe3+、Mg2+、SCN–、Cl–
B.0.1 mol·L−1 AgNO3溶液:K+、Na+、Cl-、CO32-
C.加入Mg能放出H2的溶液中:Mg2+、Na+、SO42-、NH4+
D.使酚酞变红色的溶液中:Na+、NH4+、SO42-、Cl-
9.在2.8gFe中加入100mL 3mol/L HCl,Fe完全溶解。NA代表阿伏加德罗常数的值,下列说法正确的是(NA表示阿伏加德罗常数的值)
A.HCl溶液中Cl-数为3NA B.反应转移电子为0.1mol
C.2.8g 56Fe含有的中子数为1.3NA D.反应生成标准状况下气体3.36L
10.下列物质(括号内为杂质)的除杂试剂和除杂方法均正确的是
选项 | 物质 | 除杂试剂 | 除杂方法 |
A | CO2 (HCl) | 饱和Na2CO3溶液 | 洗气 |
B | 木炭粉(氧化铁) | 足量稀盐酸 | 过滤、洗涤、干燥 |
C | H2(CO) | 通过灼热的CuO | 洗气 |
D | MgCl2溶液(MgSO4) | 过量的BaCl2溶液 | 过滤 |
A.A B.B C.C D.D
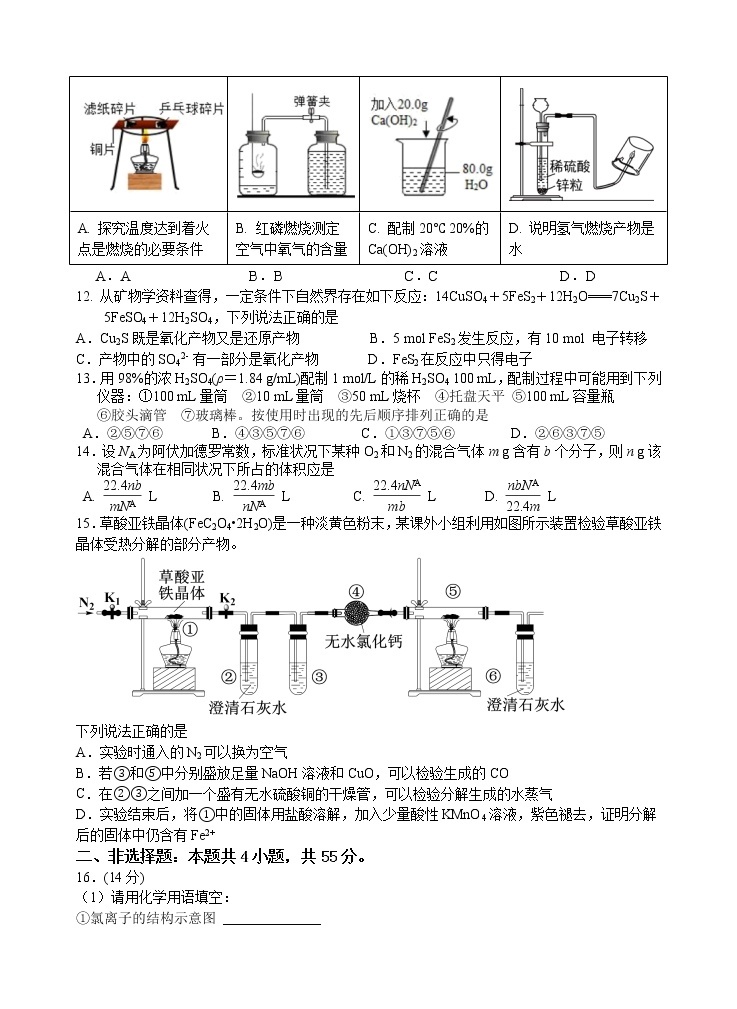
11. 利用如图装置进行实验,能达到实验目的的是
A. 探究温度达到着火点是燃烧的必要条件 | B. 红磷燃烧测定空气中氧气的含量 | C. 配制20℃ 20%的Ca(OH)2溶液 | D. 说明氢气燃烧产物是水 |
A.A B.B C.C D.D
12. 从矿物学资料查得,一定条件下自然界存在如下反应:14CuSO4+5FeS2+12H2O===7Cu2S+5FeSO4+12H2SO4,下列说法正确的是
A.Cu2S既是氧化产物又是还原产物 B.5 mol FeS2发生反应,有10 mol 电子转移
C.产物中的SO42- 有一部分是氧化产物 D.FeS2在反应中只得电子
13.用98%的浓H2SO4(ρ=1.84 g/mL)配制1 mol/L的稀H2SO4 100 mL,配制过程中可能用到下列仪器:①100 mL量筒 ②10 mL量筒 ③50 mL烧杯 ④托盘天平 ⑤100 mL容量瓶
⑥胶头滴管 ⑦玻璃棒。按使用时出现的先后顺序排列正确的是
A.②⑤⑦⑥ B.④③⑤⑦⑥ C.①③⑦⑤⑥ D.②⑥③⑦⑤
14.设NA为阿伏加德罗常数,标准状况下某种O2和N2的混合气体m g含有b个分子,则n g该混合气体在相同状况下所占的体积应是
A. L B. L C. L D. L
15.草酸亚铁晶体(FeC2O4•2H2O)是一种淡黄色粉末,某课外小组利用如图所示装置检验草酸亚铁晶体受热分解的部分产物。
下列说法正确的是
A.实验时通入的N2可以换为空气
B.若③和⑤中分别盛放足量NaOH溶液和CuO,可以检验生成的CO
C.在②③之间加一个盛有无水硫酸铜的干燥管,可以检验分解生成的水蒸气
D.实验结束后,将①中的固体用盐酸溶解,加入少量酸性KMnO4溶液,紫色褪去,证明分解后的固体中仍含有Fe2+
二、非选择题:本题共4小题,共55分。
16.(14分)
(1)请用化学用语填空:
①氯离子的结构示意图 ______________
②氨水显碱性的原因(电离方程式)_______________
(2)已知: H3PO2+NaOH(过量)=NaH2PO2+H2O。据此回答下列问题:
①该反应属于四种基本反应类型中的_______反应(选填“化合”、 “分解”、“置换”或“复分解”)。该反应_______ (选填“属 于”或“不属于”)氧化还原反应。
②H3PO2属于_______ (选填“一”、“二”或“三”)元酸。NaH2PO2属于_______ (选填“正盐”或“酸式盐”)。
(3)火箭发射时可用肼(N2H4)作燃料,NO2作氧化剂,生成N2和H2O。写出该反应的化学方程式___________________________。
(4)在一定条件下,RO3 n 和氟气可发生如下反应:RO3n + F2 + 2OH =RO4 +2F +H2O
从而可知在RO3 n 中,元素R的化合价为________
(5)下图是在一定温度下向不同电解质溶液中加入新物质时溶液的导电性发生的变化,其电流强度 (I) 随新物质加入量 (m) 的变化曲线,若澄清石灰水中通入CO2至过量,则符合变化趋势的图为_________
17.(14分)
(1)A~F是初中化学常见的六种物质,它们分别是单质、氧化物、有机物、酸、碱、盐中的一种,且均能通过化学反应生成水,如“雪花”图案所示(部分反应物、生成物和反应条件已略去)。已知A是稀盐酸,B是铁锈的主要成分,A能与某些金属反应生成D,且能与E发生中和反应,F为草木灰的主要成分。
① D的化学式为______。
②C属于上述物质类别中的______。
③E→H2O可用来检验二氧化碳,该化学方程式为______。
(2)某混合物的水溶液,只可能含有以下离子中的若干种:Na+、NH4+、Ba2+、Cl-、CO32-、SO42-。现取两份200 mL溶液进行如下实验:①第一份加足量NaOH溶液,加热,收集到气体1.36 g;②第二份加足量BaCl2溶液后,得干燥沉淀12.54 g,经足量盐酸洗涤干燥后,沉淀质量为4.66 g。根据上述实验进行推测:
溶液中一定不存在的离子是___________;可能存在的离子是__________;判断Na+是否存在____(填是或否);若存在其最小浓度为_______ mol·L-1,若不存在说明理由__________________。
18. (17分)化工专家侯德榜发明的侯氏制碱法为我国纯碱工业和国民经济发展做出了重要贡献,某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备NaHCO3,进一步处理得到产品Na2CO3和NH4Cl,实验流程如图:
回答下列问题:
(1)侯氏制碱的主要产品是Na2CO3,其俗名是________。
(2)生成NaHCO3的总反应的化学方程式为_________________。
(3)从下图A~E中选择合适的仪器制备NaHCO3,正确的连接顺序是________________
(按气流方向,用小写字母表示),A中仪器M的名称为_____________,B中使用雾化装置的优点是______________。
A. B. C.
D. E.
(4)反应完成后,将B中U形管内的混合物处理得到固体NaHCO3和滤液:
①灼烧 NaHCO3发生反应为: 2NaHCO3Na2CO3+H2O↑+CO2↑。
若灼烧前后固体质量减少1.24g,则生成的Na2CO3的质量为___________g。
②向滤液中加入NaCl粉末,存在NaCl(s)+NH4Cl(aq)→NaCl(aq)+NH4Cl(s)过程。为使NH4Cl沉淀充分析出并分离,根据NaCl和NH4Cl溶解度曲线,需采用的操作为蒸发浓缩、___、过滤、洗涤、干燥。
(5)工业纯碱中可能混有少量NaC1,同学们对工业纯碱样品展开探究。
探究一:确定纯碱样品中是否含有NaCI
实验操作 | 现象 | 结论 |
取样品加水溶解,加入过量稀盐酸至反应完全 | 有气泡产生 | 样品中有NaCl |
向上述溶液中继续滴加适量AgNO3溶液 | 有______产生 |
有同学认为该实验方案有错误,正确方案应选用______(填字母)代替稀盐酸。
a.CaCl2溶液 b.稀硝酸 c.BaC12溶液
探究二:测定纯碱样品中Na2CO3的质量分数
【方案1】称取m g样品溶解,加入过量CaC12溶液,搅拌至反应完全。过滤、洗涤、干燥,称量沉淀的质量为 n g,则样品中Na2CO3的质量分数为_______。
【方案2】如右图所示,取样品于锥形瓶中,加入足量稀盐酸。反应结束后,根据干燥管增重计算Na2CO3的质量分数。若结果大于100%,可能的原因是______。
19.(10 分)在初中化学“金属的性质”中有如下实验:将无锈铁钉浸入 CuSO4溶液,观察到铁钉表面出现红色物质。研究性学习小组对其展开了进一步探究。
【提出问题】Al 和 CuSO4溶液也能发生化学反应吗?
(1)预测 Al 能和 CuSO4溶液反应,理由是_____________________。
【进行实验】将一端缠绕的铝丝浸入 CuSO4溶液(如右图 ),观察现象。
(2)铝丝表面未出现红色物质,原因是____________________________。
【实验改进】用砂纸将铝丝表面打磨光亮,将其浸入 CuSO4溶液,观察现象。
(3)填写实验报告单:
序号 | 实验现象 | 结论与解释 |
① | 铝丝表面有少量气泡; 铝丝周围出现蓝绿色物质 | CuSO4溶液呈弱酸性,与 Al 反应产生的 气体是 ____________;蓝绿色物质成分待探究 |
② | 24h 后,铝丝仍光亮; 48h 后,铝丝表面出现少量红色物质 | 红色物质是________________,说明 Al 能和 CuSO4溶液反应,但反应较慢 |
③ | 铝丝周围溶液逐渐变成无色,铝丝 以下溶液仍为蓝色; 两层溶液界面清晰 | 反应生成的 Al2(SO4)3为无色; Al2(SO4)3 溶液的密度_________(填“>” 或“<”)CuSO4溶液 |
【深入探究】为研究上述异常现象,同学们查阅了相关资料,继续开展探究。
资料:①Cu2(OH)2SO4呈蓝绿色,不溶于水; ②Cl-可加快铝丝和其他物质的反应速率。
(4)取出铝丝,将试管中的混合物分离得到蓝绿色固体。加入稀硫酸,固体溶解形成蓝色溶液,该反应的化学方程式为___________________________________________________________。
(5)欲加快 Al 和 CuSO4溶液的反应,可加入的物质是_______________(填一种即可)。
【拓展应用】通过探究,同学们提出了铝制品使用的注意事项。
(6)下列食品不能长时间用铝制炊具盛放的是_____________(填序号)。
A.食醋 B.食用油 C.面粉 D.咸菜
参考答案
题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
答案 | B | C | B | A | C | A | D | C | B | B | A | C | D | A | B |
16. (14分)
(1) 略 (每空2分,共4分)
(2) 复分解 不属于 一 正盐 (每空1分,共4分)
(3) 2N2H4 + 2NO2 3N2 + 4H2O (无反应条件扣1分) (2分)
(4) +5 (2分)
(5) B (2分)
17. (14分)(每空2分)
(1)H2 有机物 Ca(OH)2 + CO2 = CaCO3 ↓+H2O
(2)Ba2+ ; Cl- ;是; 0.2 mol·L-1
18.(17 分)
(1)纯碱或苏打 (1分)
(2)NH3H2O+NaCl+CO2=NH4Cl+NaHCO3↓ (2分)
(3) aefbcgh (2分) 分液漏斗 (2分)
使氨盐水雾化,可增大与二氧化碳的接触面积,从而提高产率(或其他合理答案) (2分)
(4)①2.12(2 分) ②冷却结晶(1 分)
(5) ① 白色沉淀 (1分) ②b (1分) ③ 1.06n/m(2分)
④ 氢氧化钠固体吸收水蒸气或氯化氢气体 (1分)
19.(10 分)
(1)Al 比 Cu 活泼(或 Al 比 Fe 活泼)(1 分)
(2)铝丝表面有一层致密的氧化铝膜(1 分)
(3)①H2或氢气(1 分) ②Cu 或铜(1 分) ③<(1 分)
(4)Cu2(OH)2SO4+H2SO4===2CuSO4+2H2O(2 分)
(5)NaCl、CuCl2等含 Cl-物质的化学式或名称(1 分,其他合理答案均给分)
(6)AD(2 分,仅写一个答案,且正确给 1 分,有错不给分)
103,湖北省武汉市华中师范大学第一附属中学2023-2024学年高一上学期1月期末化学试题: 这是一份103,湖北省武汉市华中师范大学第一附属中学2023-2024学年高一上学期1月期末化学试题,共21页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
湖北省武汉市华中师范大学第一附属中学2023-2024学年高一上学期1月期末化学试题(Word版附答案): 这是一份湖北省武汉市华中师范大学第一附属中学2023-2024学年高一上学期1月期末化学试题(Word版附答案),共12页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
湖北省华中师范大学第一附属中学2021-2022学年高一上学期期末考试化学试题(含答案解析): 这是一份湖北省华中师范大学第一附属中学2021-2022学年高一上学期期末考试化学试题(含答案解析),文件包含精品解析湖北省华中师范大学第一附属中学2021-2022学年高一上学期期末考试化学试题原卷版docx、精品解析湖北省华中师范大学第一附属中学2021-2022学年高一上学期期末考试化学试题解析版docx等2份试卷配套教学资源,其中试卷共32页, 欢迎下载使用。












