



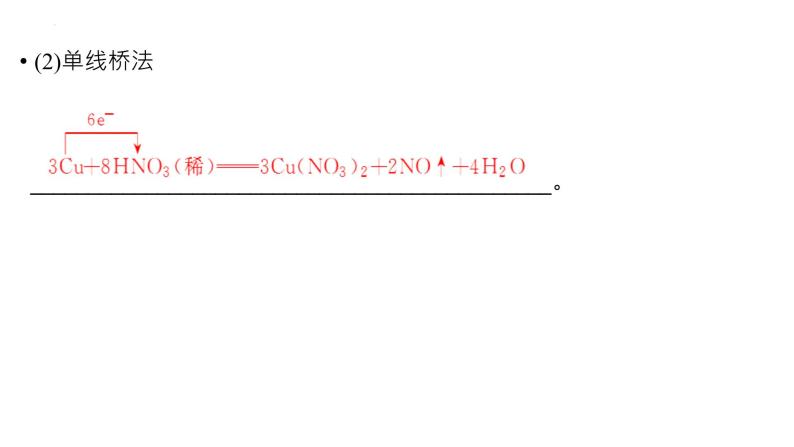
2023届高中化学一轮复习课件:氧化还原反应的基本概念和规律
展开[高考评价要求]1.了解氧化还原反应的本质是电子的转移。2.知道常见的氧化还原反应,并能利用氧化还原反应等概念对常见的反应进行分类和分析说明。3.能从元素价态的角度,依据氧化还原反应原理,预测物质的化学性质和变化。
考点 氧化还原反应的基本概念
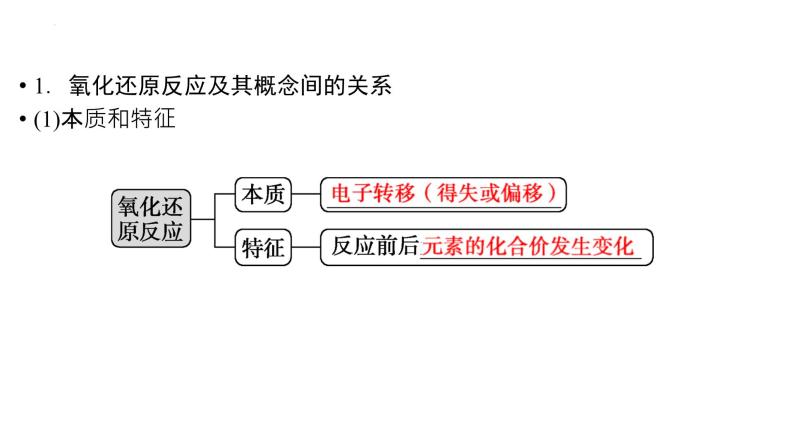
1.氧化还原反应及其概念间的关系(1)本质和特征
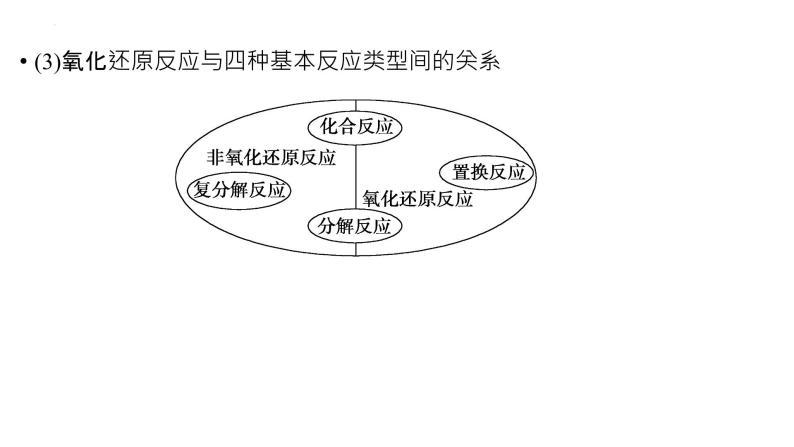
(3)氧化还原反应与四种基本反应类型间的关系
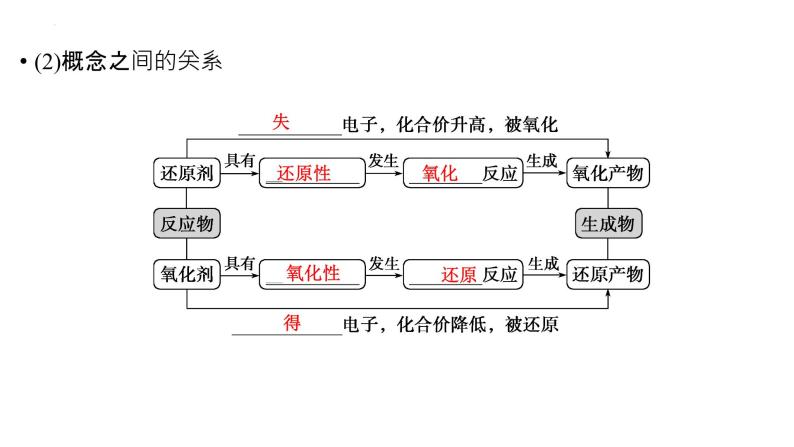
2.电子转移的表示方法请分别用双线桥法和单线桥法表示Cu与稀硝酸反应中电子转移的方向和数目:(1)双线桥法
_____________________________________________。
3.常见的氧化剂和还原剂(1)常见氧化剂常见氧化剂包括某些非金属单质、含高价态元素的化合物、过氧化物等。例如:
(2)常见还原剂常见还原剂包括活泼金属单质、非金属阴离子、含低价态元素的化合物、低价金属阳离子、某些非金属单质及其氢化物等。例如:
题组一 氧化还原反应中相关概念的理解1.菜谱中记载:河虾不宜与西红柿同食。主要原因是河虾中含有+5价砷,西红柿中含有比较多的维生素C,两者同食会生成有毒的+3价砷。下列说法正确的是( )A.在该反应中维生素C为氧化剂B.由上述信息可推知砒霜(As2O3)有毒C.因为河虾中含有砷元素,所以不能食用 D.上述反应中河虾中的+5价砷被氧化
2.某种飞船以N2H4和N2O4为动力源,发生反应:2N2H4+N2O4===3N2+4H2O,反应温度高达2 700 ℃,对于该反应,下列说法正确的是( )A.该反应属于置换反应 B.N2H4是氧化剂C.N2O4是还原剂 D.N2既是氧化产物又是还原产物
题组二 氧化还原反应中电子转移的分析方法3.下列化学方程式中电子转移方向、数目表示正确的是( )
氧化还原反应中电子转移数目的分析(1)基本方法:先标出熟悉元素的化合价,再根据化合物中正负化合价的代数和为零的原则求解其他元素的化合价。
考点 氧化性、还原性的强弱规律
1.氧化性、还原性的含义及判断(1)氧化性:__________的性质(或能力);还原性:_________的性质(或能力)。(2)氧化性、还原性的强弱取决于得失电子的_________程度,与得失电子数目的_____无关。如Na-e-===Na+,Al-3e-===Al3+,但根据金属活动性顺序,Na比Al活泼,更易失去电子,所以Na比Al的还原性强。
(3)从元素的价态判断①最高价态——只有________,如H2SO4、KMnO4等。②最低价态——只有________,如金属单质、Cl-、S2-等。③中间价态——既有________又有________,如Fe2+、S、Cl2等。
①元素处于最高价并不一定具有强氧化性。②一般情况下,元素化合价越高,氧化性越强,但氧化性:HClO>HClO2>……
2.氧化性、还原性强弱的比较方法(1)依据反应原理
C+SiO2、Na+KCl等在特定条件下的反应不能说明各元素还原性的强弱。
(2)依据金属、非金属的活动性顺序
2.下列所加物质的作用与其还原性无关的是( )A.果蔬饮料中加入维生素CB.葡萄酒中添加少量SO2C.月饼脱氧剂包中有铁粉D.面粉发酵时加入少量小苏打
考点 “价态”规律与“先后”规律
1.“价态”规律(1)升降规律:氧化还原反应中,化合价有升必有降,升降总值相等。(2)价态归中规律含不同价态的同种元素的物质间发生氧化还原反应时,该元素价态的变化一定遵循“高价+低价―→中间价”,而不会出现交叉现象。简记为“两相靠,不相交”。
如H2S与浓硫酸的反应:
(3)歧化反应规律具有多种价态的元素(如氯、硫、氮和磷元素等)均可发生歧化反应,遵循“中间价―→高价+低价”。如Cl2+2NaOH===NaCl+NaClO+H2O。
2.“先后”规律(1)同时含有几种还原剂时将按照还原性由强到弱的顺序依次反应。如向FeBr2溶液中通入少量Cl2时,因为还原性:Fe2+>Br-,所以Fe2+先与Cl2反应。(2)同时含有几种氧化剂时将按照氧化性由强到弱的顺序依次反应。如向含有Fe3+、Cu2+、H+的溶液中加入铁粉,因为氧化性:Fe3+>Cu2+>H+,所以铁粉先与Fe3+反应,然后依次与Cu2+、H+反应。
题组一 “价态”规律的应用1.(2021·湖南适应性考试)已知反应:2NaClO3+4HCl===2ClO2↑+Cl2↑+2NaCl+2H2O,下列关于该反应说法错误的是( )A.氧化性:NaClO3>Cl2B.当反应中有2 ml e-转移时,被氧化的HCl为4 mlC.氧化产物和还原产物的物质的量之比为1∶2D.产物ClO2和Cl2都可以用于自来水消毒杀菌
2.氯气跟氢氧化钾溶液在一定条件下发生反应:Cl2+KOH―→KX+KY+H2O(未配平),KX在一定条件下能自身发生反应:KX―→KY+KZ(未配平,KY与KZ的物质的量之比为1∶3)。以上KX、KY、KZ均是一元酸的钾盐,由以上条件推知在KX中氯元素的化合价是( )A.+1 B.+3C.+5 D.+7
题组二 “先后”规律的应用3.已知氧化性:Fe3+>M2+(M为不活泼的常见金属),向物质的量浓度均为1 ml·L-1的Fe2(SO4)3和MSO4的100 mL混合溶液中加入a ml铁粉,充分反应后,下列说法不正确的是( )A.当a≤0.1时,发生的反应为2Fe3++Fe===3Fe2+B.当0.1≤a<0.2时,溶液中n(Fe2+)=(0.2+a) mlC.当a≥0.2时,发生的反应为2Fe3++M2++2Fe===4Fe2++MD.若有固体剩余,则可能是铁
4.(2022·朔州高三模拟)向含有Fe2+、I-、Br-的溶液中通入适量Cl2,溶液中各种离子的物质的量变化如图所示。下列有关说法不正确的是( )A.线段BC代表Fe3+物质的量的变化情况B.原混合溶液中c(FeBr2)=6 ml·L-1C.当通入2 ml Cl2时,溶液中已发生的离子反应可表示为2Fe2++2I-+2Cl2===2Fe3++I2+4Cl-D.原溶液中n(Fe2+)∶n(I-)∶n(Br-)=2∶1∶3
1.(2020·新高考山东卷)下列叙述不涉及氧化还原反应的是( )A.谷物发酵酿造食醋B.小苏打用作食品膨松剂C.含氯消毒剂用于环境消毒D.大气中NO2参与酸雨形成
2.(2020·新高考北京卷)下列物质的应用中,利用了氧化还原反应的是( )A.用石灰乳脱除烟气中的SO2B.用明矾[KAl(SO4)2·12H2O]处理污水C.用盐酸去除铁锈(主要成分Fe2O3·xH2O)D.用“84”消毒液(有效成分NaClO)杀灭细菌
3.(2021·浙江6月选考)关于反应K2H3IO6+9HI===2KI+4I2+6H2O,下列说法正确的是( )A.K2H3IO6发生氧化反应B.KI是还原产物C.生成12.7 g I2时,转移0.1 ml电子D.还原剂与氧化剂的物质的量之比为7∶1
4.(2021·浙江1月选考)关于反应8NH3+6NO2===7N2+12H2O,下列说法正确的是( )A.NH3中H元素被氧化B.NO2在反应过程中失去电子C.还原剂与氧化剂的物质的量之比为3∶4D.氧化产物与还原产物的质量之比为4∶3
2024年高考化学一轮复习氧化还原反应的概念和规律课件: 这是一份2024年高考化学一轮复习氧化还原反应的概念和规律课件,共50页。PPT课件主要包含了目标导航,考点一,考点二,真题演练等内容,欢迎下载使用。
2024年高考化学一轮复习氧化还原反应基本概念课件: 这是一份2024年高考化学一轮复习氧化还原反应基本概念课件,共1页。
第六讲 氧化还原反应的基本概念和规律(课件)-【大一轮课堂】2024年高考化学大一轮复习课件+习题: 这是一份第六讲 氧化还原反应的基本概念和规律(课件)-【大一轮课堂】2024年高考化学大一轮复习课件+习题,共55页。PPT课件主要包含了复习目标,氧化剂和还原剂,真题验收制胜高考,知能训练素养落实等内容,欢迎下载使用。












