【最新版】初中升高高中化学衔接课程讲义专题17 铁的重要化合物
展开【知识回放】
铁在地壳中的含量仅次于 、 和 ,具第 位,主要以 和 形式存在。在Fe2O3中铁的化合价是 ,FeO中铁的化合价是 ,Fe3O4中铁的化合价是 。
【答案】氧 硅 铝 4 +2 +3 +3 +2 +2 和 +3
【新知精讲】
一、铁的重要化合物
1.铁的含量及存在形态
(1)含量:铁在地壳中的含量仅次于氧、硅和铝,居第四位。
(2)形态:铁的主要化合价为+2、+3,在地壳中主要是以化合物的形式存在。
2.铁的氧化物
名称 | 氧化亚铁 | 氧化铁 | 四氧化三铁 |
化学式 | FeO | Fe2O3 | Fe3O4 |
俗名 | — | 铁红 | 磁性氧化铁 |
铁的化合价 | +2 | +3 | +2、+3 |
颜色 | 黑色 | 红棕色 | 黑色 |
溶解性 | 不溶 | 不溶 | 不溶 |
稳定性 | 不稳定 | 稳定 | 稳定 |
氧化物类别 | 碱性氧化物 | 碱性氧化物 | 复杂氧化物 |
与盐酸反 应的离子 方程式 | FeO+2H+===Fe2++H2O、 Fe2O3+6H+===2Fe3++3H2O、 Fe3O4+8H+===2Fe3++Fe2++4H2O | ||
用途 | 氧化铁:红色油漆、涂料、炼铁原料 | ||
3.铁的氢氧化物
| Fe(OH)2 | Fe(OH)3[来源:Z|xx|k.Com] | |
颜色 | 白色 | 红褐色 | |
溶解性 | 不溶 | 不溶 | |
稳定性 | 在空气中易转化为Fe(OH)3 | 2Fe(OH)3 Fe2O3+3H2O | |
与盐酸反应(离子方程式) | Fe(OH)2+2H+===Fe2++2H2O | Fe(OH)3+3H+===Fe3++3H2O | |
制备(离子方程式)[来源:学+科+网Z+X+X+K] | Fe2++2OH-===Fe(OH)2↓ | Fe3++3OH-===Fe(OH)3↓ | |
转化[来源:Zxxk.Com] | 化学方程式 | 4Fe(OH)2+O2+2H2O===4Fe(OH)3[来源:学科网ZXXK] | |
现象 | 白色沉淀迅速变成灰绿色,最后变成红褐色 | ||
4.铁盐、亚铁盐
(1)Fe3+的检验:
(2)Fe2+和Fe3+的转化:
Fe2+Fe3+
写出下列反应的离子方程式:
①FeCl3溶液与铁粉:2Fe3++Fe===3Fe2+;
②FeCl2溶液与氯水:2Fe2++Cl2===2Fe3++2Cl-。
(3)铁盐的净水作用:铁盐在天然水中可生成Fe(OH)3胶体,和水中的悬浮物形成絮状不溶物沉降下来。
二、铜盐
1.铜属于重金属,化学性质不活泼,使用铜器皿比较安全。
2.硫酸铜、氯化铜、硝酸铜等铜盐易溶于水,都有毒。
3.铜绿的主要成分是Cu2(OH)2CO3,其难溶于水。
【科学探究】
探究一 “铁三角”的转化关系分析
问题导引
1.FeCl3溶液中逐渐加入锌粉的反应情况如何?
提示FeCl3溶液逐渐加入锌粉,开始FeCl3溶液过量,首先发生2Fe3++Zn===2Fe2++Zn2+,当锌粉过量后发生Fe2++Zn===Fe+Zn2+。
2.金属阳离子被还原一定得到金属单质吗?
提示 不一定。Fe3+被还原可以生成Fe,也可以被还原生成Fe2+。
探究二 Fe3+和Fe2+的检验、提纯
问题导引
1.若先加少量氯水,再加KSCN溶液,溶液变为红色,能否证明溶液中含有Fe2+?
提示 不能,因为若原溶液中含有Fe3+,也会有同样的现象,不能确定原溶液中一定含有Fe2+。
2.若Fe2(SO4)3溶液中可能含有Fe2+,用何种方法检验Fe2+是否存在?
提示 选用酸性KMnO4溶液,Fe2+可使紫色的酸性KMnO4溶液褪色。
【重点突破】
1.Fe、Fe2+ 、Fe3+性质
(1)Fe只有还原性,可以被氧化成+2价或+3价的铁
如Fe+2H+===H2↑+Fe2+
2Fe+3Cl22FeCl3
3Fe+4H2O(g) Fe3O4+4H2
(2)Fe2+既有氧化性又有还原性
如2Fe2++Cl2===2Fe3++2Cl- Zn+Fe2+===Fe+Zn2+
(3)Fe3+具有较强的氧化性,可被还原为+2价或0价的铁
如2Fe3++Cu===2Fe2++Cu2+
3CO+Fe2O3 2Fe+3CO2
2.Fe3+、Fe2+检验
(1)Fe3+、Fe2+的检验方法
| Fe2+ | Fe3+ |
观察法 | 浅绿色 | 棕黄色 |
加碱(NaOH)法 | ①现象:白色沉淀灰绿色红褐色沉淀 ②反应:Fe2++2OH-===Fe(OH)2↓(白色) 4Fe(OH)2+O2+2H2O===4Fe(OH)3(红褐色) | ①现象:红褐色沉淀 ②应:Fe3++3OH-===Fe(OH)3↓(红褐色) |
加盐(SCN-)法 | ①现象:加入KSCN溶液无明显现象,再滴入氯水变成红色溶液 ②反应:2Fe2++Cl2===2Fe3++2Cl- Fe3++3SCN-===Fe(SCN)3(红色) | ①现象:加入KSCN溶液,溶液变为红色 ②反应:Fe3++3SCN-===Fe(SCN)3(红色) |
(2)Fe3+与Fe2+检验时的注意事项
①根据Fe3+、Fe2+的颜色利用观察法检验Fe3+、Fe2+时,适用于浓度较大时,若溶液较稀,离子浓度较小,易产生干扰,一般不用此法检验。
②利用KSCN检验Fe2+时,要注意加入试剂的顺序,即先加入KSCN溶液,再加入氯水,以免发生误检。
③Fe3+与SCN-作用后的“溶液”显红色,注意并不是“沉淀”。
【典题探究】
典例1
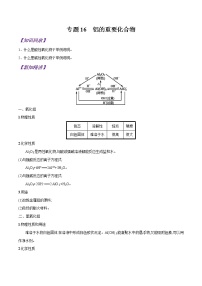
已知有以下物质相互转化
试回答:(1)B的化学式: 、D的化学式: 。
(2)写出由E转变成F的化学方程式: 。
(3)常用 检验G中的阳离子,其现象为 。
(4)向G溶液加入A的有关反应的离子方程式为 。
【答案】:(1)FeCl2 KCl 学&科网
(2)4Fe(OH)2+2H2O+O2===4Fe(OH)3
(3)KSCN溶液 棕黄色溶液变为红色溶液
(4)2Fe3++Fe===3Fe2+
变式训练1-1
按下图要求写出下列三个反应的化学方程式,属于离子反应的只写出离子方程式。
(1)BC+D: ;
(2)EF: ;
(3)FD: 。
【答案】:(1)Fe3O4+8H+===Fe2++2Fe3++4H2O
(2)4Fe(OH)2+O2+2H2O===4Fe(OH)3
(3)Fe(OH)3+3H+===Fe3++3H2O
变式训练1-2
除去FeCl2溶液中少量的FeCl3,最好的办法是( )
A.加入氢氧化钠溶液 B.通入氯气
C.加入铜粉 D.加入铁粉
【答案】:D
【解析】:要实现“Fe3+→Fe2+”的转化,需要加入还原剂,且不引入新的杂质离子,最好的办法是加入足量铁粉充分反应后过滤,发生的化学反应为2FeCl3+Fe===3FeCl2。学&科网
变式训练1-3
下列关于Fe2+和Fe3+的叙述中,错误的是( )
A.Fe2+的水溶液为浅绿色
B.Fe3+的水溶液为黄色
C.Fe3+具有氧化性,Fe2+具有还原性
D.Fe3+溶液中滴入含SCN-的溶液,立即出现红色沉淀
【答案】:D
【解析】:Fe3+溶液中滴入含SCN-的溶液,生成红色可溶性物质,不是红色沉淀。
典例2
向某溶液中加入含Fe2+的溶液后,无明显变化。当再滴入几滴新制氯水后,混合溶液变成红色,则下列结论错误的是( )
A.该溶液中一定含有SCN-
B.氧化性:Fe3+>Cl2
C.Fe2+与SCN-不能形成红色物质
D.Fe2+被氧化为Fe3+
【答案】:B
变式训练2-1
要证明某溶液中不含Fe3+,而可能含有Fe2+,进行如下实验操作的最佳顺序为( )
①加入足量氯水
②加入足量酸性KMnO4溶液
③加入少量KSCN溶液
A.①③ B.③②
C.③① D.①②③
【答案】:C
【解析】:先加入少量KSCN溶液,若无红色,证明无Fe3+,然后加足量的氯水,若出现红色,说明有Fe2+存在。不用加入足量酸性KMnO4溶液的原因是酸性KMnO4溶液是紫红色的溶液,干扰Fe2+检验。学&科网
变式训练2-2
硫酸亚铁缓释片可以补铁、防治贫血,但存放不当很容易变质,药片中的Fe2+被氧化生成Fe3+。若将药片配成溶液,需使用刚刚煮沸过又冷却的蒸馏水,原因是 。
实验室检验Fe3+,除了可以用碱外,常用的试剂是 (填化学式),若 ,则证明有Fe3+。
【答案】:防止水中溶解的氧气氧化Fe2+ KSCN 溶液变成红色
【解析】:硫酸亚铁缓释片溶于水时,药片中的Fe2+易被水中溶解的O2氧化为Fe3+,因此将药片配成溶液时,应预先将蒸馏水煮沸,以除去水中溶解的O2;检验Fe3+,还可以用KSCN溶液,Fe3+与SCN-发生反应使溶液变红色。
变式训练2-3
下列离子的检验方法合理的是( )
A.向某溶液中滴入KSCN溶液呈红色,说明不含Fe2+
B.向某溶液中通入Cl2,然后再加入KSCN溶液变红色,说明原溶液中含有Fe2+
C.向某溶液中加入NaOH溶液,得到红褐色沉淀,说明溶液中含有Fe3+
D.向某溶液中加入NaOH溶液得白色沉淀,又观察到颜色逐渐变为红褐色,说明溶液中含有Fe2+,不含有Mg2+
【答案】:C
【最新版】初中升高高中化学衔接课程讲义专题25 硝酸的氧化性: 这是一份【最新版】初中升高高中化学衔接课程讲义专题25 硝酸的氧化性,文件包含专题25硝酸的氧化性-初升高化学衔接精品专题解析版doc、专题25硝酸的氧化性-初升高化学衔接精品专题原卷版doc等2份学案配套教学资源,其中学案共12页, 欢迎下载使用。
【最新版】初中升高高中化学衔接课程讲义专题24 浓硫酸的特性: 这是一份【最新版】初中升高高中化学衔接课程讲义专题24 浓硫酸的特性,文件包含专题24浓硫酸的特性-初升高化学衔接精品专题解析版doc、专题24浓硫酸的特性-初升高化学衔接精品专题原卷版doc等2份学案配套教学资源,其中学案共13页, 欢迎下载使用。
【最新版】初中升高高中化学衔接课程讲义专题23 氨: 这是一份【最新版】初中升高高中化学衔接课程讲义专题23 氨,文件包含专题23氨-初升高化学衔接精品专题解析版doc、专题23氨-初升高化学衔接精品专题原卷版doc等2份学案配套教学资源,其中学案共18页, 欢迎下载使用。