
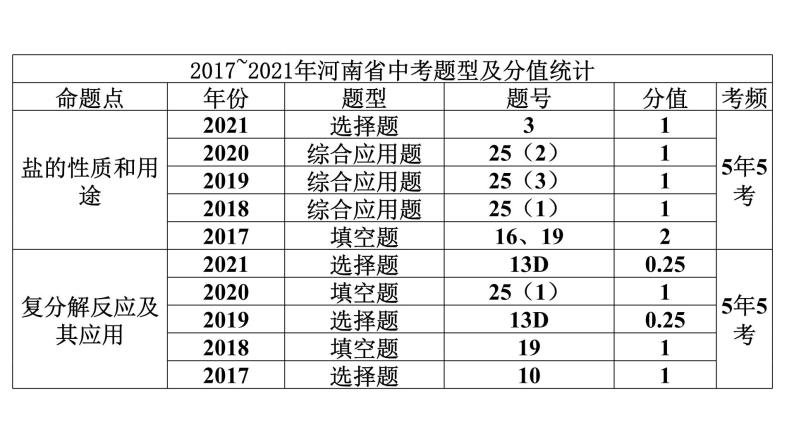
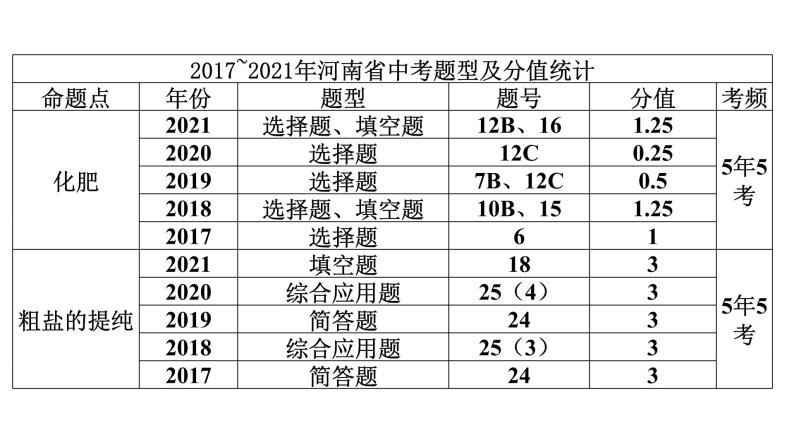


2022中考化学(人教版)单元复习 第1部分 第11单元 基础过关课件PPT
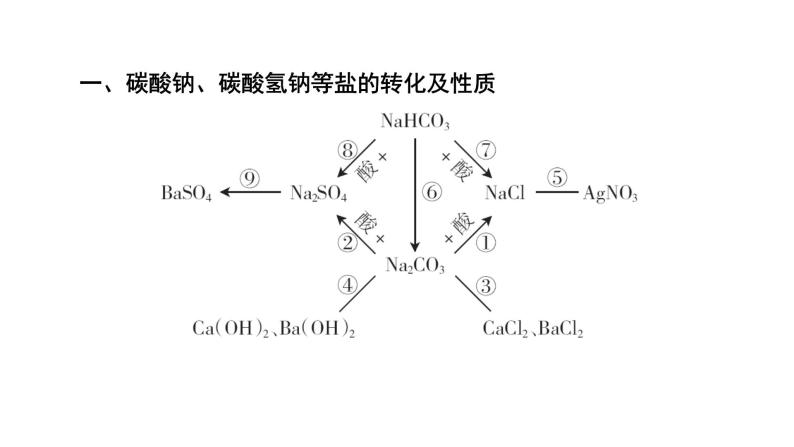
展开一、碳酸钠、碳酸氢钠等盐的转化及性质
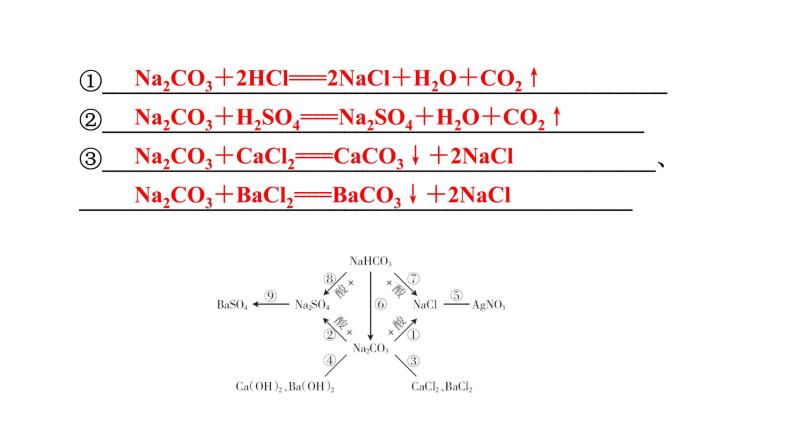
①_________________________________________________②_______________________________________________③________________________________________________、________________________________________________
Na2CO3+2HCl===2NaCl+H2O+CO2↑ Na2CO3+H2SO4===Na2SO4+H2O+CO2↑ Na2CO3+CaCl2===CaCO3↓+2NaCl Na2CO3+BaCl2===BaCO3↓+2NaCl
④__________________________________________________、__________________________________________________⑤_______________________________________________⑥______________________________________⑦_________________________________________________
Na2CO3+Ca(OH)2===CaCO3↓+2NaOH Na2CO3+Ba(OH)2===BaCO3↓+2NaOH NaCl+AgNO3===AgCl↓+NaNO3
NaHCO3+HCl===NaCl+H2O+CO2↑
⑧__________________________________________________⑨__________________________________________________ ____________________________________________________________________________________________________
2NaHCO3+H2SO4===Na2SO4+2H2O+2CO2↑ Na2SO4+BaCl2===BaSO4↓+2NaCl [或Na2SO4+Ba(OH)2===BaSO4↓+2NaOH, 或Na2SO4+Ba(NO3)2===BaSO4↓+2NaNO3]
二、含钙化合物的转化①_______________________________②_________________________________________________________ _________________________________________
CaO+H2O===Ca(OH)2
Ca(OH)2+2HCl===CaCl2+2H2O[或Ca(OH)2+MgCl2=== CaCl2+Mg(OH)2↓等]
③_________________________________________________________ _____________________________________④___________________________⑤________________________________________________⑥________________________________________________
Ca(OH)2+Na2CO3===CaCO3↓+2NaOH[或Ca(OH)2+CO2===CaCO3↓+H2O] CaCO3+2HCl===CaCl2+H2O+CO2↑ CaCl2+Na2CO3===CaCO3↓+2NaCl
一、盐的性质和用途(必考)1.生活中常见的盐
2.常见的有颜色的盐溶液
3.盐的化学性质(后四条为盐的通性,即“盐四条”)
2AgNO3+Cu===Cu(NO3)2+2Ag
CuSO4+Fe===FeSO4+Cu
Na2CO3+2HCl=== 2NaCl+H2O+CO2↑ CaCO3+2HCl=== CaCl2+H2O+CO2↑ NaHCO3+HCl=== NaCl+H2O+CO2↑
AgNO3 +HCl=== AgCl↓+HNO3 BaCl2+H2SO4=== BaSO4↓+2HCl
Na2CO3+Ca(OH)2=== CaCO3↓+2NaOH MgCl2+2NaOH === Mg(OH)2↓+2NaCl Na2SO4+Ba(OH)2=== BaSO4↓+2NaOH CuSO4+2NaOH === Cu(OH)2↓+Na2SO4
Na2CO3+CaCl2=== CaCO3↓+2NaCl Na2CO3+BaCl2=== BaCO3↓+2NaCl BaCl2+CuSO4 === BaSO4↓+CuCl2
三、化学肥料(必考)1.化肥的分类和主要作用(2018~2021、2012~2016考)
2.化肥的简易鉴别(10年4考,2021、2017~2019考)
3.使用化肥、农药与环境的关系(1)不合理施用化肥对环境的影响:造成大气污染(产生氮化物和硫化物气体)、水污染(氮、磷含量升高使水体富营养化)、土壤污染(造成土壤酸化、板结)。(2)农药使用不当会造成环境污染,农产品上残留的农药会危害人体健康。
命题点1 盐的性质和用途(10年10考)1. (2021,3)侯德榜是我国制碱工业的先驱。侯氏制碱法中的“碱”是指纯碱,其化学式为( )A.Na2CO3B.NaHCO3C.NaOHD.NaCl2.(2018,25节选)(1)焙制糕点所用发酵粉中含有碳酸氢钠,其俗名为_____(填字母代号)。a.纯碱 b.烧碱 c.苏打 d.小苏打
3.(2014,3)发明了“联合制碱法”的科学家是( )
4.(2017,10)右图表示向一定量CaCl2和盐酸混合溶液中滴加Na2CO3溶液的变化过程。x表示Na2CO3溶液的质量,则y可能表示( )A.气体的体积B.沉淀的质量C.NaCl的质量D.混合溶液的pH
5.(2017,16节选;2011,14节选)在医疗上可用小苏打治疗胃酸(HCl)过多症,其原理是___________________________________________ (用化学方程式表示)。
NaHCO3+HCl===NaCl+CO2↑+H2O
6.(2012,20)有一包白色粉末,其中含有CuSO4、BaCl2、NaOH、Na2CO3中的一种或几种。某化学小组为确定白色粉末的成分,进行了如下实验:(Ⅰ)取一定量的白色粉末,加入足量水,振荡,得到无色透明溶液;(Ⅱ)取少量(Ⅰ)的溶液,加入足量盐酸,有气泡产生。(1)该白色粉末中肯定含有什么物质?可能含有什么物质?肯定含有Na2CO3,可能含有NaOH。(2)为确定可能含有的物质是否存在,还需做什么实验?请写出简要的实验步骤。取少量(Ⅰ)的溶液,加入足量的BaCl2(或CaCl2)溶液,静置,取上层清液滴加酚酞溶液。
命题点2 复分解反应及其应用(10年10考)7.(2018备用卷,12)下列各组物质中,能发生复分解反应且反应前后溶液总质量变小的是( )A.锌和稀硫酸B.氢氧化钠溶液和盐酸C.硫酸和氯化钡溶液D.氯化钾溶液和硫酸钠溶液
8.(2014,10)下列各组物质中,能相互反应且反应前后溶液总质量保持不变的是( )A.铝和硫酸铜溶液B.硫酸和烧碱溶液C.氧化铁固体和盐酸D.碳酸钾溶液和硝酸钠溶液9.(2019备用卷,13)下列各组物质在pH=1的溶液中能大量共存且溶液为无色的是( )A.NaCl、KOH、Na2CO3B.KNO3、HCl、CaCl2C.Na2SO4、FeCl3、NaNO3D.BaCl2、NH4NO3、H2SO4
10.(2016备用卷,10)下列物质能在pH=13的溶液中大量共存且溶液为无色的是( )A.HCl、AgNO3、Na2CO3B.NaNO3、KNO3、NH4ClC.K2SO4、K2CO3、NaOHD.KMnO4、CuSO4、NaNO3
11.(2016,23节选)(1)复分解反应发生后,生成物肯定是_______(填“单质”或“化合物”)。12.(2013,21节选)(1)复分解反应发生的条件是有沉淀析出,或有气体放出,或有_________________生成。
命题点3 化肥(10年10考)13.(2017,6)下列化肥分别与熟石灰混合研磨后,能闻到刺激性气味的是( )A.NH4ClB.KNO3C.NaNO3D.Ca3(PO4)2
16.(2021,16节选)施用化肥是农业增产的重要手段,尿素[CO(NH2)2]属于_______(填“氮肥”“磷肥”或“钾肥”)。17.(2018,15节选)在尿素、硫酸钾、磷酸二氢铵三种化肥中,属于复合肥料的是_____________。命题点4 粗盐的提纯(详见中招对点练11)
1.实验用品烧杯、玻璃棒、蒸发皿、坩埚钳、酒精灯、漏斗、药匙、量筒(10 mL)、铁架台(带铁圈)、托盘天平、滤纸、火柴。2.实验操作
粗盐中难溶性杂质的去除
蒸发皿中出现较多固体
【总结】本实验中玻璃棒的作用
防止因局部温度过高,造成液滴飞溅
例题 (2021营口)如图为“去除粗盐中难溶性杂质并计算产率”的实验操作示意图:(1)请将上述操作进行合理排序:_____________(填序号)、计算产率;操作④中的错误是_________________。
(2)操作②中,用玻璃棒不断搅拌的目的是_____________________ ______________。(3)过滤后,如果滤液仍然浑浊,原因可能是__________________ ___________________________________________________。
滤纸破损(或过滤时漏斗内液面高于滤纸边缘,或盛接滤液的烧杯不干净等)
(4)下列情况可能导致精盐产率偏低的是_______。A.溶解时加入的水过少导致粗盐未溶完B.过滤时漏斗内液面高于滤纸边缘C.所得精盐中含有少量水分D.转移时有部分精盐残留在蒸发皿上
考点 盐的性质和用途
例1 (2021鞍山)下列有关盐的用途说法不正确的是( )A.氯化钠可用于配制生理盐水B.碳酸钙可用作补钙剂C.亚硝酸钠可用于腌制蔬菜D.小苏打可用于焙制糕点
(1)反应①选用的盐是___________,该反应属于___________(填基本反应类型)。
例2 如图为“盐的化学性质”思维导图,图中四个反应的反应物如表所示(每种物质只能选用一次)。
(2)反应③生成的盐不溶于水,且在高温下能分解为_________和_______ (填化学式)。(3)写出下列序号对应反应的化学方程式:②__________________________________________;④_________________________________________。
CaCO3+2HCl===CaCl2+H2O+CO2↑ BaCl2+Na2SO4===BaSO4↓+2NaCl
1.(2020柳州)向甲物质中逐滴加入X溶液至过量,生成沉淀或气体的质量与加入X溶液的质量关系不符合如图的是( )
2.(2020青岛改编)化学课堂上,同学们分小组合作探究碳酸钠的性质,请你参与探究并填空。【实验记录与分析】
Na2CO3能与CaCl2发生反应
【反思与拓展】(1)分析实验一可得出:盐溶液_________(填“一定”或“不一定”)显中性。(2)对比实验三、四的现象,从微观角度分析,两个反应的实质相同,即溶液中相互结合的离子都是________________________________ _____。
(3)实验结束后,同学们将四支试管中的物质倒入同一烧杯内,静置,观察到烧杯底部有白色固体,上层为红色溶液。①为处理废液,将烧杯内混合物过滤后,向红色滤液中加入稀盐酸,有气泡产生,说明滤液中一定没有的溶质是_______(填序号)。A.NaOHB.Na2CO3C.CaCl2D.Ca(OH)2②继续加入稀盐酸至溶液颜色恰好为无色,此时溶液中的溶质除酚酞外还有___________(填化学式)。
考点 复分解反应及其应用(重难、易错点)
考向1 判断复分解反应能否发生例3 下列物质混合,能发生复分解反应且有明显现象的是( )A.铝与硫酸亚铁溶液B.氢氧化钠溶液与氯化镁溶液C.澄清石灰水与稀盐酸D.硫酸钠溶液与氯化铜溶液
考向2 判断物质或离子能否共存例4 已知某无色溶液中大量共存的物质有KNO3、HCl、X、NH4Cl,其中X可能是( )A.AgNO3B.KOHC.Na2SO4D.FeCl3
技巧点拨 判断物质或离子能否共存时,主要看物质相互交换成分或阴、阳离子相互结合是否有沉淀、气体或水生成,若有沉淀、气体或水生成,则不能共存。解题时还应注意题目中的附加条件,如:①溶液的酸碱性。若溶液呈酸性,还应判断各物质能否与H+发生反应;若溶液呈碱性,还应判断各物质能否与OH-发生反应;若溶液呈中性,则溶液中不含H+或OH-。②溶液的颜色。若溶液为无色,则不可能存在Cu2+、Fe2+、Fe3+等离子。
考向3 物质的检验与鉴别例6 (2021解析与检测)有一包白色固体样品,可能含有NaOH、Na2CO3、K2SO4、BaCl2中的一种或几种,为确定其组成,进行如下实验:步骤Ⅰ:取少量样品于烧杯中,加入足量水,充分搅拌,静置,有固体剩余。
步骤Ⅱ:取步骤Ⅰ所得上层清液于试管中,滴入几滴酚酞溶液,溶液变为红色;再滴入过量稀盐酸,无气泡产生,红色逐渐褪去,得到无色溶液。步骤Ⅲ:取步骤Ⅱ所得溶液于试管中,滴入过量Ba(NO3)2溶液,无明显现象。
根据上述实验,回答下列问题:(1)步骤Ⅱ中溶液的红色褪去,发生反应的化学方程式是_________________________________。(2)分析上述实验过程,关于样品的组成,可以得到的结论是什么?该样品中一定含有BaCl2和NaOH,至少含有Na2CO3和K2SO4中的一种。
NaOH+HCl===NaCl+H2O
(3)若要进一步确定样品的组成,还需进行的实验是什么?(写出实验操作、现象及结论)取少量步骤Ⅰ所得固体于试管中,滴入足量稀盐酸,若固体不溶解,则样品中含有K2SO4;若固体完全溶解,则样品中含有Na2CO3;若固体部分溶解,则样品中含有Na2CO3和K2SO4。
3.下列各组物质的稀溶液,根据自身的性质和相互间的反应,不用其他试剂就可以鉴别的是( )A.FeCl3 NaNO3 K2SO4B.CuCl2 KCl KOHC.NaNO3 H2SO4 KClD.BaCl2 NaOH KNO3
考向4 判断物质之间能否发生转化例7 (2021梧州)“X→Y→Z”物质间转化,均可通过一步反应实现的是( )
技巧点拨 一般情况下AgCl、BaSO4、KNO3、NaNO3等不能一步转化为其他物质。
4.甲、乙两种物质间有如图所示的转化关系(“→”表示一步实现,部分物质和反应条件略去)。不符合上述要求的一组物质是( ) A.NaCl、NaNO3B.NaOH、Na2CO3C.CaCO3、CaCl2D.CuSO4、Cu(OH)2
考点 化肥的分类和检验
例8 (2021青海)小明发现爸爸买回的化肥有CO(NH2)2、KCl、KNO3,其中还缺少的化肥是( )A.氮肥B.复合肥C.钾肥D.磷肥
例9 下列区分化肥的方法不可行的是( )A.NH4HCO3与K2SO4:闻气味B.NH4NO3与KCl:加水溶解C.(NH4)2SO4与NH4Cl:加熟石灰研磨 D.CO(NH2)2与磷矿粉:观察外观
2022中考化学(人教版)单元复习 第1部分 第12单元 基础过关课件PPT: 这是一份2022中考化学(人教版)单元复习 第1部分 第12单元 基础过关课件PPT,共40页。PPT课件主要包含了知识梳理,蛋白质,维生素,夜盲症,坏血病,佝偻病和发育不良,甲状腺肿大,烧焦羽毛,河南真题,葡萄糖等内容,欢迎下载使用。
2022中考化学(人教版)单元复习 第1部分 第9单元 基础过关课件PPT: 这是一份2022中考化学(人教版)单元复习 第1部分 第9单元 基础过关课件PPT,共60页。PPT课件主要包含了知识梳理,被溶解,能溶解其他物质,NH4NO3,NaOH,浓H2SO4,NaCl,显著增大,KNO3,CaOH2等内容,欢迎下载使用。
2022中考化学(人教版)单元复习 第1部分 第7单元 基础过关课件PPT: 这是一份2022中考化学(人教版)单元复习 第1部分 第7单元 基础过关课件PPT,共60页。PPT课件主要包含了知识梳理,可燃物,3常见灭火实例,隔绝氧气或空气,清除或隔离可燃物,检验气体,的纯度,严禁烟火,新能源必考,生物质能等内容,欢迎下载使用。












