



常见的酸PPT课件免费下载
展开一、【课程的主要内容】
1、碳酸钙和稀盐酸反应2、氢氧化钙和稀盐酸反应3、二氧化碳通入澄清石灰水4、二氧化碳和水反应5、碳酸受热分解6、氢氧化钙和碳酸钠反应7、用双氧水和二氧化锰制备氧气8、硝酸银和稀盐酸反应9、硝酸银和碳酸钠反应10、碳酸银和稀硝酸反应
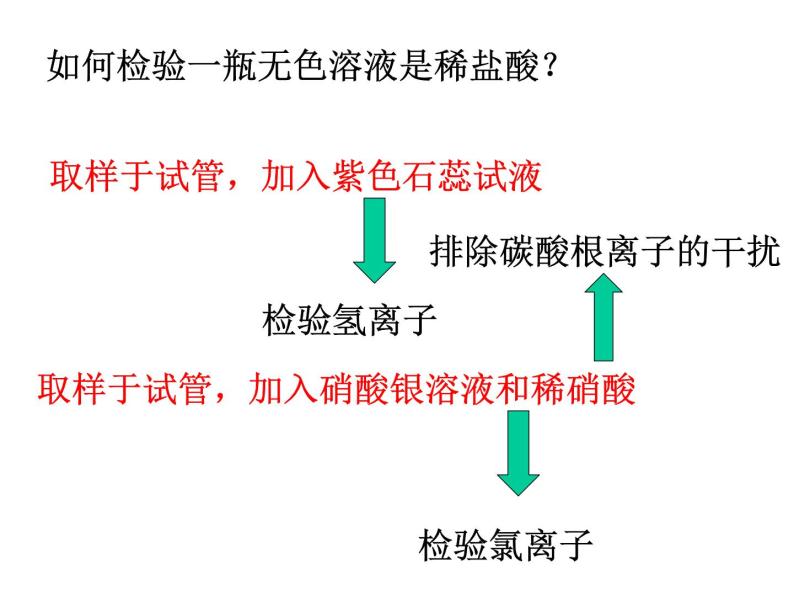
如何检验一瓶无色溶液是稀盐酸?
取样于试管,加入紫色石蕊试液
取样于试管,加入硝酸银溶液和稀硝酸
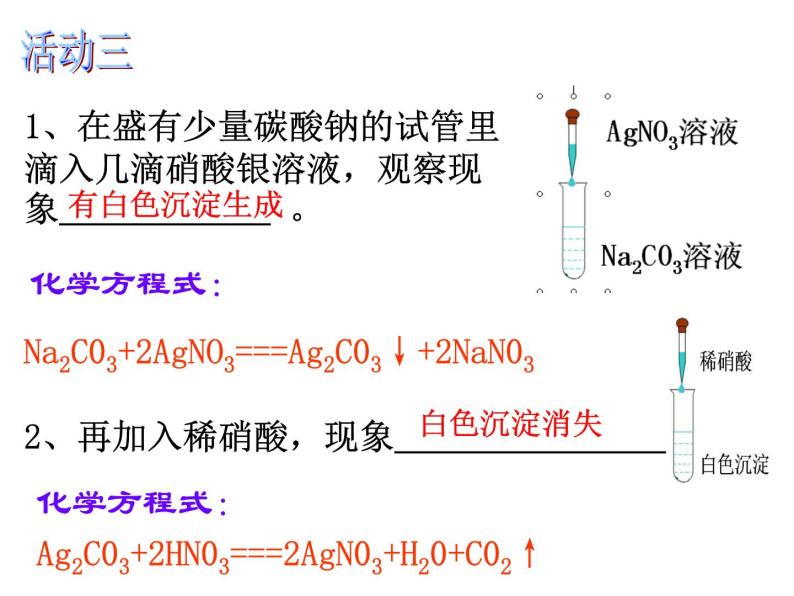
1、在盛有少量碳酸钠的试管里滴入几滴硝酸银溶液,观察现象 。
2、再加入稀硝酸,现象 。
Na2C03+2AgNO3===Ag2C03↓+2NaN03
Ag2C03+2HN03===2AgN03+H20+C02↑
实验桌上有未贴标签的稀盐酸和NaCl溶液(中性溶液),请同学们设计实验鉴别。
分别取两溶液少许于试管中,再分别滴加石蕊试液
(1)为什么不用酚酞来区别? (2)ⅹⅹ小组是用石蕊来鉴别,那么你能否告诉我通过你的探究你认为是稀盐酸中的什么微粒使石蕊溶液变红?
不能!酚酞溶液遇稀盐酸和NaCl溶液都不变色。
石蕊溶液本身含有水,因此不是水分子的作用;NaCl溶液中有Cl-,而NaCl溶液不能使石蕊溶液变红,那么也不是Cl-的作用;应该是酸中的H+使石蕊溶液变红。
注意: 酸碱指示剂与酸或碱的溶液反应时, 变色的是指示剂,而不是酸、碱
判断:1、酸溶液能使紫色的石蕊溶液变成红色( )2、紫色的石蕊溶液遇到酸溶液变成红色( )3、紫色的石蕊溶液使酸溶液变成红色 ( )
把鸡蛋壳放入盛有盐酸的试管中,将燃着的火柴伸入试管口,如图所示。你看到了什么现象?反应的化学方程为
CaCO3 + 2HCl=CaCl2 + CO2↑+ H2O
蛋壳表面产生大量气泡,燃着的火柴会熄灭
二、【思考与探究】
化学性质2、盐酸能与某些盐反应生成盐酸盐和新的酸
方法一:样品中滴入稀盐酸,产生气泡
方法二:样品中滴入稀盐酸,产生气泡,放入燃着的木条,木条熄灭
方法三:样品中滴入稀盐酸,产生气泡,将气体通入澄清石灰水,澄清石灰水变浑浊
向盛有少量氢氧化铜粉末的试管中加入2毫升盐酸。你看到了什么现象? ______________________________________。反应的化学方程式为: 。
蓝色固体消失,溶液变成蓝色
Cu(OH)2 + 2HCl=CuCl2 +2H2O
化学性质3、盐酸能与碱反应生成盐酸盐和水
向盛有少量氧化铜粉末的试管中加入2毫升盐酸,微微加热。你看到了什么现象? ______________________________________。反应的化学方程式为: 。
CuO + 2HCl=CuCl2 +H2O
黑色粉末消失,溶液变成蓝色
化学性质4、盐酸能与某些金属氧化物反应生成盐酸盐和水
氧化铜可以溶解在稀盐酸中
取一枚生锈的铁钉(铁锈的主要成分是Fe2O3 ),观察它的颜色。小心地让生锈的铁钉沿着试管壁滑到试管底部,向试管中滴加少量稀盐酸。铁钉表面和溶液颜色发生了什么变化?铁锈与盐酸反应主要的化学方程式为:
铁锈消失,溶液变成黄色
Fe2O3 + 6HCl=2FeCl3 + 3H2O
稀盐酸可以用于除铁锈,可观察到_____________,反应的化学方程式为__________________。
Fe2O3 + 6HCl === 2FeCl3 + 3 H2O
后来看到铁钉表面有气泡生成,而铁锈中的氧化铁与稀盐酸反应时却没有气体产生,那么这气体是怎么来的?是什么?是否是铁与稀盐酸反应产生的呢?
A试管中Fe2O3溶解,溶液变黄色,无气泡产生。
B试管中铁钉表面产生气泡,溶液浅绿色
Fe + 2HCl === FeCl2 + H2 ↑
三、【拓展学习】
活动:其他金属能与稀盐酸反应吗?
试管中锌粒表面产生气泡。
锌、铁与稀盐酸反应的化学方程式是:
Fe + 2HCl === FeCl2 + H2 ↑Zn + 2HCl === ZnCl2 + H2↑
铁等金属能跟稀盐酸反应产生气体,且产生的气体是氢气。
化学性质:盐酸能与某些金属反应生成盐酸盐和氢气
在金属加工时,工人师傅常用稀硫酸或稀盐酸进行“钢铁酸洗”,以除去钢铁制品表面的铁锈,但酸洗的时间不能太长。这是怎么回事呢?
生活中我们都提倡使用铁锅炒菜。因为铁锅中有铁元素,如果在炒菜或煮东西时,加上醋,铁和酸反应,生成有铁离子的盐类,使铁元素更易融入菜中,人吃了饭菜就可以补充人体中的铁元素,可有效减少缺铁性贫血。有人做过试验,用铁锅炒洋葱,把油加热5分钟以后,洋葱里含铁量比原来提高一两倍。如果加上盐和醋后再同样加热5分钟,含铁量提高到原来的15到19倍。所以我们中国的铁锅可是世界有名的... ...
在用稀盐酸除铁锈时,酸不能太多,且放置时间也不能太长,不然稀盐酸会继续跟铁反应
实验室中可用稀盐酸来制取氢气
完成书本P15(1、3)
打开浓盐酸试剂瓶,发现瓶口有“白雾”出现.已知盐酸中含有水分子(H2O)、氢离子(H+)和氯离子(Cl-).下列实验能证明“白雾”中含有氢离子的是
A. ①③ B. ②④ C. ①②④ D. ①③④
电生磁PPT课件免费下载: 浙教版初中科学八年级下册课文《电生磁》,完整版PPT课件免费下载,优秀PPT背景图搭配,精美的免费ppt模板。轻松备课,欢迎免费下载使用。
月相PPT课件免费下载: 浙教版初中科学七年级下册课文《月相》,完整版PPT课件免费下载,优秀PPT背景图搭配,精美的免费ppt模板。轻松备课,欢迎免费下载使用。
电能PPT课件免费下载: 浙教版初中科学九年级上册课文《电能》,完整版PPT课件免费下载,优秀PPT背景图搭配,精美的免费ppt模板。轻松备课,欢迎免费下载使用。